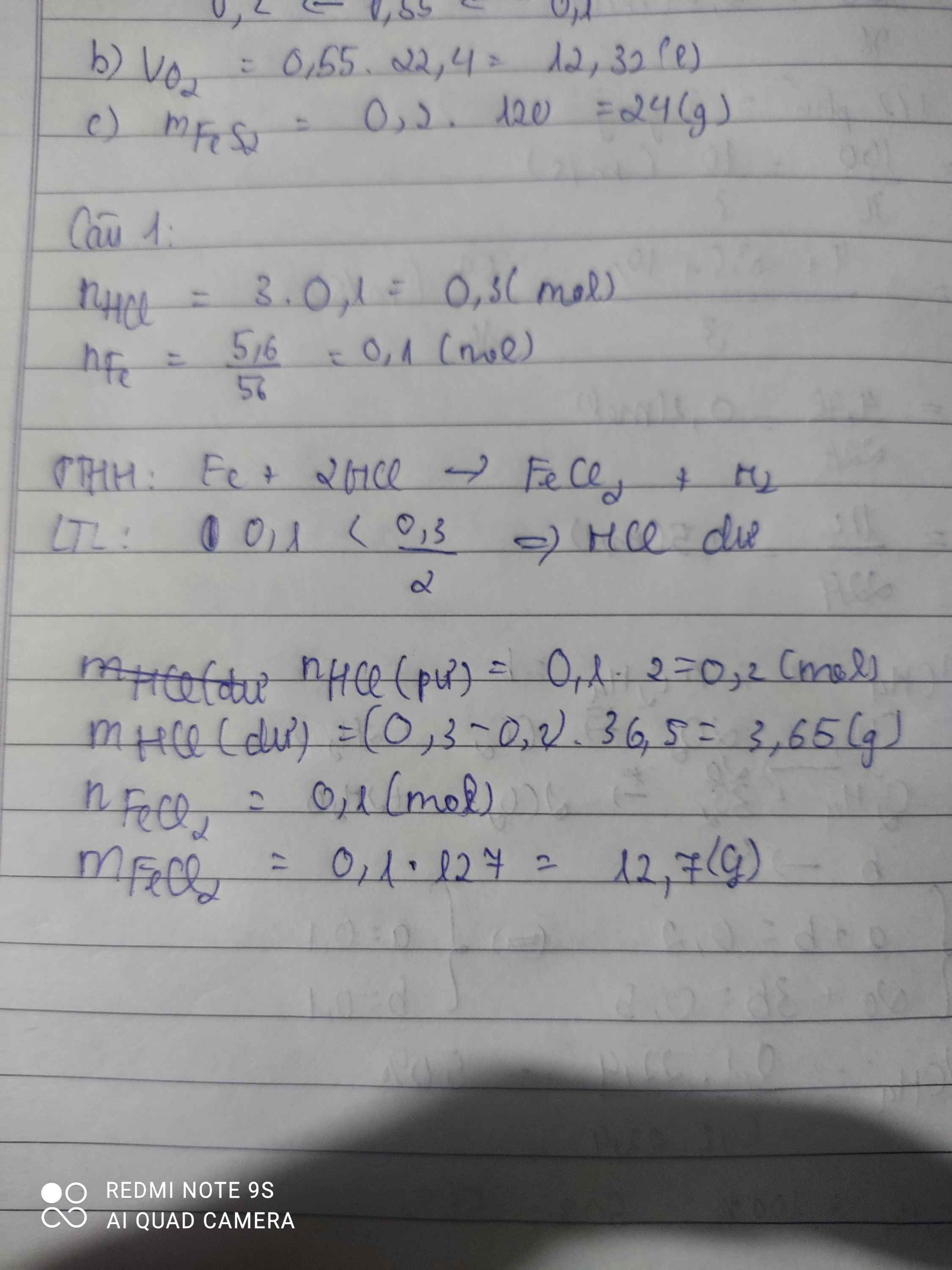Những câu hỏi liên quan
GIÚP EM BÀI NÀY VS Ạ GẮP LẮM R
Câu 1: Cho 100 ml dung dịch HCl 3M vào bình phản ứng chứa 5,6 gam Fe, phản ứng kết thúc thu được dung dịch A. Xác định khối lượng các chất có trong dd A. (Cho MH = 1,
MCl = 35,5, MFe = 56)
2HCl+Fe->FeCl2+H2
0,1----0,1 mol
n HCl=0,3 mol
n Fe=0,1 mol
=>HCl dư . dư 0,1 mol
=>m FeCl2=0,1.127=12,7g
=>m HCl dư=0,1.36,5=3,65g
Đúng 2
Bình luận (0)
Có 500 ml dung dịch X chứa các ion K+; Cl- và Ba2+. Lấy 100 ml dung dịch X phản ứng với dung dịch NaOH dư, kết thúc các phản ứng thu được 19,7 gam kết tủa. Lấy 100 ml dung dịch X tác dụng với dung dịch Ba(OH)2 dư, sau khi các phản ứng kết thúc thu được 29,55 gam kết tủa. Cho 200 ml dung dịch X phản ứng với lượng dư dung dịch AgNO3, kết thúc phản ứng thu được 28,7 gam kết tủa. Mặt khác, nếu đun sôi đến cạn 50 ml dung dịch X thì khối lượng chất rắn khan thu được là A. 23,700 gam B. 14,175 gam C....
Đọc tiếp
Có 500 ml dung dịch X chứa các ion K+; Cl- và Ba2+. Lấy 100 ml dung dịch X phản ứng với dung dịch NaOH dư, kết thúc các phản ứng thu được 19,7 gam kết tủa. Lấy 100 ml dung dịch X tác dụng với dung dịch Ba(OH)2 dư, sau khi các phản ứng kết thúc thu được 29,55 gam kết tủa. Cho 200 ml dung dịch X phản ứng với lượng dư dung dịch AgNO3, kết thúc phản ứng thu được 28,7 gam kết tủa. Mặt khác, nếu đun sôi đến cạn 50 ml dung dịch X thì khối lượng chất rắn khan thu được là
A. 23,700 gam
B. 14,175 gam
C. 11,850 gam
D. 10,062 gam
Đáp án C
Trong 100ml dd X có 0,1 mol Ba2+, 0,15 mol .
Trong 200ml dung dịch X có 0,2 mol Cl-.
Do đó trong 50 ml dung dịch X có 0,05 mol Ba2+, 0,075 mol , 0,05 mol Cl- và x mol K+
Theo định luật bảo toàn điện tích được x = 0,025
Khi cô cạn xảy ra quá trình:

Đúng 0
Bình luận (0)
Có 500 ml dung dịch X chứa các ion: K+, HCO3-, Cl- và Ba2+. Lấy 100 ml dung dịch X phản ứng với dung dịch NaOH dư, kết thúc các phản ứng thu được 19,7 gam kết tủa. Lấy 100 ml dung dịch X tác dụng với dung dịch Ba(OH)2 dư, sau khi các phản ứng kết thúc thu được 29,55 gam kết tủa. Cho 200 ml dung dịch X phản ứng với lượng dư dung dịch AgNO3, kết thúc phản ứng thu được 28,7 gam kết tủa. Mặt khác, nếu đun sôi đến cạn 50 ml dung dịch X thì khối lượng chất rắn khan thu được là A. 23,700 g. B. 14,17...
Đọc tiếp
Có 500 ml dung dịch X chứa các ion: K+, HCO3-, Cl- và Ba2+. Lấy 100 ml dung dịch X phản ứng với dung dịch NaOH dư, kết thúc các phản ứng thu được 19,7 gam kết tủa. Lấy 100 ml dung dịch X tác dụng với dung dịch Ba(OH)2 dư, sau khi các phản ứng kết thúc thu được 29,55 gam kết tủa. Cho 200 ml dung dịch X phản ứng với lượng dư dung dịch AgNO3, kết thúc phản ứng thu được 28,7 gam kết tủa. Mặt khác, nếu đun sôi đến cạn 50 ml dung dịch X thì khối lượng chất rắn khan thu được là
A. 23,700 g.
B. 14,175 g.
C. 11,850 g.
D. 10,062 g.
Trong 100ml dung dịch X có 0,1 mol Ba2+, 0,15 mol HCO3-
Trong 200ml dung dịch X có 0,2 mol Cl-
Do đó trong 50ml dung dịch X có 0,05 mol Ba2+, 0,075 mol HCO3- , 0,05 mol Cl- và x mol K+.
Theo định luật bảo toàn điện tích được x = 0,025.
Khi cô cạn xảy ra quá trình: 2HCO3- ⟶ CO32- + CO2 + H2O
Do đó: n C O 3 2 - = 0 , 0375
Vậy khối lượng chất rắn khan thu được là: m K + + m B a 2 + + m C O 3 2 - + m C l - = 11 , 85 ( g a m )
Đáp án C
Đúng 0
Bình luận (0)
Cho một lá sắt có khối lượng 5 gam vào 50 ml dung dịch CuSO 4 15% có khối lượng riêng là 1,12 g/ml. Sau một thời gian phản ứng, người ta lấy lá sắt ra khỏi dung dịch, rửa nhẹ, làm khô, cân nặng 5,16 gam. Tính nồng độ phần trăm các chất còn lại trong dung dịch sau phản ứng.
Khối lượng dung dịch CuSO 4 : m dd CuSO 4 = 1,12 x 50 = 56 (gam).
CuSO 4 + Fe → FeSO 4 + Cu
64x — 56x = 5,16 - 5 = 0,16 (gam) => x = 0,02 mol.
m CuSO 4 tham gia phản ứng = 0,02 x 160 = 3,2 (gam);
100 gam dung dịch CuSO 4 có 15 gam CuSO 4 nguyên chất.
56 gam dung dịch CuSO 4 có X gam CuSO 4 nguyên chất.
x = 56 x 15/100 = 8,4g; m CuSO 4 còn lại = 8,4 - 3,2 = 5,2g
m FeSO 4 = 0,02 x 152 = 3,04g
m dd sau p / u = 56 - 0,16 = 55,84g
C % CuSO 4 = 5,2/55,84 x 100% = 9,31%
C % FeSO 4 = 3,04/55,84 x 100% = 5,44%
Đúng 1
Bình luận (0)
Có 500 ml dung dịch X chứa các ion: K+,
H
C
O
3
-
,Cl – và Ba2+ . Lấy 100 ml dung dịch X phản ứng với dung dịch NaOH dư, kết thúc các phản ứng thu được 19,7 gamkết tủa. Lấy 100 ml dung dịch X tác dụng với dung dịch Ba(OH)2 dư, sau khi các phản ứng kết thúc thu được 29,55 gam kết tủa . Cho 200 ml dung dịch X phản ứng với lượng dư dung dịch AgNO3, kết thúc phản ứng thu được 28,7 gam kết tủa. Mặt khác, nếu đun sôi đến cạn 50...
Đọc tiếp
Có 500 ml dung dịch X chứa các ion: K+, H C O 3 - ,Cl – và Ba2+ . Lấy 100 ml dung dịch X phản ứng với dung dịch NaOH dư, kết thúc các phản ứng thu được 19,7 gamkết tủa. Lấy 100 ml dung dịch X tác dụng với dung dịch Ba(OH)2 dư, sau khi các phản ứng kết thúc thu được 29,55 gam kết tủa . Cho 200 ml dung dịch X phản ứng với lượng dư dung dịch AgNO3, kết thúc phản ứng thu được 28,7 gam kết tủa. Mặt khác, nếu đun sôi đến cạn 50 ml dung dịch X thì khối lượng chất rắn khan thu được là
A. 23,700 gam.
B. 14,175 gam.
C. 11,850gam
D. 10,062 gam.
Đáp án C
+ Lấy 100 ml dung dịch X phản ứng với dung dịch NaOH dư, kết thúc các phản ứng thu được 19,7 gam kết tủa⇒ n BaCO3 = n Ba2+ 0,1 mol . Lấy 100 ml dung dịch X tác dụng với dung dịch Ba(OH)2 dư, sau khi các phản ứng kết thúc thu được 29,55 gam kết tủa
⇒ n BaCO3- = n HCO3- = 0,15 mol
⇒ Trong 100ml ddX có 0,1 mol Ba2+ , 0,15 mol HCO3- .
+ Cho 200 ml dung dịch X phản ứng với lượng dư dung dịch AgNO3, kết thúc phản ứng thu được 28,7 gam kết tủa ⇒ Trong 200ml ddX có nCl- = n AgCl = 0,2 mol
⇒ Trong 50ml ddX có 0,05 mol Ba2+ ; 0,075 mol HCO3- , 0,05 mol Cl- ⇒ nK+ = 0,025
2HCO3- → CO32- + CO2 + H2O
0,075 → 0,0375 0,0375(mol)
Khi đun sôi đến cạn: mkhan = m HCO3- + m Ba2+ + m K+ + m Cl- - m CO2 – m H2O
= 0,05.137 + 0,075.61 + 0,05.35,5 + 0,025.39 – 0,0375.44 - 0,0375.18 = 11,85g
Đúng 0
Bình luận (0)
cho 1,96g bột sắt vào 100ml dung dịch CuSO4 10% có khối lượng riêng là 1,12 g/ml
a, viết PTHH
b, Xác định nồng độ mol của chất trong dung dịch khi phản ứng kết thúc. Giả thiết rằng thể tích dung dịch sau phản ứng thay đổi không đáng kể
giúp mình với ạaa
a, \(Fe+CuSO_4\rightarrow FeSO_4+Cu\)
b, \(n_{Fe}=\dfrac{1,96}{56}=0,035\left(mol\right)\)
\(m_{ddCuSO_4}=100.1,12=112\left(g\right)\)
\(\Rightarrow n_{CuSO_4}=\dfrac{112.10\%}{160}=0,07\left(mol\right)\)
Xét tỉ lệ: \(\dfrac{0,035}{1}< \dfrac{0,07}{1}\), ta được CuSO4 dư.
Theo PT: \(n_{CuSO_4\left(pư\right)}=n_{FeSO_4}=n_{Cu}=n_{Fe}=0,035\left(mol\right)\)
\(\Rightarrow n_{CuSO_4\left(dư\right)}=0,07-0,035=0,035\left(mol\right)\)
Ta có: m dd sau pư = 1,96 + 112 - 0,035.64 = 111,72 (g)
\(\Rightarrow\left\{{}\begin{matrix}C\%_{FeSO_4}=\dfrac{0,035.152}{111,72}.100\%\approx4,76\%\\C\%_{CuSO_4}=\dfrac{0,035.160}{111,72}.100\%\approx5,01\%\end{matrix}\right.\)
Đúng 2
Bình luận (0)
. Cho 2,8 gam bột Fe và 0,81 gam Al vào 100 ml dung dịch A chứa Cu(NO3)2 và AgNO3, khuấy kỹ đến khi phản ứng kết thúc. Sau phản ứng còn lại chất rắn B gồm 3 kim loại có khối lượng 8,12 gam. Cho chất rắn B tác dụng với dung dịch HCl dư thu được 0,672 lít H2 (ở đktc). Tính nồng độ mol của từng muối trong dung dịch A.
\(n_{Fe}=\dfrac{2,8}{56}=0,05mol\)
\(n_{Al}=\dfrac{0,81}{27}=0,03mol\)
\(B:8,12g\left\{{}\begin{matrix}Cu:a\left(mol\right)\\Ag:b\left(mol\right)\\Fe:c\left(mol\right)\end{matrix}\right.\Rightarrow64a+108b+56c=8,12\)(*)
\(n_{H_2}=\dfrac{0,672}{22,4}=0,03mol\)
\(Fe+2HCl\rightarrow FeCl_2+H_2\uparrow\)
0,03 0,03
\(\Rightarrow c=n_{Fe}=0,03mol\)
Thay vào (*) ta được: \(64a+108b=8,12-0,03\cdot56\left(1\right)\)
\(n_{Fepư}=0,05-0,03=0,02mol\)
\(BTe:2n_{Cu}+n_{Ag}=3n_{Fepư}+2n_{H_2}\)
\(\Rightarrow2a+b=2\cdot0,02+3\cdot0,03\left(2\right)\)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}a=0,05\\b=0,03\end{matrix}\right.\)
\(C_{M_{Cu\left(NO_3\right)_2}}=\dfrac{0,05}{0,1}=0,5M\)
\(C_{M_{AgNO_3}}=\dfrac{0,03}{0,1}=0,3M\)
Đúng 2
Bình luận (0)
a) Cho 2,25 gam hỗn hợp A gồm Al, Fe, Cu tác dụng với dung dịch HCl dư, sau khi phản ứng kết thúc thu được 1344 ml (đktc) khí và còn lại 0,6 gam chất rắn không tan. Tính % khối lượng mỗi kim loại trong A.
b) Hấp thụ hoàn toàn 1,344 lít SO2 ( đktc) vào 13,95 ml dung dịch KOH 28%, có khối lượng riêng là 1,147g/ml. Hãy tính nồng độ phần trăm các chất có trong dung dịch sau phản ứng
1) Ptpư:
2Al + 6HCl \(\rightarrow\) 2AlCl3 + 3H2
Fe + 2HCl \(\rightarrow\) FeCl2 + H2
Cu + HCl \(\rightarrow\) không phản ứng
=> 0,6 gam chất rắn còn lại chính là Cu:
Gọi x, y lần lượt là số mol Al, Fe
Ta có:
3x + 2y = 2.0,06 = 0,12
27x + 56 y = 2,25 – 0,6 = 1,65
=> x = 0,03 (mol) ; y = 0,015 (mol)
=> \(\%Cu=\frac{0,6}{2,25}.100\%=26,67\%\); \(\%Fe=\frac{56.0,015}{2,25}.100\%=37,33\%\); %Al = 36%
2) \(n_{SO_2}=\frac{1,344}{22,4}=0,06mol\); m (dd KOH) = 13,95.1,147 = 16 (gam)
=> mKOH = 0,28.16 = 4,48 (gam)=> nKOH = 0,08 (mol)=> \(1<\)\(\frac{n_{KOH}}{n_{SO_2}}<2\)
=> tạo ra hỗn hợp 2 muối: KHSO3: 0,04 (mol) và K2SO3: 0,02 (mol)
Khối lượng dung dịch sau pu = 16 + 0,06.64 = 19,84 gam
=> \(C\%\left(KHSO_3\right)=\frac{0,04.120}{19,84}.100\%\)\(=24,19\%\)
\(C\%\left(K_2SO_3\right)=\frac{0,02.158}{19,84}.100\%\)\(=15,93\%\)
Đúng 0
Bình luận (1)
Cho V ml dung dịch NaOH 0,1M vào 100 ml dung dịch Al2(SO4)3 0,1M, sau các phản ứng kết thúc, lọc lấy kết tủa nung đến khối lượng không đổi được 0,51 gam chất rắn. Giá trị lớn nhất của V là A. 500 B. 800 C. 300 D. 700
Đọc tiếp
Cho V ml dung dịch NaOH 0,1M vào 100 ml dung dịch Al2(SO4)3 0,1M, sau các phản ứng kết thúc, lọc lấy kết tủa nung đến khối lượng không đổi được 0,51 gam chất rắn. Giá trị lớn nhất của V là
A. 500
B. 800
C. 300
D. 700
Đáp án D
• 0,1V mol NaOH + 0,01 mol Al2(SO4)3 → ↓ Al(OH)3
Nung ↓ → 0,005 mol Al2O3
→ nAl(OH)3 = 0,01 mol.
• V lớn nhất khi NaOH dư
6NaOH + Al2(SO4)3 → 2Al(OH)3↓ + 3Na2SO4 (*)
NaOH + Al(OH)3 → NaAlO2 + 2H2O (**)
Theo (*) nNaOH = 0,01 × 6 = 0,06 mol; nAl(OH)3 = 0,01 × 2 = 0,02 mol.
Theo (**) nAl(OH)3 phản ứng = 0,02 - 0,01 = 0,01 mol
→ nNaOH = 0,01 mol
→ ∑nNaOH = 0,06 + 0,01 = 0,07 mol
→ VNaOH = 0,07 : 0,1 = 0,7 lít = 700 ml
Đúng 0
Bình luận (0)
Cho một lượng hỗn hợp X gồm Ba và Na vào 100 ml dung dịch Y gồm HCl 0,4M và FeCl3 0,3M. Kết thúc các phản ứng, thu được 1,12 lít khí (ở đktc) và m gam kết tủa. Giá trị của m là A. 2,675 B. 2,140 C. 1,070 D. 3,210
Đọc tiếp
Cho một lượng hỗn hợp X gồm Ba và Na vào 100 ml dung dịch Y gồm HCl 0,4M và FeCl3 0,3M. Kết thúc các phản ứng, thu được 1,12 lít khí (ở đktc) và m gam kết tủa. Giá trị của m là
A. 2,675
B. 2,140
C. 1,070
D. 3,210