Cho 6,5 gam Zn vào 200ml dung dịch CuSO4 10% có D = 1,12 g/ml.
a, Tính m chất rắn sau phản ứng.
b, Tính CM, C% dung dịch sau phản ứng
Mình cần gấp mngui ơii TvT
Cho 6,5 gam bột Zn vào dung dịch CuSO4 dư, sau phản ứng hoàn toàn thu được m gam chất rắn. Giá trị của m là:
A. 3,2.
B. 5,6.
C. 12,9.
D. 6,4.
cho 1,12 gam fe và 6,5 gam zn vào 200ml dung dịch y gồm Cu (NO3)2 tất cả hai 1M AgNO3 1M sau phản ứng thu được dung dịch a và chất rắn b xác định khối lượng chất rắn b .
cô cạn dung dịch thu (m) gam muối khan xác định m
12./ Cho 3,92 gam bột sắt vào 200ml dung dịch CuSO4 10% ( D= 1,12 g/ml ) .
a. Tính khối lượng kim loại mới tạo thành
b. Tính nồng độ mol của dung dịch sau phản ứng ( giả sử thể tích dung dịch thay đổi không đáng kể
Ta có: \(n_{Fe}=\dfrac{3,92}{56}=0,07\left(mol\right)\)
\(PTHH:Fe+CuSO_4--->FeSO_4+Cu\downarrow\)
a. Theo PT: \(n_{Cu}=n_{FeSO_4}=n_{Fe}=0,07\left(mol\right)\)
\(\Rightarrow m_{Cu}=0,07.64=4,48\left(g\right)\)
Ta có: \(V_{dd_{FeSO_4}}=V_{dd_{CuSO_4}}=\dfrac{200}{1000}=0,2\left(lít\right)\)
\(\Rightarrow C_{M_{FeSO_4}}=\dfrac{0,07}{0,2}=0,35M\)
Cho 6,5 gam bột Zn vào dung dịch CuSO4 dư, sau khi phản ứng xảy ra hoàn toàn thu được m gam chất rắn. Giá trị của m là
A. 12,9.
B. 3,2.
C. 6,4.
D. 5,6.
Cho 6,5 gam bột Zn vào dung dịch CuSO4 dư, sau khi phản ứng xảy ra hoàn toàn thu được m gam chất rắn. Giá trị của m là
A. 12,9.
B. 3,2.
C. 6,4.
D. 5,6.
Cho 6,5 gam bột Zn vào dung dịch CuSO4 dư, sau khi phản ứng xảy ra hoàn toàn thu được m gam chất rắn. Giá trị của m là
A. 12,9.
B. 3,2.
C. 6,4.
D. 5,6.
Cho 6,5 gam bột Zn vào dung dịch CuSO4 dư, sau khi phản ứng xảy ra hoàn toàn thu được m gam chất rắn. Giá trị của m là
A. 12,9
B. 3,2
C. 6,4
D. 5,6
Cho m gam bột Cu vào 200ml dung dịch AgNO3 0,2M, sau phản ứng thu được 3,88 gam chất rắn X và dung dịch Y. Cho 2,925 gam bột Zn vào dung dịch Y sau phản ứng thu được 5,265 gam chất rắn Z và dung dịch chỉ chứa 1 muối duy nhất. Giá trị của m là
A. 3,17
B. 2,56
C. 1,92
D. 3,2.
n A g N O 3 = 0 , 2 . 0 , 2 = 0 , 04
Thông thường, khi đọc xong đề bài các bạn sẽ viết các phản ứng:
Cu + 2AgNO3⟶Cu(NO3 )2 + 2Ag
Zn + Cu(NO3)2 ⟶ Zn(NO3)2 + Cu
Zn + 2AgNO3 ⟶ Zn(NO3)2 +2Ag.
Tuy nhiên phản ứng giữa Cu và AgNO3 ta không thể biết được chất nào dư, chất nào hết, do đó nếu làm theo cách bình thường ta sẽ thử xét 2 trường hợp, nhưng khi cho Zn vào dung dịch Y thì thì ta cũng không biết được chất nào dư, chất nào hết.
Do đó nếu nhìn theo cách bình thường thì bài toán trở nên rất phức tạp.
Tuy nhiên đọc lại đề bài 1 lần nữa, ta thấy có một giả thiết quan trọng là “dung dịch chỉ chứa 1 muối duy nhất”, đây chính là nút thắt của bài toán.
Dễ thấy dung dịch sau phản ứng chỉ chứa muối Zn(NO3)2
⇒ Tất cả ion sẽ đi hết vào muối Zn(NO3)2.
![]()
Khi ta không biết rõ chất nào dư hay hết, phản ứng đã xảy ra hoàn toàn hay chưa thì chúng ta nên nghĩ đến định luật bảo toàn khối lượng:
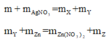
Cộng vế theo vế 2 phương trình trên ta được:
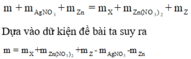
Hay m = 3,88 + 0,02.189 + 5,265 - 0,04.170 - 2,925 = 3,2 gam.
Đáp án D.
Cho 6,5 gam Zn vào 200ml dung dịch H2SO4 1M.
a hỏi chất nào dư sau phản ứng? dư bn mol?
b tính khối lượng muối tạo thành
c tính nồng độ mol của các chất trong dung dịch sau p/ứ. coi thể tích dd không thay đổi
PT: \(Zn+H_2SO_4\rightarrow ZnSO_4+H_2\)
a, Ta có: \(n_{Zn}=\dfrac{6,5}{65}=0,1\left(mol\right)\)
\(n_{H_2SO_4}=0,2.1=0,2\left(mol\right)\)
Xét tỉ lệ: \(\dfrac{0,1}{1}< \dfrac{0,2}{1}\). ta được H2SO4 dư.
Theo PT: \(n_{H_2SO_4\left(pư\right)}=n_{ZnSO_4}=n_{Zn}=0,1\left(mol\right)\)
\(\Rightarrow n_{H_2SO_4\left(dư\right)}=0,2-0,1=0,1\left(mol\right)\)
b, Ta có: \(m_{ZnSO_4}=0,1.161=16,1\left(g\right)\)
c, \(C_{M_{H_2SO_4\left(dư\right)}}=\dfrac{0,1}{0,2}=0,5M\)
\(C_{M_{ZnSO_4}}=\dfrac{0,1}{0,2}=0,5M\)
Bạn tham khảo nhé!