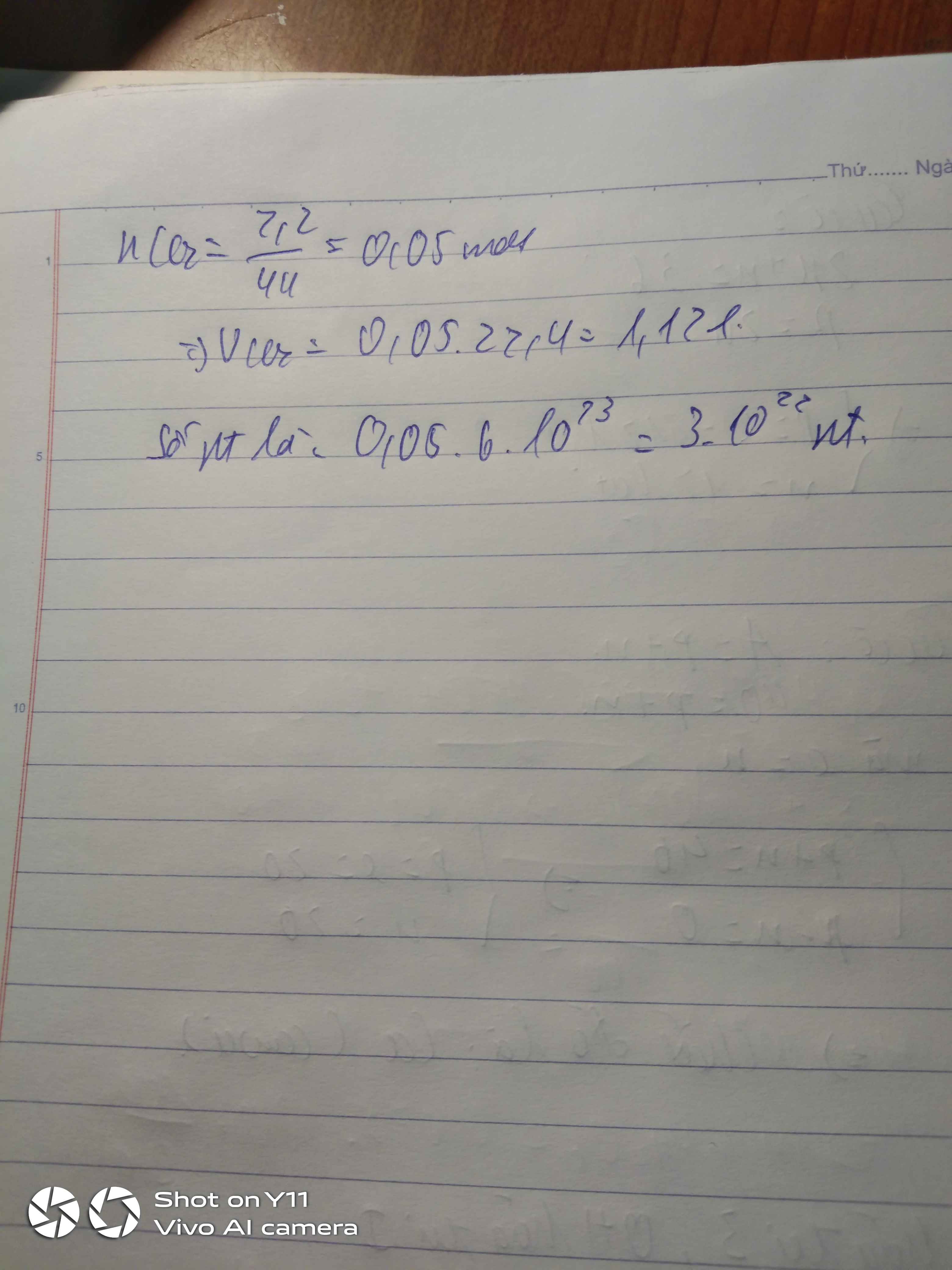cho nguyên tử khoiis H: 1; C:12; N:14;O:16;Na:23;P:31;S:32;Cl:35,5;Ca:40;Zn:65 tính thể tích của các chất ở đktc a) 0,05mol khí ozon (O3) B) 6,6g CO2 C) 10g SO3

Những câu hỏi liên quan
Cho 10g CaCO3 tác dụng với dung dịch HCL dư. a,Tính thể tích khí CO2 thu được ở đktc. b,Dẫn khí CO2 thu được vào lọ đựng 25g dung dịch NaOH 40%. Tính khối lượng muối cacbonnat thu được. (biết Ca=40, C=12, O=16, H=1, Na=23, Cl=35,5)
a) CaCO3+2HCl=>CaCl2+H2O+CO2
n CaCO3=10/100 = 0,1 mol
theo phương trình : n CO2 = n CaCO3 = 0,1 mol
=> V CO2 = 0,1*22,4 = 2,24 lít
b) CO2+2NaOH => Na2CO3+H2O
có thể xảy ra phản ứng :
Na2CO3+CO2+H2O=>2NaHCO3
m NaOH = 25*0,4 = 10 gam
=> n NaOH = 10/40 = 0,25 mol
mà nếu theo phương trình đầu tiên của câu b:
n CO2 = 1/2 n NaOH = 1/2*0,25 = 0,125 mol
mà thực tế n CO2 có 0,1 mol
=> n CO2 hết, n NaOH dư
=> chỉ tạo ra 1 muối là Na2CO3
n Na2CO3 = n CO2 = 0,1 mol
=> m Na2CO3 = 0,1*106=10,6 gam
Đúng 1
Bình luận (0)
câu 1 : cho 12 gam cacbon (C) cháy trong o khí oxi (O2) , sau phản ứng thu được khí cacbon điôxit (co2)a, lập phương trình phản ứng ?b, tính khối lượng oxi tham gia phản ứng và thể tích khí co2 sinh ra ở (đktc)cho biết : C12 ; O 16câu 2 : phân tử khối là khối lươngh của một phân tử tính bằng đơn vị cacbon (đvc)phân tử khối của một chất bằng tổng nguyên tử khối của các nguyên tử trong phân tử chất đó.hãy tính phân tử khối của các chất sau:o2 , h2o, co2 , so3 , scl , h2so4, al2(so4)3(biết 016 , h1...
Đọc tiếp
câu 1 : cho 12 gam cacbon (C) cháy trong o khí oxi (O2) , sau phản ứng thu được khí cacbon điôxit (co2)
a, lập phương trình phản ứng ?
b, tính khối lượng oxi tham gia phản ứng và thể tích khí co2 sinh ra ở (đktc)
cho biết : C=12 ; O =16
câu 2 : phân tử khối là khối lươngh của một phân tử tính bằng đơn vị cacbon (đvc)
phân tử khối của một chất bằng tổng nguyên tử khối của các nguyên tử trong phân tử chất đó.
hãy tính phân tử khối của các chất sau:
o2 , h2o, co2 , so3 , scl , h2so4, al2(so4)3
(biết 0=16 , h=1 ; c=12 ;s=32; cl=35,5 ; al=27)
Ai biết làm giúp mình với thanks nhiều lắm
CÂU 1:
a) C + O2 → CO2
b) nC= \(\frac{m}{M}\) = \(\frac{12}{12}\) = 1 mol
C + O2 → CO2
1mol→1mol→1mol
mO2=n.M=1. (16.2)=32g
VCO2= n.22,4=1.22,4=22,4 l
CÂU 2:
MO2= 16.2=32 g/mol
MH2O= 1.2+16=18g/mol
MCO2= 12+16.2=44g/mol
MSO3=32+16.3=80g/mol
MSCl=32+35,5=67,5g/mol
MH2SO4=1.2+32+16.4=98g/mol
MAl2(SO4)3=27.2+(32+16.4).3=342g/mol
Mình cũng chẳng biết bạn có hiểu không nữa vì mỗi trường mỗi cô có cách giảng khác nhau mà. Tạm hiểu nha nhưng mình chắc đúng 100% đấy
Đúng 0
Bình luận (0)
Bài 2
PTK của O2= 16 \(\times\) 2 = 32 ( đvC)
PTK của : H2O= \(1\times2+16\) =18 ( đvC)
PTk của : SO3= \(32+16\times3\) = 80 ( đvC)
PTK của : SCl = 32 + 35,5 =67.5 ( đvC )
PTK của : H2SO4 =\(1\times2+32+16\times4\)= 98 ( đvc )
PTK của : Al2(SO4)3=\(27\times2+\left(32+16\times4\right)\times3\)= 362 ( đvC)
chúc bạn học tốt <3
Đúng 0
Bình luận (1)
Cho 14 gam sắt tác dụng với dung dịch HCl, sau phản ứng thu được khí hidro và FeCl2 .
a) Viết PTHH.
b) Tính khối lượng HCl cần dùng.
c)Tính thể tích khí thu được(đktc)
(Cho biết nguyên tử khối: H=1, O=16, C=12, Na =23, Fe=56, Cl=35,5, S =32, Al=27, Zn= 65)
Mình cần gấp ạ^^
nFe = \(\dfrac{14}{56}\) = 0,25 (mol)
a) Fe + 2HCl → FeCl2 + H2
b) Theo phương trình phản ứng, ta có
nFe = 2nHCl = 2.0,25 = 0,5 (mol)
=> mHCl = 0,5.36,5= 18,25 (mol)
c) Theo phương trình phản ứng, ta có:
nFe = nH2 = 0,25 (mol)
=> VH2= 0,25.22,4 = 5,6 (lít)
Đúng 0
Bình luận (0)
10/. Cho 30,6 gam hỗn hợp Na2CO3 và CaCO3 tác dụng với 1 lượng vừa đủ dd HCl 20% ,
tạo thành 6,72 lít chất khí (đktc) và 1 dd A
a/. Tính khối lượng mỗi chất trong hỗn hợp.
b/. Tính nồng độ % các chất trong dung dịch A.
( cho Na = 23, K = 39, Mg = 24, Ca = 40, Fe = 56, Cu = 64, Zn = 65, Ag = 108, H = 1, C =
12, N = 14, O = 16, Cl = 35,5, S = 32)
a)Na2CO3+2HCl--->2NaCl+H2O+CO2
x------------------------------------------------x-
CaCO3+2HCl--->CaCl2+H2O+CO2
y-----------------------------------------y
Ta có n CO2=6,72/22,4=0,3(mol)
Theo bài ra ta có hpt
\(\left\{{}\begin{matrix}106x+100y=30,6\\x+y=0,3\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}x=0,1\\y=0,2\end{matrix}\right.\)
%m Na2CO3=0,1.106/30,6.100%=34,64%
%m CaCO3=100%-34,64%=65,36%
b) n HCl=2n CO2=0,6(mol)
m HCl=0,6.36,5=21,9(g)
m dd HCl=21,9.100/20=109,5(g)
m dd sau pư=m hh+m dd HCl-m CO2
=30,6+109,5-18=122,1(g)
%m NaCl=0,2.58,5/122,1.100%=9,58%
%m CaCl2=0,2.111/122,1.100%=18,18%
n
giup minh voi minh cam on a
10)
a) PTHH: Na2CO3 + 2 HCl -> 2 NaCl + H2O + CO2
x_____________2x______2x________x__x(mol)
CaCO3 + 2 HCl -> CaCl2 +H2O + CO2
y_________2y______y_y_________y(mol)
nCO2= x+y=6,72/22,4=0,3 (1)
mNa2CO3 + mCaCO3= mhh
<=> 106x+100y= 30,6 (2)
từ (1)., (2) có hpt:
\(\left\{{}\begin{matrix}x+y=0,3\\106x+100y=30,6\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}x=0,1\\y=0,2\end{matrix}\right.\)
=> mNa2CO3= 0,1. 106 =10,6(g)
=> \(\%mNa2CO3=\frac{10,6}{30,6}.100\approx34,641\%\\ \Rightarrow\%mCaCO3\approx100\%-34,641\%\approx65,359\%\)
b) nHCl= 2x+2y= 2.0,1+2.0,2=0,6(mol)
=> mHCl= 0,6.36,5= 21,9(g)
=> mddHCl= (21,9.100)/20= 109,5(g)
=> mddsau= m(hh)+ mddHCl - mCO2= 30,6+109,5 - 0,3.44= 126,9(g)
mNaCl= 2x.58,5= 2.0,1.58,5= 11,7(g)
mCaCl2= 2y.111= 2.0,2.111= 44,4(g)
=> \(C\%ddNaCl=\frac{11,7}{126,9}.100\approx9,22\%\\ C\%ddCaCl2=\frac{44,4}{126,9}.100\approx34,988\%\)
Cho biết ở (đktc ) , nếu lấy khí CÒ và khí CLo với thể tich bằng nhau thì khối lượng và số nguyên tử của 2 khí này có = nhau không ( giải thich )
Cho biết AL= 27 , Cl =35,5 , C=12 , O = 16 , Na =23 , S = 32
gọi số mol của Cl2 là n (mol)
vì thể tích của CO và Cl2 bằng nhau (cùng ở ĐKTC) nên số mol của chúng bằng nhau:=> nCO=nCl2=n(mol)
ta có: +) NCO = n.6.1023 (nguyên tử)
+)NCl2 = n.6.1023 (nguyên tử)
=>NCO=NCl2
Vậy số nguyên tử của CO và Cl2 bằng nhau
Đúng 0
Bình luận (0)
cho 4.6 gam kim loại A hóa trị I vào nước thấy thoát ra 2.24 lít khí hiđro (đktc). Xác định kim loại A
(biết o=16,c=12,h=1,s=32,cu=64,p=31,zn=65,fe=56,na=23,cl=35.5)
\(n_{H_2}= \dfrac{2,24}{22,4} = 0,1(mol)\\ 2A + 2H_2O \to 2AOH + H_2\\ n_A = 2n_{H_2} = 0,2(mol)\\ \Rightarrow M_A = \dfrac{4,6}{0,2} = 23(Natri)\)
Đúng 2
Bình luận (0)
Bài 4: Một hỗn hợp X gồm 1,5 mol khí O2; 2,5 mol khí N2; 1,2.1023 phân tử H2 và 6,4 g khí SO2.
a) Tính thể tích của hỗn hợp khí X ở đktc.
b) Tính khối lượng của hỗn hợp khí X .
(Cho C =12, O =16, H =1, N =14, S =32, Cu =64, Ca =40, Zn =65, Ba =137, K =39, Al=27)
\(a.n_{H_2}=\dfrac{1,2.10^{23}}{6.10^{23}}=0,2\left(mol\right)\\ n_{SO_2}=\dfrac{6,4}{64}=0,1\left(mol\right)\\ V_X=\left(1,5+2,5+0,2+0,1\right).22,4=96,32\left(l\right)\\b. m_X=1,5.32+2,5.28+0,2.2+6,4=124,8\left(g\right)\)
Đúng 2
Bình luận (0)
a.nH2=1,2.10236.1023=0,2(mol)nSO2=6,464=0,1(mol)VX=(1,5+2,5+0,2+0,1).22,4=96,32(l)b.mX=1,5.32+2,5.28+0,2.2+6,4=124,8(g)
Đúng 0
Bình luận (0)
Hòa tan hoàn toàn 9,6 gam kim loại R trong axit H2SO4 đặc, nóng, tạo ra 3,36 lít khí A ở điều kiện tiêu chuẩn. Xác định kim loại R, biết khí A có tỉ khối so với khí hidro là 32.( cho Na=23; Al=27; Zn=65; Fe=56; Cu=64; Ca= 40; C=12; O=16; Cl=35,5 ). Cần giúp đỡ nhanh ạ !!
MA = 32.2 = 64(g/mol) ⇒ A là SO2
nSO2 = 0,15(mol)
Gọi n là hóa trị của kim loại R
Bảo toàn electron , ta có : n.nR = 2nSO2 = 0,3
⇒ nR = \(\dfrac{0,3}{n}\) mol
⇒ R = \(\dfrac{9,6}{\dfrac{0,3}{n}} = 32n\)
Với n = 2 thì R = 64(Cu)
Vậy kim loại R là Cu
Đúng 1
Bình luận (0)
Tính thể tích ở đktc và số phân tử của 2,2 gam khí CO2. Cho nguyên tử khối: O=16, Cu=64, Mg=24, Fe=56, Cl=35,5, Ag =108, N=14.