Để đốt cháy hết 1,6(g) hợp chất Y cần dùng 1,2.1023 phân tử oxi, thu được khí CO2 và hơi nước theo tỉ lệ số mol là 1 : 2.
1. Tính khối lượng CO2 và hơi nước tạo thành.
2. Tìm công thức phân tử của Y, biết tỉ khối của Y đối với H2 là 8.
để đốt cháy hết 1,6 gam hợp chât Y cần dùng 1,2.10^23 phân tử oxi , thu được khí co2 và hơi nước theo tỉ lệ số mol là 1:2 . a.tính khối lượng khí co2 và hơi nước tạo thành
b. tính cthh của Y, biết tỉ khối của Y đối vs Hidro là 8
Để đốt cháy hết 1.6g hợp chất Y cần dùng 1.2.10^23 phân tử oxi, thu được khí CO2 và hơi nước theo tỉ số mol là 1:2
a)Tìm khối lượng khí CO2 và hơi nước tạo thành
b)Tìm CTPT của Y biết tỉ khối của Y đối với H2=8
nO2= 0,2 mol.
m O2= 6,4 gam
=> tổng m H2O + CO2= 1,6 + 6,4= 8 gam .
gọi a là nCO2 => 2a là nH2O. ta có :
44a + 36a= 8 => a= 0,1 mol
=> mCO2= 4,4 gam
=>mH2O= 3,6 gam
b. nCO2= 0,1 mol => nC= 0,1 mol
nH2O= 0.2 mol => nH= 0,4 mol
nC:nH= 1:4 =>CTPT có dạng (CH4)n.
vì M_Y= 16 <=> 16n=>n=1. => CTPT của Y là CH4.
Để đốt cháy hết 1.6g hợp chất Y cần dùng 1.2.10^23 phân tử oxi, thu được khí CO2 và hơi nước theo tỉ số mol là 1:2
a)Tìm khối lượng khí CO2 và hơi nước tạo thành
b)Tìm CTPT của Y biết tỉ khối của Y đối với H2=8
nO2= 0,2 mol.
m O2= 6,4 gam
=> tổng m H2O + CO2= 1,6 + 6,4= 8 gam .
gọi a là nCO2 => 2a là nH2O. ta có :
44a + 36a= 8 => a= 0,1 mol
=> mCO2= 4,4 gam
=>mH2O= 3,6 gam
b. nCO2= 0,1 mol => nC= 0,1 mol
nH2O= 0.2 mol => nH= 0,4 mol
nC:nH= 1:4 =>CTPT có dạng (CH4)n.
vì M_Y= 16 <=> 16n=>n=1. => CTPT của Y là CH4.
câu 1
để đốt cháy 3,2g hỗn hợp chấy Y cần dùng 2,4.1023 phân tử oxi , thu dc khí CO2 và hơi nc theo tỉ lệ mol là 1/2
a) tính khối lượng khí CO2 và hơi nc tạo thành
b) tính CT phân tử của Y biết tỉ khối của Y đối với H2 bằng 8
câu 2
dùng khí CO để khử hoàn toàn 20g một hỗn hợp (hỗn hợp Y) gồm CuO và Fe2O3 ở nhiệt độ cao . sau phản ứng , thu dc chất rắn chỉ là các kim loại , lượng kim loại này dc cho phản ứng cới dung dịch H2SO4 loãng ( lấy dư ) , thì thấy có 3,2 gam một kim loại màu đỏ 0 tan
a) rính phần trăm khối lượng các chất có trong hỗn hợp Y
b) nếu dùng khí sản phẩm ở các phản ứng khử Y , cho đi qua dung dịch Ca(OH)2 dư thì thu dc bao nhiêu gam kết tủa . biết hiệu suất của phản ứng này chỉ đạt 80%
câu 3
1) xác định độ tan cuẩ Na2CO3 trong nc ở 18oc . biết ở nhiệt đọ này , khi hòa tan hết 143g muối Na2CO3 . 10 H2O trong 160g nc thì dc dung dịch bão hòa
2) cho hỗn hợp khí X gồm CO2 và N2 (ở dktc) có tỉ khối đối với khí oxi là 1,255
a) tính thành phần phần trăm theo thể tích của mỗi khí trong hỗn hợp X
b) tính khối lượng của 1 lít hỗn hợp khí X ở dktc
câu 4
một hỗn hợp gồm Zn và Fe có khối lượng 18,6 gam . hòa tan hốn hợp này trong 500ml dung dịch axit H2SO4 1M
1) chứng tỏ rằng hỗn hợp này tan hết
2) nếu dùng một lượng hốn hợp Zn và Fe gấy đôi trường hợp trc , lượng H2SO4 vẫn như cũ thì hỗn hợp này có tan hết 0
3) trong trường hợp 1) hãy tính khối lượng mỗi kim loại có trong hỗn hợp biết rằng lượng H2 sinh ra trong phản ứng tác dung vừa đủ với 24g CuO
Để đốt cháy 16g một chất X cần dùng 44,8 lít khí Oxi(đktc ) thu được khí CO2 và hơi nước theo tỷ lệ mol là 2 : 1 .Tính khối lượng khí CO2 và khối lượng H2O tạo thành.
nO2 = 44,8 : 22,4 = 2 (l)
pthh X + O2 -->2 CO2 +H2O
2---> 4-------> 2 (mol)
=> mCO2 = 4 . 44 = 176(g)
=> mH2O = 2.18 = 36 (g)
Gọi nH2O = a (mol)
=> nCO2 = 2a (mol)
mH2O = 18a (g)
mCO2 = 2a . 44 = 88a (g)
nO2 = 44,8/22,4 = 2 (mol)
mO2 = 2 . 32 = 64 (g)
Áp dụng ĐLBTKL, ta có:
mX + mO2 = mH2O + mCO2
=> 16 + 64 = 18a + 88a
=> a = 40/53 (mol)
mCO2 = 88 . 40/53 = 3520/53 (g)
mH2O = 18 . 40/53 = 720/53 (g)
Đốt cháy 16g chất A cần 4,48 lít khí oxi (đktc) thu được khí CO2 và hơi nước theo tỉ lệ số mol là 1 : 2 . Tính khối lượng CO2 và H2O tạo thành?
TK:
https://lazi.vn/edu/exercise/452918/dot-chay-16g-chat-a-can-4-48-lit-khi-oxi-o-dktc-thu-duoc-khi-co2-va-hoi-nuoc-theo-ti-le-so-mol-la-1-2-tinh-khoi-luong
Đốt cháy hoàn toàn a(g) hợp chất X cần dùng 44,8 lít khí oxi (đktc) thu được V (lít) khí CO2 và b(g) nước. Cho b(g) hơi nước tác dụng hết với 124g Na2O. Tìm a biết khí CO2 và hơi nước tạo thành theo tỉ lệ số mol là 1:1
Ta cÓ PTHH :
H2O + Na2O \(\rightarrow\) 2NaOH
nNa2O = m/M = 124/62 = 2 (mol)
TheO PT : => nH2O = nNa2O = 2(mol)
Vì nCO2 : nH2O =1:1 => nCO2 = nH2O = 2(mol)
Do đó: mCO2 = n .M = 2 . 44 =88(g) và mH2O = n .M = 2 .18 =36(g)
nO2 = V/22.4 = 44.8/22.4 = 2(mol)
=> mO2 = n .M = 2 x 32 = 64(g)
Theo ĐLBTKL : mX + mO2 = mCO2 + mH2O
=> a + 64 = 88 + 36
=> a =60 (g)
Hỗn hợp X chứa ba chất hữụ cơ đồng phân. Nếu làm bay hơi 2,10 g X thì thể tích hơi thu được bằng thể tích của 1,54 g khí C O 2 ở cùng điều kiện. Để đốt cháy hoàn toàn 1,50 g X cần dùng vừa hết 2,52 lít O 2 (đktc). Sản phẩm cháy chỉ có C O 2 và H 2 O theo tỉ lệ 11 : 6 về khối lượng.
1. Xác định công thức phân tử của ba chất trong X.
2. Dựa vào thuyết cấu tạo hoá học, hãy viết công thức cấu tạo (triển khai và rút gọn) của từng chất đó.
Ba chất đồng phân có công thức phân tử giống nhau. Đốt X ta chỉ được C O 2 và H 2 O , vậy các chất trong X có chứa C, H và có thể có chứa O.
Theo định luật bảo toàn khối lượng :
m C O 2 + m H 2 O = m X + m O 2 = 5,1(g)
Mặt khác mCO2: mH2O = 11:6
Từ đó tìm được: m C O 2 = 3,30 g và m H 2 O = 1,80 g
Khối lượng C trong 3,30 g
C
O
2
: 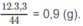
Khối lương H trong 1,80 g
H
2
O
: 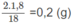
Khối lượng O trong 1,50 g X : 1,50 - 0,9 - 0,2 = 0,4 (g).
Các chất trong X có dạng C x H y O z
x : y : z = 0,075 : 0,2 : 0,025 = 3 : 8 : 1.
Công thức đơn giản nhất là C 3 H 8 O .
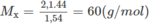
⇒ CTPT cũng là C 3 H 8 O .
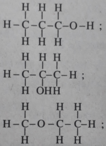
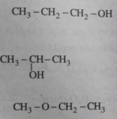
Để đốt cháy hết 16 g hợp chất X cần 44,8 lít khí oxi (điều kiện tiêu chuẩn) . Sau khi kết thúc phản ứng chỉ thu được CO2 và hơi nước theo tỉ lệ số mol là 1 : 2 . Xác định công thức hóa học của x biết công thức đơn giản chính là công thức hóa học
Gọi số mol CO2, H2O là a, b
=> 2a = b
\(n_{O_2}=\dfrac{44,8}{22,4}=2\left(mol\right)\)
Theo ĐLBTKL: 44a + 18b = 16 + 2.32 = 80
=> a = 1; b = 2
Bảo toàn C: nC = 1(mol)
Bảo toàn H: nH = 4 (mol)
Xét mC + mH = 1.12 + 4.1 = 16(g)
=> X chỉ chứa C và H
nC : nH = 1 : 4
=> CTPT: CH4