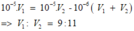Tính tỉ lệ V1 : V2
a/ Trộn V1 (ml) dd HNO3 (pH = 1) với V2 (ml) dd HNO3 (pH = 3) để được dd có pH = 2.
b/ Pha thêm V1(ml) nước vào V2 (ml) dd NaOH (pH = 13) để được dd có pH = 12
Bài 3. Dung dịch A gồm NaOH 0,08M và Ba(OH)2 0,02M. Dung dịch B gồm HCl 0,05M và H2SO4 0,06M
Trộn V1 ml dd A với V2 ml dd B thu được dd có pH = 13. Tính tỉ lệ V1 : V2
\(n_{OH^-}=0,12V_1\)
\(n_{H^+}=0,17V_2\)
\(n_{OH^-dư}=\left(V_1+V_2\right).10^{-1}\)
Ta có:
\(n_{OH^-dư}+n_{H^+}=n_{OH^-}\)
\(\Leftrightarrow\left(V_1+V_2\right).10^{-1}=0,12V_1\)
\(\Leftrightarrow0,1V_1=0,02V_2\)
\(\Rightarrow\dfrac{V_1}{V_2}=\dfrac{1}{5}\)
Dung dịch A gồm NaOH 0,08M và Ba(OH)2 0,02M. Dung dịch B gồm HCl 0,05M và H2SO4 0,06M
Trộn V1 ml dd A với V2 ml dd B thu được dd có pH = 7. Tính tỉ lệ V1 : V2
\(pH=7\Rightarrow n_{H^+}=n_{OH^-}\)
\(\Leftrightarrow\left(0,05+0,06.2\right)\text{}V_2=\left(0,08+0,02.2\right)V_1\)
\(\Rightarrow V_1:V_2=17:12\)
Trộn lẫn V1 ml dd NaOH 3% có D=1,05g/ml và V2 ml dd NaOH 10%, D= 1,12g/ml để pha chế được 2 lít dd NaOH 8% có khối lượng riêng là 1,1g/ml. Tính V1 và V2
1.
Nồng độ mol/lit của đ NaOH(1)=\(\dfrac{3.10.1,05}{40}\)=0.7875
......................................... khi trộn là: =\(\dfrac{8.10.1,1}{40}\)=2.2
Áp dụng quy tắc đường chéo ta có
Vdd1/(2-Vdd1)=0.42477
---> Vdd1=0.6l
Vdd2=1.4l
Có V1 ml HCl ( pH = 2 ). Cần thêm V2 ml H2O để được dd HCl mới có pH = 3. Quan hệ V1 và V2 là :
A. V2 = 9 V1
B. V2 = 10 V1
C. V2 = V1
D. V1 = 9V2
Đáp án A
pH lúc sau = 3 ⇒ [H+] đầu = 10[H+]M lúc sau
⇒ V2 + V1 = 10V1 ⇒ V2 = 9V1
Đáp án A.
Trộn v1 ml dd hcl 0.1M và h2so4 0.05M với v2 dd naoh 0.1M với ba(oh)2 0.1M thu đc dd A có thể tích 1 lít ph= 12 tính v1 v2
Trộn v1 ml dd HCl 10M với V2 ml nước được 40ml dd HCl 2M . Tính v1 và v2?
nHCl(cuối)=0,04.2=0,08(mol)
Ta có: 10V1=0,08
<=>V1=0,008(l)=8(ml)
Mặt khác: V1+V2=40
<=>8+V2=40
<=>V2=32(ml)
Vậy: V1=8(ml); V2=32(ml)
Chúc em học tốt!
13. Trộn 300ml dd HCl 0,1M vào 200ml dd H2SO4 0,05M thì thu đc dd X có pH là a. Giá trị của a là?
16. Trộn V1(ml) dd HCl 0,001M vào V2(ml) dd H2SO4 0,05M thì thu đc 100ml dd có pH bằng 1,153. Giá trị V1 và V2 lần lượt là?
C1
nH2SO4 = 0,2.0,05 = 0,01 mol
nHCl = 0,3.0,1 = 0,03 mol
=> nH+ = 2nH2SO4 + nHCl = 2.0,01 + 0,03 = 0,05 mol
=> [H] = n/V = 0,05/(0,2 + 0,3) = 0,1
=> pH = -log[H+] = -log(0,1) = 1
Trộn V 1 ml dung dịch NaOH có pH = 13 với V 2 ml dung dịch Ba OH 2 có pH = 11, thu được dung dịch mới có pH = 12. Tỉ số V 1 : V 2 có giá trị là
A. 1/1
B. 2/1
C. 1/10
D. 10/1
Phải lấy dd HCl (V1) có pH = 5 cho vào dd KOH (V2) có pH = 9 theo tỷ lệ thể tích V1:V2 là bao nhiêu để được dd có pH = 8
A. 99 : 101
B. 101 : 99
C. 11 : 9
D. 9:11
Đáp án D
Cách 1: pH=8 => KOH dư
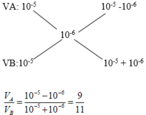
Cách 2: Do O H - dư nên ta có: