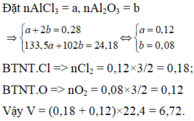1. Đốt cháy hoàn toàn 11.9 gam hỗn hợp gồm nhôm và kẽm cần dùng 4,48 lít khí
O2 (đktc).
Theo phản ứng: Al + O2 ⎯⎯to→ Al2O3; Zn + O2 ⎯⎯to→ ZnO. Tính khối lượng
mỗi chất có trong hỗn hợp ban đầu?

Những câu hỏi liên quan
2. Để đốt cháy hết 13,2 gam hỗn hợp gồm bột Fe và Mg cần dùng hết 4,48 lít khí
O2 (đktc) tạo ra sản phẩm là Fe3O4 và MgO theo phản ứng:
Fe + O2 ⎯⎯to→ Fe3O4; Mg + O2 ⎯⎯to→ MgO Tính khối lượng mỗi chất có
trong hỗn hợp ban đầu?
Gọi x, y lần lượt là số mol của Fe và Mg.
Theo đề, ta có: \(56x+24y=13,2\) (*)
Ta có: \(n_{O_2}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\)
PTHH:
\(3Fe+2O_2\overset{t^o}{--->}Fe_3O_4\left(1\right)\)
\(2Mg+O_2\overset{t^o}{--->}2MgO\left(2\right)\)
Theo PT(1): \(n_{O_2}=\dfrac{2}{3}.n_{Fe}=\dfrac{2}{3}x\left(mol\right)\)
Theo PT(2): \(n_{O_2}=\dfrac{1}{2}.n_{Mg}=\dfrac{1}{2}y\left(mol\right)\)
\(\Rightarrow\dfrac{2}{3}x+\dfrac{1}{2}y=0,2\) (**)
Từ (*) và (**), ta có HPT:
\(\left\{{}\begin{matrix}56x+24y=13,2\\\dfrac{2}{3}x+\dfrac{1}{2}y=0,2\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}x=0,15\\y=0,2\end{matrix}\right.\)
\(\Rightarrow m_{Fe}=0,15.56=8,4\left(g\right)\)
\(m_{Mg}=0,2.24=4,8\left(g\right)\)
Đúng 1
Bình luận (0)
* Ví dụ 1: Đốt cháy hoàn toàn 7,8 g hỗn hợp 2 kim loại Al và Mg cần dùng 4,48 lít O2 (đktc),sau phản ứng kết thúc thu được hỗn hợp chất rắn gồm Al2O3 và MgO.a. Tính khối lượng của mỗi kim loại trong hỗn hợp ban đầu.b. Tính khối lượng của Al2O3 và MgO thu được sau phản ứng.Ví dụ 2: Để đốt cháy hết 6,72 lít hỗn hợp khí CH4 và C2H6 cần dùng 24 gam O2 , sau phản ứng thu được CO2 và H2O.a. Tính khối lượng của mỗi khí trong hỗn hợp ban đầu.b. Tính thể tích khí CO2 thu được sau phản ứng. Biết...
Đọc tiếp
* Ví dụ 1: Đốt cháy hoàn toàn 7,8 g hỗn hợp 2 kim loại Al và Mg cần dùng 4,48 lít O2 (đktc),sau phản ứng kết thúc thu được hỗn hợp chất rắn gồm Al2O3 và MgO.
a. Tính khối lượng của mỗi kim loại trong hỗn hợp ban đầu.
b. Tính khối lượng của Al2O3 và MgO thu được sau phản ứng.
Ví dụ 2: Để đốt cháy hết 6,72 lít hỗn hợp khí CH4 và C2H6 cần dùng 24 gam O2 , sau phản ứng thu được CO2 và H2O.
a. Tính khối lượng của mỗi khí trong hỗn hợp ban đầu.
b. Tính thể tích khí CO2 thu được sau phản ứng. Biết các thể tích khí đều đo ở đktc.
giúp tui!
Đốt cháy hoàn toàn 7,56 gam bột nhôm cần dùng V lít (đktc) hỗn hợp khí gồm O2 và Cl2, thu được 24,18 gam hỗn hợp rắn X gồm AlCl3 và Al2O3 (không có khí thoát ra). Giá trị của V là A. 6,272 lít B. 5,376 lít C. 7,168 lít D. 6,720 lít
Đọc tiếp
Đốt cháy hoàn toàn 7,56 gam bột nhôm cần dùng V lít (đktc) hỗn hợp khí gồm O2 và Cl2, thu được 24,18 gam hỗn hợp rắn X gồm AlCl3 và Al2O3 (không có khí thoát ra). Giá trị của V là
A. 6,272 lít
B. 5,376 lít
C. 7,168 lít
D. 6,720 lít
đốt cháy hoàn toàn 10,8 gam Al cần V lít oxi (đktc) thu được Al2O3 theo phương trình Al + O2 -> Al2O3
a. Hãy cân bằng phương trình phản ứng trên
b. Tính V
a) PTHH: 4 Al + 3 O2 -to-> 2 Al2O3
b) nAl= 10,8/27=0,4(mol)
=>nO2= 3/4. nAl=3/4. 0,4= 0,3(mol)
=>V=V(O2,đktc)=0,3.22,4=6,72(l)
Đúng 2
Bình luận (0)
Số mol của nhôm
nAl = \(\dfrac{m_{Al}}{M_{Al}}=\dfrac{10,8}{27}=0,4\left(mol\right)\)
a) Pt : 4Al + 3O2 → 2Al2O3\(|\)
4 3 2
0,4 0,2
b) Số mol của khí oxi
nO2 = \(\dfrac{0,4.2}{4}=0,2\left(mol\right)\)
Thể tích của khí oxi
VO2 = nO2 . 22,4
= 0,2. 22,4
= 4,48 (l)
Chúc bạn học tốt
Đúng 1
Bình luận (3)
Hỗn hợp rắn A gồm Mg, Al và Cu. Đốt cháy m gam rắn A cần dùng 2,24 lít (đktc) hỗn hợp gồm
O
2
và
O
3
có tỉ khối so với He bằng 9,6 thu được hỗn hợp rắn B gồm các oxit. Hòa tan hoàn toàn B cần dùng 200 ml dung dịch HCl 0,6M và
H
2
SO
4
xM. Cô cạn dung dịch sau phản ứng thu được (3m+5,94) gam muối khan. Giá trị của m là A. 6,4 g...
Đọc tiếp
Hỗn hợp rắn A gồm Mg, Al và Cu. Đốt cháy m gam rắn A cần dùng 2,24 lít (đktc) hỗn hợp gồm O 2 và O 3 có tỉ khối so với He bằng 9,6 thu được hỗn hợp rắn B gồm các oxit. Hòa tan hoàn toàn B cần dùng 200 ml dung dịch HCl 0,6M và H 2 SO 4 xM. Cô cạn dung dịch sau phản ứng thu được (3m+5,94) gam muối khan. Giá trị của m là
A. 6,4 gam
B. 7,8 gam
C. 8,6 gam
D. 12,4 gam
Đốt cháy hoàn toàn 6,3 gam hơn hợp X gồm kim loại Mg và Al (tỉ lệ tương ứng 3 : 2) cần dùng vừa đủ với lít khí O2 (đktc), thu được hỗn hợp Y gồm hai onit bazo.
Pls help me! Đây là câu hỏi khó ;-;
Theo đề bài, ta có: \(\dfrac{m_{Mg}}{3}=\dfrac{m_{Al}}{2}\) và \(m_{Mg}+m_{Al}=6,3\)
Áp dụng tính chất dãy tỉ số bằng nhau, ta có:
\(\dfrac{m_{Mg}}{3}=\dfrac{m_{Al}}{2}=\dfrac{m_{Mg}+m_{Al}}{3+2}=\dfrac{6,3}{5}=1,26\\ \Rightarrow\left\{{}\begin{matrix}m_{Mg}=3.1,26=3,78\left(g\right)\\m_{Al}=2.1,26=2,52\left(g\right)\end{matrix}\right.\\ \Rightarrow\left\{{}\begin{matrix}n_{Mg}=\dfrac{3,78}{24}=0,1575\left(mol\right)\\n_{Al}=\dfrac{2,52}{27}=\dfrac{7}{75}\left(mol\right)\end{matrix}\right.\)
\(PTHH:2Mg+O_2\underrightarrow{t^o}2MgO\\ \left(mol\right)0,1575\rightarrow.......0,1575\\ PTHH:4Al+3O_2\underrightarrow{t^o}2Al_2O_3\\ \left(mol\right)....\dfrac{7}{75}\rightarrow.........\dfrac{7}{150}\)
Bạn dựa theo đề làm tiếp nhé, tại không thấy cái đề :v
Đúng 1
Bình luận (2)
Đốt cháy hoàn toàn 7,2 gam kim loại M (có hóa trị không đổi) cần 5,6 lít hỗn hợp khí gồm Cl2 và O2 (đktc). Phản ứng hoàn toàn thu được 23 gam hỗn hợp chất rắn. Kim loại M là A. Ca B. Cu C. Zn D. Mg
Đọc tiếp
Đốt cháy hoàn toàn 7,2 gam kim loại M (có hóa trị không đổi) cần 5,6 lít hỗn hợp khí gồm Cl2 và O2 (đktc). Phản ứng hoàn toàn thu được 23 gam hỗn hợp chất rắn. Kim loại M là
A. Ca
B. Cu
C. Zn
D. Mg
Đốt cháy hoàn toàn 7,2 gam kim loại M (có hóa trị không đổi) cần 5,6 lít hỗn hợp khí gồm Cl2 và O2 (đktc). Phản ứng hoàn toàn thu được 23 gam hỗn hợp chất rắn. Kim loại M là : A. Cu. B. Be. C. Mg. D. Ca.
Đọc tiếp
Đốt cháy hoàn toàn 7,2 gam kim loại M (có hóa trị không đổi) cần 5,6 lít hỗn hợp khí gồm Cl2 và O2 (đktc). Phản ứng hoàn toàn thu được 23 gam hỗn hợp chất rắn. Kim loại M là :
A. Cu.
B. Be.
C. Mg.
D. Ca.
Chọn đáp án C
Đặt nCl2 = x; nO2 = y ⇒ nkhí = x + y = 0,25 mol. Bảo toàn khối lượng:
7,2 + 71x + 32y = 23 ||⇒ giải hệ có: x = 0,2 mol; y = 0,05 mol.
Gọi n là hóa trị của M. Bảo toàn electron: n × nM = 2nCl2 + 4nO2.
⇒ nM = 0,6 ÷ n ⇒ MM = 7,2 ÷ (0,6 ÷ n) = 12n.
⇒ n = 2 và MM = 24 ⇒ M là Magie (Mg) ⇒ chọn C.
Đúng 0
Bình luận (0)
Đốt cháy hoàn toàn 7,2 gam kim loại M (có hóa trị không đổi) cần 5,6 lít hỗn hợp khí gồm Cl2 và O2 (đktc). Phản ứng hoàn toàn thu được 23 gam hỗn hợp chất rắn. Kim loại M là A. Ca. B. Cu. C. Zn D. Mg.
Đọc tiếp
Đốt cháy hoàn toàn 7,2 gam kim loại M (có hóa trị không đổi) cần 5,6 lít hỗn hợp khí gồm Cl2 và O2 (đktc). Phản ứng hoàn toàn thu được 23 gam hỗn hợp chất rắn. Kim loại M là
A. Ca.
B. Cu.
C. Zn
D. Mg.