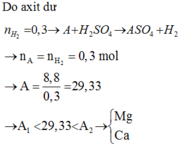Cho 6,8 gam hỗn hợp G gồm hai kim loại A và B liên tiếp trong nhóm IIA tác dụng với dung dịch H 2 S O 4 loãng dư, sau phản ứng thu được 5,6 lít khí (ở đktc). Xác định thành phần % khối lượng của từng kim loại trong G.

Những câu hỏi liên quan
A, B là 2 kim loại nằm ở hai chu kì liên tiếp thuộc nhóm IIA. Cho 4,4 gam một hỗn hợp gồm A và B tác dụng với HCl 1M (dư) thu được 3,36 lít khí (đktc).
a) Viết các phương trình phản ứng và xác định tên hai kim loại trên.
b) Tính thể tích dung dịch HCl đã dùng, biết rằng HCl dùng dư 25% so với lượng cần thiết
Gọi công thức chung của 2 kim loại là R
PTHH: \(R+2HCl\rightarrow RCl_2+H_2\uparrow\)
Ta có: \(n_{H_2}=\dfrac{3,36}{22,4}=0,15\left(mol\right)\) \(\Rightarrow\left\{{}\begin{matrix}n_{HCl\left(p/ứ\right)}=0,3\left(mol\right)\\n_R=0,15\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}V_{ddHCl}=\dfrac{0,3\cdot125\%}{1}=0,375\left(l\right)\\\overline{M}_R=\dfrac{4,4}{0,15}\approx29,33\end{matrix}\right.\)
Vì \(24< 29,33< 40\) nên 2 kim loại cần tìm là Magie và Canxi
Đúng 2
Bình luận (3)
Cho 6,4 gam hỗn hợp 2 kim loại liên tiếp thuộc nhóm IIA của bảng tuần hoàn, tác dụng với dung dịch H2SO4 loãng dư, thu được 4,48 lít H2 (đktc). hai kim loại đó là A. Be và Mg. B. Mg và CA. C. Ca và Sr. D. Sr và BA.
Đọc tiếp
Cho 6,4 gam hỗn hợp 2 kim loại liên tiếp thuộc nhóm IIA của bảng tuần hoàn, tác dụng với dung dịch H2SO4 loãng dư, thu được 4,48 lít H2 (đktc). hai kim loại đó là
A. Be và Mg.
B. Mg và CA.
C. Ca và Sr.
D. Sr và BA.
nR = nH2 = 0,2 ⇒ R = 6,4/0,2 = 32 ⇒ Chọn B.
Đúng 0
Bình luận (0)
Cho 6,4 gam hỗn hợp 2 kim loại liên tiếp thuộc nhóm IIA của bảng tuần hoàn, tác dụng với dung dịch H2SO4 loãng dư, thu được 4,48 lít H2 (đktc). hai kim loại đó là A. Be và Mg B. Mg và Ca C. Ca và Sr D. Sr và Ba
Đọc tiếp
Cho 6,4 gam hỗn hợp 2 kim loại liên tiếp thuộc nhóm IIA của bảng tuần hoàn, tác dụng với dung dịch H2SO4 loãng dư, thu được 4,48 lít H2 (đktc). hai kim loại đó là
A. Be và Mg
B. Mg và Ca
C. Ca và Sr
D. Sr và Ba
Đáp án B
nR = nH2 = 0,2 => R = 6,4/0,2 = 32
Đúng 0
Bình luận (0)
A, B là 2 kim loại nằm ở 2 chu kỳ liên tiếp thuộc nhóm IIA. Cho 4,4 gam một hỗn hợp gồm A và B tác dụng với dung dịch HCl 1M (dư) thu được 3,36 lít khí (đktc). Hai kim loại đó là A. Mg và Ca B. Ca và Ba C. Mg và Ba D. Be và Sr
Đọc tiếp
A, B là 2 kim loại nằm ở 2 chu kỳ liên tiếp thuộc nhóm IIA. Cho 4,4 gam một hỗn hợp gồm A và B tác dụng với dung dịch HCl 1M (dư) thu được 3,36 lít khí (đktc). Hai kim loại đó là
A. Mg và Ca
B. Ca và Ba
C. Mg và Ba
D. Be và Sr
Đáp án A
Hướng dẫn Gọi công thức chung của hai kim loại là M = a mol
M + 2HCl ® MCl2 + H2
(mol): a 2a a
Số mol H2 = 0,15 mol nên a = 0,15 mol
Ta có: Ma = 4,4 ® M = 29,33
A và B là 2 kim loại nằm ở 2 chu kỳ liên tiếp thuộc nhóm IIA nên A là Mg và B là Ca
Đúng 0
Bình luận (0)
Hỗn hợp X gồm 2 kim loại thuộc hai chu kì liên tiếp nhau và thuộc nhóm IA. Cho 5,4 gam X tác dụng với dung dịch H2SO4 loãng (dư) thì thu được 2,24 lít khí hiđro (đktc) và dung dịch B. a. Xác định hai kim loại và % khối lượng mỗi kim loại trong hỗn hợp? b. Tính khối lượng muối thu được khi cô cạn dung dịch B?
\(n_{H_2}=\dfrac{2,24}{22,4}=0,1mol\)
\(2X+H_2SO_4\rightarrow X_2SO_4+H_2\)
0,2 \(\leftarrow\) 0,1
\(\Rightarrow\overline{M_X}=\dfrac{5,4}{0,2}=27\) \(\Rightarrow X_1< 27< X_2\)
Mà X1, X2 thuộc nhóm IA
\(\Rightarrow\left\{{}\begin{matrix}X_1:Na\\X_2:K\end{matrix}\right.\) Gọi \(n_{Na}=x\left(mol\right)\) , \(n_K=y\left(mol\right)\)
\(\Rightarrow\left\{{}\begin{matrix}BTKL:23x+39y=5,4\\BTe:x+y=2n_{H_2}=0,2\end{matrix}\right.\) \(\Rightarrow\left\{{}\begin{matrix}x=0,15mol\\y=0,05mol\end{matrix}\right.\)
\(\%m_{Na}=\dfrac{0,15\cdot23}{5,4}\cdot100\%=63,89\%\)
\(\%m_K=100\%-63,89\%=36,11\%\)
Khi cô cạn dung dịch thu được muối: \(\left\{{}\begin{matrix}n_{Na^+}=0,15mol\\n_{K^+}=0,05mol\\n_{SO_4^{2-}}=n_{H_2SO_4}=n_{H_2}=0,1mol\end{matrix}\right.\)
\(\Rightarrow m_{m'}=0,15\cdot23+0,05\cdot39+0,1\cdot\left(32+4\cdot16\right)=15g\)
Đúng 0
Bình luận (0)
Hỗn hợp A gồm 2 kim loại X, Y thuộc hai chu kì liên tiếp ở phân nhóm IIA. Cho 2,64 gam A tác dụng hết với dung dịch H2SO4 loãng thu dược 2,016 khí (đktc). Xác định X, Y A. Mg, Ca B. Be, Mg C. Ca, Ba D. Ca, Sr
Đọc tiếp
Hỗn hợp A gồm 2 kim loại X, Y thuộc hai chu kì liên tiếp ở phân nhóm IIA. Cho 2,64 gam A tác dụng hết với dung dịch H2SO4 loãng thu dược 2,016 khí (đktc). Xác định X, Y
A. Mg, Ca
B. Be, Mg
C. Ca, Ba
D. Ca, Sr
Đáp án A
Hướng dẫn Thay thế hỗn hợp kim loại bằng một kim loại tương đương ![]()
Số mol H2 = 0,09 (mol)
![]() + H2SO4 →
+ H2SO4 → ![]() SO4 + H2
SO4 + H2
(mol) 0,09 ![]() 0,09
0,09
![]()
=> Mg =24< 29,33 < 40=Ca
X, Y là Mg, Ca
Đúng 1
Bình luận (0)
Cho 12,8 gam hỗn hợp 2 kim loại thuộc 2 chu kì liên tiếp nhóm IIA tác dụng hết với dung dịch HCl ( dùng dư 15% so với lượng phản ứng) thu được 8,96 lít khí ( đktc) và dung dịch .
a. Xác định tên 2 kim loại, tính phần trăm khối lượng của mỗi kim loại trong hỗn hợp.
b.Tính thể tích dung dịch NaOH 0,5M cần dùng để trung hòa lượng axit dư trong ½ dung dịch X
Đây là VD cho dạng bài tương tự nhé! Bạn xem thử!
https://hoc24.vn/hoi-dap/tim-kiem?id=237172646178&q=Cho+4,4g+h%E1%BB%97n+h%E1%BB%A3p+2+kim+lo%E1%BA%A1i+nh%C3%B3m+IIA+thu%E1%BB%99c+hai+chu+k%C3%AC+li%C3%AAn+ti%E1%BA%BFp+t%C3%A1c+d%E1%BB%A5ng+v%E1%BB%9Bi+dung+d%E1%BB%8Bch+HCl+d%C6%B0+thu+%C4%91%C6%B0%E1%BB%A3c+3,36+l%C3%ADt+H2+(%C4%91ktc).+a)+X%C3%A1c+%C4%91%E1%BB%8Bnh+t%C3%AAn+kim+lo%E1%BA%A1i.+b)+T%C3%ADnh+C%+c%E1%BB%A7a+dung+d%E1%BB%8Bch+thu+%C4%91%C6%B0%E1%BB%A3c.
Đúng 1
Bình luận (0)
Cho 26,8 gam hỗn hợp hai muối cacbonat của hai kim loại nhóm IIA, thuộc 2 chu kỳ liên tiếp nhau trong bảng hệ thống tuần hoàn các nguyên tố hóa học, tác dụng vừa đủ với 219g dung dịch HCl 10%. Sau khi phản ứng kết thúc, cô cạn dung dịch thu được m(g) muối clorua khan. Giá trị của m là (Cho nguyên tử khối theo u của Mg24, Ca40; Ba137; Be9)
Đọc tiếp
Cho 26,8 gam hỗn hợp hai muối cacbonat của hai kim loại nhóm IIA, thuộc 2 chu kỳ liên tiếp nhau trong bảng hệ thống tuần hoàn các nguyên tố hóa học, tác dụng vừa đủ với 219g dung dịch HCl 10%. Sau khi phản ứng kết thúc, cô cạn dung dịch thu được m(g) muối clorua khan. Giá trị của m là (Cho nguyên tử khối theo u của Mg=24, Ca=40; Ba=137; Be=9)
\(n_{HCl}=\dfrac{219.10}{100.36,5}=0,6\left(mol\right)\)
ACO3 + 2HCl --> ACl2 + CO2 + H2O
BCO3 + 2HCl --> BCl2 + CO2 + H2O
=> nHCl = 2.nCO2 = 2.nH2O
=> nCO2 = nH2O = 0,3 (mol)
Theo ĐLBTKL: mhh ban đầu + mHCl = mhh muối clorua + mCO2 + mH2O
=> mhh muối clorua = 26,8 + 0,6.36,5 - 0,3.44 - 0,3.18 = 30,1 (g)
Đúng 1
Bình luận (0)
Cho 8,8 gam hỗn hợp 2 kim loại kế tiếp thuộc nhóm IIA của bảng tuần hoàn tác dụng với dung dịch H2SO4 loãng dư thu được 6,72 lít H2 (đktc). Hai kim loại đó là A. Mg và Ca B. Sr và Ba C. Be và Mg D. Ca và Sr
Đọc tiếp
Cho 8,8 gam hỗn hợp 2 kim loại kế tiếp thuộc nhóm IIA của bảng tuần hoàn tác dụng với dung dịch H2SO4 loãng dư thu được 6,72 lít H2 (đktc). Hai kim loại đó là
A. Mg và Ca
B. Sr và Ba
C. Be và Mg
D. Ca và Sr