Cho 6,00 g P2O5 vào 25,0 ml dung dịch H3PO4 6,00% (D = 1,03 g/ml). Tính nồng độ phần trăm H3PO4 trong dung dịch tạo thành?

Những câu hỏi liên quan
Tính nồng độ phần trăm của dung dịch sau khi pha 600ml dung dịch H3po4 2M(D=1,2g/mL) vào 200ml dung dịch h3po4 ( D=1,1 g/mL)
\(n_{H_3PO_4}=0,6.2=1,2\left(mol\right)\Rightarrow m_{H_3PO_4}=1,2.98=117,6\left(g\right)\)
mdd sau khi pha = 600.1,2+200.1,1 = 940 (g)
\(C\%_{ddH_3PO_4}=\dfrac{117,6.100\%}{940}=12,51\%\)
Đúng 3
Bình luận (1)
Cái 200ml dd H3PO4 có D=1,1g/ml thì cái đó có cho CM không? hay số mol gì đó
Đúng 2
Bình luận (1)
Cho 100 ml dung dịch H2SO4 2M ( D = 1,2 g/m) tác dụng với 100 ml dung dịch BaCl2 1m ( D = 1,32 g/ml )
a) Tính khối lượng chất kết tủa tạo thành
b) Tính nồng độ phần trăm và nồng độ mol của dung dịch tạo thành
\(n_{H_2SO_4}=0.1\cdot2=0.2\left(mol\right)\)
\(m_{dd_{H_2SO_4}}=100\cdot1.2=120\left(g\right)\)
\(n_{BaCl_2}=0.1\cdot1=0.1\left(mol\right)\)
\(m_{dd_{BaCl_2}}=100\cdot1.32=132\left(g\right)\)
\(BaCl_2+H_2SO_4\rightarrow BaSO_4+2HCl\)
\(0.1................0.1.........0.1...............0.2\)
\(\Rightarrow H_2SO_4dư\)
\(m_{BaSO_4}=0.1\cdot233=23.3\left(g\right)\)
\(V_{dd}=0.1+0.1=0.2\left(l\right)\)
\(C_{M_{H_2SO_4\left(dư\right)}}=\dfrac{0.2-0.1}{0.2}=0.5\left(M\right)\)
\(C_{M_{HCl}}=\dfrac{0.2}{0.2}=1\left(M\right)\)
\(m_{\text{dung dịch sau phản ứng}}=120+132-23.3=228.7\left(g\right)\)
\(C\%_{H_2SO_4\left(dư\right)}=\dfrac{0.1\cdot98}{228.7}\cdot100\%=4.28\%\)
\(C\%_{HCl}=\dfrac{0.2\cdot36.5}{228.7}\cdot100\%=3.2\%\)
Đúng 3
Bình luận (1)
Đốt cháy a gam photpho đỏ trong không khí lấy dư, rồi cho sản phẩm thu được vào 500,0 ml dung dịch
H
3
P
O
4
85,00% (D 1,7 g/ml). Sau khi phản ứng xảy ra hoàn toàn nồng độ của dung dịch
H
3
P
O
4
xác định được là 92,60%. Tính giá trị của a.
Đọc tiếp
Đốt cháy a gam photpho đỏ trong không khí lấy dư, rồi cho sản phẩm thu được vào 500,0 ml dung dịch H 3 P O 4 85,00% (D = 1,7 g/ml). Sau khi phản ứng xảy ra hoàn toàn nồng độ của dung dịch H 3 P O 4 xác định được là 92,60%. Tính giá trị của a.
Photpho cháy trong không khí lấy dư theo phản ứng :
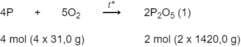
P 2 O 5 tác dụng với tạo thành H 3 P O 4 theo phản ứng :
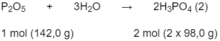
Theo phản ứng (1): 4 x 31,0 g P tạo ra 2 x 142,0 g P 2 O 5
a g P tạo ra 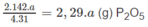
Theo các phản ứng (1) và (2) :
4 x 31,0 (g) P tạo ra 4 x 98,0 (g) H 3 P O 4
a (g) P tạo ra 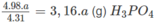
Khối lượng H 3 P O 4 có trong 500,0 ml dung dịch 85,00% :
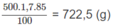
Khối lượng H 3 P O 4 sau khi đã hoà tan P 2 O 5 : 722,5 g + 3,16 x a g.
Khối lượng của dung dịch H 3 P O 4 sau khi đã hoà tan P 2 O 5 :
500,0 x 1,7 g + 2,29 x a g = 850,0 g + 2,29 x a g
Ta có phương trình về nồng độ phần trăm của dung dịch H 3 P O 4 :
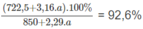
Giải phương trình được a = 62,16 g photpho.
Đúng 0
Bình luận (0)
Câu 1:Cho 150 ml dung dịch H3PO4 1M tác dụng với 225 ml dung dịch NaOH 1Ma, Tính khối lượng tạo thànhb, Tính nồng độ mol của các chất tan trong dung dịch thu đượcCâu 2:Cho 150 ml dung dịch H3PO4 1M tác dụng với 350 ml dung dịch KOH 1Ma, Tính khối lượng tạo thànhb, Tính nồng độ mol của các chất tan trong dung dịch thu được
Đọc tiếp
Câu 1:
Cho 150 ml dung dịch H3PO4 1M tác dụng với 225 ml dung dịch NaOH 1M
a, Tính khối lượng tạo thành
b, Tính nồng độ mol của các chất tan trong dung dịch thu được
Câu 2:
Cho 150 ml dung dịch H3PO4 1M tác dụng với 350 ml dung dịch KOH 1M
a, Tính khối lượng tạo thành
b, Tính nồng độ mol của các chất tan trong dung dịch thu được
Câu 1:Cho 150 ml dung dịch H3PO4 1M tác dụng với 225 ml dung dịch NaOH 1Ma, Tính khối lượng tạo thànhb, Tính nồng độ mol của các chất tan trong dung dịch thu đượcCâu 2:Cho 150 ml dung dịch H3PO4 1M tác dụng với 350 ml dung dịch KOH 1Ma, Tính khối lượng tạo thànhb, Tính nồng độ mol của các chất tan trong dung dịch thu được
Đọc tiếp
Câu 1:
Ta có: \(n_{H_3PO_4}=0,15.1=0,15\left(mol\right)\)
\(n_{NaOH}=0,225.1=0,225\left(mol\right)\)
\(\Rightarrow\dfrac{n_{NaOH}}{n_{H_3PO_4}}=\dfrac{0,225}{0,15}=1,5\)
⇒ Pư tạo muối NaH2PO4 và Na2HPO4.
a, Giả sử: \(\left\{{}\begin{matrix}n_{NaH_2PO_4}=x\left(mol\right)\\n_{Na_2HPO_4}=y\left(mol\right)\end{matrix}\right.\)
BTNT Na, có: x + 2y = 0,225 (1)
BTNT P, có: x + y = 0,15 (2)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}x=0,075\left(mol\right)\\y=0,075\left(mol\right)\end{matrix}\right.\)
⇒ mNaH2PO4 = 0,075.120 = 9 (g)
mNa2HPO4 = 0,075.142 = 10,65 (g)
b, \(C_{M_{NaH_2PO_4}}=C_{M_{Na_2HPO_4}}=\dfrac{0,075}{0,375}=0,2M\)
Câu 2:
Ta có: \(n_{H_3PO_4}=0,15\left(mol\right)\)
\(n_{KOH}=0,35\left(mol\right)\)
\(\Rightarrow\dfrac{n_{KOH}}{n_{H_3PO_4}}=2,333\)
Vậy: Pư tạo muối Na2HPO4 và Na3PO4.
a, Giả sử: \(\left\{{}\begin{matrix}n_{Na_2HPO_4}=x\left(mol\right)\\n_{Na_3PO_4}=y\left(mol\right)\end{matrix}\right.\)
BTNT Na, có: 2x + 3y = 0,35 (1)
BTNT P, có: x + y = 0,15 (2)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}x=0,1\left(mol\right)\\y=0,05\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow m_{Na_2HPO_4}=0,1.142=14,2\left(g\right)\)
\(m_{Na_3PO_4}=0,05.164=8,2\left(g\right)\)
b, Ta có: \(\left\{{}\begin{matrix}C_{M_{Na_2HPO_4}}=\dfrac{0,1}{0,5}=0,2M\\C_{M_{Na_3PO_4}}=\dfrac{0,05}{0,5}=0,1M\end{matrix}\right.\)
Bạn tham khảo nhé!
Đúng 2
Bình luận (0)
Cho 100 ml dung dịch H 3 PO 4 vào 200 ml dung dịch NaOH 1,2M thì thu được dung dịch có chứa 19,98 gam chất tan. Nồng độ mol của dung dịch H 3 PO 4 là
A. 1,5M.
B. 0,1M.
C. 1,2M.
D. 1,6M.
cho 500ml dung dịch Ca(OH)2 2M phản ứng với 500d dung dịch H3PO4 10%
a. Tính khối lượng các chất trong dung dịch sau phản ứng
b. Tính nồng độ phần trăm của các chất sau phản ứng
c. Tính nồng độ mol của các chất sau phản ứng
cho biết D Ca(OH)2 = 1,5g/ml, D H3PO4 = 1,25 g/ml
Các thầy cô giải giúp em với ạ
Cho 142 g P2O5 vào 500 gam dung dịch H3PO4 23,72% được dung dịch A. Tìm nồng độ % của dung dịch A A. 63% B. 32% C. 49% D. 56%
Đọc tiếp
Cho 142 g P2O5 vào 500 gam dung dịch H3PO4 23,72% được dung dịch A. Tìm nồng độ % của dung dịch A
A. 63%
B. 32%
C. 49%
D. 56%
Đáp án C
nP2O5=1 mol
nH3PO4=23,72%.500/98=1,21 mol
P2O5 + 3H2O → 2H3PO4
1 3 2
nH3PO4=2+1,21=3,21 mol => C% H3PO4 (dd A) = 3,21.98/(142+500)=49%
Đúng 0
Bình luận (0)
Hòa tan 14,2 gam P2O5 trong 250 g dung dịch H3PO4 9,8%. Nồng độ % của dung dịch axit H3PO4 thu được là:
A. 5,4
B. 14,7
C. 16,7
D. 17,6
Đáp án C
Ta có: nP2O5= 0,1 mol; mH3PO4 ban đầu= 250.9,8/100=24,5 gam
P2O5+ 3H2O→ 2H3PO4
0,1 0,2 mol
Tổng khối lượng H3PO4 là: 0,2.98+ 24,5=44,1 gam
Khối lượng dung dịch là: 14,2+ 250=264,2 gam
![]()
Đúng 0
Bình luận (0)

















