Một bạn học sinh đã đổ nhầm dung dịch sắt (II) sunfat vào lọ chứa sẵn dung dịch kẽm sunfat. Để thu được dung dịch chứa duy nhất muối kẽm sunfat, theo em dùng kim loại nào?
A. Đồng
B. Sắt
C. Kẽm
D. Nhôm
Nhúng bản kẽm và bản sắt vào cùng một dung dịch đồng sunfat. Sau một thời gian, nhấc hai bản kim loại ra thì trong dung dịch thu được nồng độ mol của kẽm sunfat bằng 2,5 lần của sắt sunfat. Mặt khác khối lượng của dung dịch giảm 0,11 gam. Khối lượng đồng bám trên mỗi kim loại là:
A. 1,28 gam và 3,2 gam
B. 6,4 gam và 1,6 gam
C. 1,54 gam và 2,6 gam
D. 8,6 gam và 2,4 gam
hòa tan hoàn toàn 3,22 gam hỗn hợp gồm sắt , magie, kẽm bằng một lượng vừa đủ dung dịch axit sunfuric loãn, thu được 0,06 mol khí hidro và dung dịch chứa a gam hỗn hợp gồm sắt (II) sunfat, magie sunfat, kẽm sunfat.
a,viết các phương trình hóa học
b.tính giá trị của a
Pt: Fe + H2SO4 --> FeSO4 + H2
.....Mg + H2SO4 --> MgSO4 + H2
.....Zn + H2SO4 --> ZnSO4 + H2
Theo pt: nH2SO4 = nH2 = 0,06 mol
=> nSO4 = nH2SO4 = 0,06 mol
a = mkim loại + mSO4 = 3,22 + 0,06 . 96 = 8,98 (g)
Pt: Fe + 2HCl --> FeCl2 + H2
......Mg + 2HCl --> MgCl2 + H2
......Zn + 2HCl --> ZnCl2 + H2
Theo pt: nHCl = 2nH2 = 2 . 0,06 = 0,12 mol
=> nCl - = 0,12 mol
a = mkim loại + mgốc axit = 3,22 + 0,12 . 36,5 = 7,6 (g)
Bài 1: Cho các dung dịch : đồng (II) sunfat, sắt (II) sunfat, Magie sunfat, bạc nitrat và các kim loại: Cu,Fe,Mg,Ag .Theo em những cặp chất nào (kim loại và muối ) phản ứng được với nhau?viết PTHH
Bài 2: Bạc có lẫn sắt và kẽm.Làm thế nào để thu được bạc tinh khiết?
Bài 3: Dung dịch kẽm suntat có lẫn tạp chất là đồng (II)sunfat. Dùng kim loại nào để làm sạch muối kẽm sunfat?giải thích và viết PTHH
Bài 2. Để thu được bạc tinh khiết ta cho hỗn hợp trên vào dung dịch AgNO3 , chất rắn sau phản ứng là bạc tinh khiết
\(Zn+2AgNO_3\rightarrow Zn\left(NO_3\right)_2+2Ag\\ Fe+2AgNO_3\rightarrow Fe\left(NO_3\right)_2+2Ag\)
Bài 3. Dùng kim loại kẽm để làm sạch muối kẽm sunfat do kẽm tác dụng được với CuSO4, tạo thành dung dịch ZnSO4 và kim loại đồng
\(Zn+CuSO_4\rightarrow ZnSO_4+Cu\)
Ngâm một lá kẽm trong dung dịch muối sunfat có chứa 4,48 gam ion kim loại X điện tích 2+. Sau phản ứng, khối lượng lá kẽm tăng thêm 1,88 gam. Công thức hóa học của muối sunfat đó là:
A. CdSO4
B. CuSO4
C. NiSO4
D. FeSO4
Đáp án A
Khối lượng kẽm tăng lên chính bằng chênh lệch giữa khối lượng kẽm tan ra và kim loại X bám vào
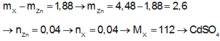
Câu 18. Cho kim loại kẽm vào axit sunfuric thu được dung dịch có chứa 24,15gam kẽm sunfat vào khí hiđrô(đkttc) a/ Nêu hiện tượng phản ứng trên?
A. Sủi bọt khí B. dung dịch đổi màu
C. Kết tủa trắng. D. Không hiện tượng.
b/ Tính khối lượng axit H2SO4 cần dùng.
A. 14. B. 14,5 C. 14,7 D.14,8
b/ Tính thể tích khí hiđro tạo thành ở đktc.
A. 0,56 B. 1,12 C. 2,8 D.3.36
c/ Tính thể tích khí oxi (đktc) cần dùng để đốt cháy hết lượng khí hidro trên.
A. 3,36 B. 1,68 C. 11,2 D. 16,8
Câu 19. Thể tích (đktc) của 9.1023 phân tử khí H2
A.33,6 B. 2,8 C. 5,6 D.11,2
Câu 20. Hãy cho biết 6,72 lít khí oxi (đktc)
a/ Có bao nhiêu mol oxi?
A.0,12 B . 0,035 C.0,03 D. 0,3
b/ Có bao nhiêu phân tử khí oxi?
A. 1,7.1023 B. 1,5.1023 C 1,8.1023 D. 3.1023
c/ Có khối lượng bao nhiêu gam?
A . 12 B 9,6 C.9 D.11
d/ Cần phải lấy bao nhiêu gam khí N2 để có số phân tử gấp 4 lần số phân tử có trong 3.2 g khí oxi.
A . 11,2 B. 14 C 33 D. 23
Câu 21. Tính khối lượng của: 0,75 mol khí NO(đktc); 1,8.1023 phân tử NaCl; 8,96 lít khí CO2(đktc).
A. 53 B. 54 C. 55,65 D. 57,65
MÌNH CẦN LỜI GIẢI THÍCH CHI TIẾT Ạ
Câu 21. Tính khối lượng của: 0,75 mol khí NO(đktc); 1,8.1023 phân tử NaCl; 8,96 lít khí CO2(đktc).
A. 53 B. 54 C. 55,65 D. 57,6
\(m_{NO}=0,75.30=22,5g\)
\(m_{NaCl}=\left(\dfrac{1,8.10^{23}}{6.10^{23}}\right).58,5=17,55g\)
\(m_{CO_2}=\left(\dfrac{8,96}{22,4}\right).44=17,6g\)
\(\Rightarrow m_{hh}=22,5+17,55+17,6=57,6\) g
\(\Rightarrow D\)
< Bạn ơi, câu này mhh mình ra 57,6 g nên mình đổi đáp án câu D lại nhé! >
Câu 18. Cho kim loại kẽm vào axit sunfuric thu được dung dịch có chứa 24,15gam kẽm sunfat vào khí hiđrô(đkttc) a/ Nêu hiện tượng phản ứng trên?
A. Sủi bọt khí B. dung dịch đổi màu
C. Kết tủa trắng. D. Không hiện tượng.
b/ Tính khối lượng axit H2SO4 cần dùng.
A. 14. B. 14,5 C. 14,7 D.14,8
\(PTHH:Zn+H_2SO_4\rightarrow ZnSO_4+H_2\)
\(n_{ZnSO_4}=\dfrac{24,15}{161}=0,15mol\)
\(m_{H_2SO_4}=0,15.98=14,7g\)
\(\Rightarrow\) Đáp án C
b/ Tính thể tích khí hiđro tạo thành ở đktc.
A. 0,56 B. 1,12 C. 2,8 D.3.36
\(V_{H_2}=0,15.22,4=3,36l\)
\(\Rightarrow\) Đáp án D
c/ Tính thể tích khí oxi (đktc) cần dùng để đốt cháy hết lượng khí hidro trên.
A. 3,36 B. 1,68 C. 11,2 D. 16,8
\(PTHH:2O_2+H_2\rightarrow2H_2O\)
\(n_{H_2}=0,15mol\)
\(n_{O_2}=\dfrac{0,15}{2}=0,075mol\)
\(\Rightarrow V_{O_2}=0,075.22,4=1,68l\)
\(\Rightarrow\) Đáp án B
Câu 19. Thể tích (đktc) của 9.1023 phân tử khí H2
A.33,6 B. 2,8 C. 5,6 D.11,2
\(n_{H_2}=\dfrac{9.10^{23}}{6.10^{23}}=1,5mol\)
\(V_{H_2}=1,5.22,4=33,6l\)
\(\Rightarrow A\)
Câu 20. Hãy cho biết 6,72 lít khí oxi (đktc)
a/ Có bao nhiêu mol oxi?
A.0,12 B . 0,035 C.0,03 D. 0,3
\(n_{O_2}=\dfrac{6,72}{22,4}=0,3mol\\ \Rightarrowđáp.án.D\)
b/ Có bao nhiêu phân tử khí oxi?
A. 1,7.1023 B. 1,5.1023 C 1,8.1023 D. 3.1023
\(Số.phân.tử.khí.O_2=0,3.6.10^{23}=1,8.10^{23}\) phân tử
\(\RightarrowĐáp.án.C\)
c/ Có khối lượng bao nhiêu gam?
A . 12 B 9,6 C.9 D.11
\(m_{O_2}=0,3.32=9,6g\)
\(\RightarrowĐáp.án.B\)
d/ Cần phải lấy bao nhiêu gam khí N2 để có số phân tử gấp 4 lần số phân tử có trong 3.2 g khí oxi.
A . 11,2 B. 14 C 33 D. 23
\(PTHH:N_2+O_2\rightarrow2NO\)
\(n_{O_2}=\dfrac{3,2}{32}=0,1mol\)
\(n_{N_2}=0,1.4=0,4mol\)
\(m_{N_2}=0,4.28=11,2g\)
\(\RightarrowĐáp.án.A\)
Câu 1: hòa tan hoàn toàn một đọa kẽm trong ống nghiệm đựng dung dịch axit sunfuric , sau phản ứng thu đc kẽm sunfat và 2,24 lít khí A ( ở đktc )
a, Viết PTHH
b, Tính m của kẽm đã phản ứng
Câu 2: cho 11,2g sắt tác dụng vs dung dịch chứa 10,95g axit clohidric tạo ra sắt (II) clorua và khí hidro
a, Viết PTHH
b, Chất nào dư, m là bao nhiêu ?
c, Tính thể tích của khí hidro ở đktc
Câu 3: để hòa tan hoàn toàn 7g một kim loại hóa trị II cần dùng dung dịch axit chứa 9,125g , xác định tên của kim loại R trên
Câu 1 :
\(n_{H_2}=\dfrac{2.24}{22.4}=0.1\left(mol\right)\)
\(Zn+H_2SO_4\rightarrow ZnSO_4+H_2\)
\(0.1.....................................0.1\)
\(m_{Zn}=0.1\cdot65=6.5\left(g\right)\)
Câu 2 :
\(n_{Fe}=\dfrac{11.2}{56}=0.2\left(mol\right)\)
\(n_{HCl}=\dfrac{10.95}{36.5}=0.3\left(mol\right)\)
\(Fe+2HCl\rightarrow FeCl_2+H_2\)
\(1..............2\)
\(0.2...........0.3\)
\(LTL:\dfrac{0.2}{1}>\dfrac{0.3}{2}\Rightarrow Fedư\)
\(m_{Fe\left(dư\right)}=\left(0.2-0.15\right)\cdot56=2.8\left(g\right)\)
\(V_{H_2}=0.15\cdot22.4=3.36\left(l\right)\)
Câu 3 :
Axit HCl em nhé !
\(n_{HCl}=\dfrac{9.125}{36.5}=0.25\left(mol\right)\)
\(R+2HCl\rightarrow RCl_2+H_2\)
\(0.125..0.25\)
\(M_R=\dfrac{7}{0.125}=56\left(\dfrac{g}{mol}\right)\)
\(R:Fe\left(Sắt\right)\)
2. Nghiên cứu tổng khối lượng các chất trước và sau phản ứng hóa học.
Làm thế nào có thể biết được tổng khối lượng của các chất trước phản ứng hóa học và tổng khối lượng của các chất sau phản ứng hóa học có thay đổi hay không?
Hãy thực hiện thí nghiệm (ghi hiện tượng và kết quả thu được vào bảng 1.3):
- Lấy 2 - 3 mảnh/viên kẽm nhỏ, dùng giấy ráp đánh nhẹ cho hết lớp oxit mỏng ở phía ngoài (1), sau đó dùng cân kĩ thuật/cân điện tử/bộ cảm biến để cân tổng khối lượng của các mảnh/viên.
- Lấy 50 ml dung dịch muối đồng sunfat CuSO4 nồng độ khoảng 0,5M cho vào các cốc thủy tinh sạch (loại 100 ml) (2), dùng cân kĩ thuật/cân điện tử/ bộ cảm biến để cân khối lượng cốc đựng dung dịch muối đồng sunfat.
- Cho các mảnh/viên kẽm (1) vào cốc đựng dung dịch muối đồng sunfat (2), quan sát hiện tượng xảy ra trong khoảng 3 phút, nhận xét về sự thay đổi màu sắc của dung dịch muối đồng sunfat và các mảnh/viên kẽm.
- Dùng cân kĩ thuật/cân điện tử/bộ cảm biến để cân lại tổng khối lượng của cốc đựng dung dịch muối đồng sunfat và các mảnh/viên kẽm sau thí nghiệm.
Trả lời các câu hour sau:
a) Nhận xét về tổng khối lượng của các cốc đựng dung dịch muối đồng sunfat và các mảnh/viên kẽm sau thí nghiệm so với tổng khối lượng của các mảnh/viên kẽm và khối lượng cốc đựng dung dịch muối đồng sunfat trước thí nghiệm.
b) So sánh các số liệu thu được của nhóm em với số liệu của các nhóm khác (giống nhau, khác nhau). Giải thích.
Trong giờ thực hành hóa học, một học sinh nhúng một đinh sắt vào dung dịch muối đồng sunfat C u S O 4 . Sau một thời gian, lấy đinh sắt ra khỏi dung dịch muối. Thanh sắt bị phủ một lớp màu đỏ gạch và dung dịch có muối sắt (II) sunfat F e S O 4 . Hãy cho biết phản ứng trên thuộc loại phản ứng nào?
Cho các cặp oxi hóa - khử được sắp xếp theo thứ tự tăng dần tính oxi hóa của các ion kim loại: A l 3 + / A l ; F e 2 + / F e ; S n 2 + / S n ; C u 2 + / C u . Tiến hành các thí nghiệm sau: (a) Cho sắt vào dung dịch đồng(II) sunfat. (b) Cho đồng vào dung dịch nhôm sunfat. (c) Cho thiếc vào dung dịch đồng(II) sunfat. (d) Cho thiếc vào dung dịch sắt(II) sunfat. Trong các thí nghiệm trên, những thí nghiệm có xảy ra phản ứng là
A. (b) và (c)
B. (b) và (d)
C. (a) và (c)
D. (a) và (b)