Cho 10ml dung dịch X gồm HCl 1M và H2SO4 0,5M. Thể tích dung dịch NaOH 1M cần để trung hoà dung dịch X đã cho là:
A. 10ml
B. 15ml
C. 20ml
D. 25ml
Nhỏ 30ml dung dịch NaOH 2M vào 20ml dung dịch hỗn hợp gồm HCl C1 (mol/l) và HNO3 C2 (mol/l). Để trung hòa NaOH dư cần 30ml dung dịch HBr 1M. Mặt khác, trộn 10ml dung dịch HCl C1 với 20ml dung dịch HNO3 C2 thì thể tích dung dịch NaOH 1M cần để trung hòa là 20ml. Giá trị C1 và C2 là:
A. 1,0 và 0,5
B. 0,5 và 1,0
C. 0,5 và 1,5
D. 1,0 và 1,0
Đáp án A
Thí nghiệm 1 có nOH-= nH+
Nên 30.2= 20.C1+ 20.C2+ 30.1
Thí nghiệm 2 có nOH-= nH+
Nên 10.C1+ 20.C2 = 1.20
Suy ra C1 = 1,0 và C2 = 0,5
1) để trung hòa 10mL dung dịch HCL nồng độ x M cần 50mL dung dịch NaOH 0,5M. Xác định giá trị của x 2) để chuẩn độ 10mL dung dịch HCL cần 20mL dung dịch NaOH 0,1M. Xác định nồng độ của dung dịch HCL trên
1) Để trung hòa HCl, số mol HCl phải bằng số mol NaOH. Vì vậy, ta có:
n(HCl) = n(NaOH)
x * 10 = 0,5 * 50
x = (0,5 * 50) / 10
x = 2,5 triệu
Vậy, nồng độ của dung dịch HCl là 2.5 M.
2) Ta có:
n(HCl) = n(NaOH)
n(HCl) = 0,1 * 20/10
Vậy, nồng độ của dung dịch HCl là 0.2 M.
\(1)n_{NaOH}=0,05.0,5=0,025mol\\ NaOH+HCl\rightarrow NaCl+H_2O\\ \Rightarrow n_{NaOH}=n_{HCl}=0,025mol\)
\(C_M\) \(_{HCl}=\dfrac{0,025}{0,01}=2,5M\)
\(2)n_{NaOH}=0,1.0,02=0,002mol\\ HCl+NaOH\rightarrow NaCl+H_2O\\ n_{NaOH}=n_{HCl}=0,002mol\)
\(C_M\) \(_{HCl}=\dfrac{0,002}{0,01}=0,2M\)
Cho 10 ml dung dịch X chứa HCl 1M và H 2 SO 4 0,5M. thể tích dung dịch NaOH 1M cần để trung hòa dung dịch X là
A. 10 ml.
B. 15 ml.
C. 20 ml.
D. 25 ml.
Cho 10ml dung dịch H 3 PO 4 1M vào 15ml dung dịch NaOH 1M thu được dung dịch X. Hãy cho biết thành phần chất tan trong X?
A. H 3 PO 4 và NaH 2 PO 4 .
B. Na 2 HPO 4 và Na 3 PO 4 .
C. NaH 2 PO 4 và Na 2 HPO 4 .
D. Na 3 PO 4 và NaOH .
Chọn C
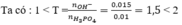
Vậy sau phản ứng thu được hai muối NaH 2 PO 4 và Na 2 HPO 4 .
Đổ 10ml dung dịch KOH vào 15ml dung dịch H2SO4 0,5M , dung dịch vẫn dư axit . Thêm 3ml dung dịch NaOH 1M vào thì dung dịch trung hòa . Nồng độ mol/l của dung dịch KOH là ?
Giả sử: \(C_{M\left(KOH\right)}=x\left(M\right)\)
Ta có: \(n_{H^+}=2n_{H_2SO_4}=2.0,015.0,5=0,015\left(mol\right)\)
\(\Sigma n_{OH^-}=0,01x+0,003\left(mol\right)\)
PT ion: \(OH^-+H^+\rightarrow H_2O\)
Do sau pư thu được dung dịch trung hòa nên:
\(n_{OH^-}=n_{H^+}\)
\(\Rightarrow0,01x+0,003=0,015\)
\(\Rightarrow x=1,2\)
Bạn tham khảo nhé!
Cho 10ml dung dịch hỗn hợp 2 axit HCl 2M và H2SO4 1M Để trung hòa hoàn toàn 10ml dung dịch 2 axit đó cần dùng vừa đủ bao nhiêu ml dung dịch NaOH 0,5M
nHCl= 0,02; nH2SO4 = 0,01
=> nH+=0,04
H+ + OH- ---> H2O
0,04 0,04
=> nNaOH= 0,04
=> V = 0,08(l)
Cần bao nhiêu lít dung dịch NaOH 0,5M để trung hoà 400 ml hỗn hợp dung dịch axit gồm H 2 S O 4 0,5M và HCl 1M?
A. 1,5 lít
B. 0,5 lít
C. 1,6 lít
D. 1,0 lít
Cho 10ml dung dịch hỗn hợp 2 axit HCl 2M và H2SO4 1M Để trung hòa hoàn toàn 10ml dung dịch 2 axit đó cần dùng vừa đủ bao nhiêu ml dung dịch NaOH 0,5M
Help meeeeee!!!!
\(PTHH:NaOH+HCl\rightarrow NaCl+H2O\)
\(2NaOH+H2SO4\rightarrow Na2SO4+H2O\)
Ta có : \(n_{HCL}=0,02\left(mol\right)\)
\(\Rightarrow n_{NaOH}=0,04\left(mol\right)\)
\(\Rightarrow V_{dd_{NaOH}}=\frac{0,04}{0,5}=0,08l=80ml\)
NaOH +HCl---.NaCl +H2O(1)
2NaOH +H2SO4----,Na2SO4+H2O(2)
n\(_{HCl}=0,01.2=0,02\left(mol\right)\)
n\(_{H2SO4}=0,01.1=0,01\left(mol\right)\)
Theo pthh1
n\(_{NaOH}=n_{HCl}=0,02\left(mol\right)\)
Theo pthh2
n\(_{NaOH}=2n_{H2SO4}=0,02\left(mol\right)\)
\(\Sigma n_{NaOH}=0,02+0,02=0,04\left(mol\right)\)
V\(_{NaOH}=\frac{0,04}{0,5}=0,08\left(l\right)=80ml\)
Cho 14,7 gam axit glutamic vào dung dịch H2SO4 0,5M và HCl 1M, thu được dung dịch X chứa 19,83 gam chất tan. Thể tích dung dịch NaOH 1M và KOH 0,6M cần lấy để phản ứng vừa đủ với chất tan trong dung dịch X là:
A. 160,0 ml
B. 225,0 ml
C. . 180,0 ml
D. 200,0 ml
Giải thích: Đáp án D
Glutamic: 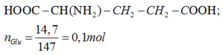
Ta có ∶ Glu + (HCl,H2SO4) ⟶ Muối
Bảo toàn khối lượng ta có :
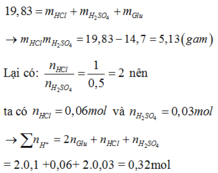
Suy ra số mol OH− cần để phản ứng với số chất tan trong dung dịch X cũng là số mol OH−phản ứng với tổng số mol H+
![]()