Tính oxi hóa của I2 so với F2, Cl2, Br2 thì
A. Mạnh hơn
B. Yếu hơn
C. Bằng nhau
D. Cả A và C
Đặc điểm nào dưới đây là đặc điểm chung của các đơn chất halogen (F2, Cl2, Br2,I2):
A. Ở điều kiện thường là chất khí.
B. Có tính oxi hóa mạnh.
C. Vừa có tính oxi hóa, vừa có tính khử.
D. Tác dụng mạnh với nước.
C1 :
Chọn phát biểu sai:
A. F2 oxi hóa mãnh liệt H2O.
B. Cl2 phản ứng một phần với H2O và oxi hóa được H2O.
C. Br2 phản ứng một phần với H2O và không oxi hóa được H2O.
D. I2 không phản ứng với H2O.
C2 :
Nhận xét nào đúng về tính chất hóa học của nhóm Halogen:
A. F2, Cl2, Br2, I2 chỉ có tính oxi hóa mạnh.
B. Tính khử giảm dần theo chiều F2 → I2.
C. Tính oxi hóa tăng dần theo chiều F2 → I2.
D. F2 chỉ có tính oxi hóa mạnh. Cl2, Br2, I2 vừa có tính oxi hóa, vừa có tính khử.
Giải thích nữa nha
1.
Chọn B.
Cl2 tác dụng với nước nhưng nó tự oxi hoá khử chính nó, nước chỉ là môi trường.
I2 phản ứng rất ít với nước, gần như là không phản ứng.
2.Chọn D
(F2 chỉ có thể giảm số oxi hoá 0 xuống -1 nên chỉ có tính oxi hoá. Các halogen khác có các số oxi hoá dương nên ngoài tính oxi hoá còn có tính khử)
Nêu tên tất cả các dẫn chứng chứng minh rằng tính oxi hóa của F2 > Cl2 > Br2 > I2
Tính oxi hóa:F2>Cl2>Br2>I2.phản ứng minh họa:
Flo phản ứng mãnh liệt với hiđro ở nhiệt độ thấp (-250 độ C):F2+H2--->2HF
Clo phản ứng với hidro trong điều kiện nhiệt độ và ánh sáng:Cl2+H2---->2HCl,
Brom phản ứng với hidro trong nhiệt độ cao:Br2+H2--to->2HBr,
Iot phản ứng với hiđro theo phản ứng thuận nghịch và cần xúc tác:I2+H2-<-->2HI.
Chất chỉ có tính oxi hoá là
A. F 2 B. Cl 2
C. Br 2 D. cả 3 chất F 2 , Cl 2 , Br 2
Dùng phản ứng với nước có chứng minh được tính oxi hóa của F2>Cl2 >Br2>I2 không ?
Ko thể vì
F2+H2O->HF+H2O
Cl2+H2O->HCl+HClO
Br2 ko tan nổi trên mặt nước
I2 ko tan chìm xuống nước
So sánh tính chất oxi hóa của các đơn chất F2,Cl2, Br2, I2 và tính khử của những hợp chất HF, HCl, HBr, HI. Dẫn ra những phương trình hóa học để minh họa.
Tính oxi hóa giảm dần từ F2 đến I2.
- Flo là phi kim mạnh nhất, oxi hóa được tất cả các kim loại kể cả vàng và platin. Clo, Br và Iot tác dụng được với một số kim loại.
- Phản ứng với hiđro.

- Halogen đứng trước đẩy halogen đứng sau ra khỏi muối của chúng:
Cl2 + 2NaBr → 2NaCl + Br2
Br2 + 2NaI → 2NaBr + I2
Tính khử của axit tăng theo chiều: HF < HCl < HBr < HI.
- Chỉ có thể oxi hóa F- bằng dòng điện. Còn ion Cl-, Br-, I- đều có thể bị oxi hóa khi tác dụng với chất oxi hóa mạnh.
- HF hoàn toàn không thể hiện tính khử, HCl chỉ thể hiện tính khử khi tác dụng với những chất oxi hóa mạnh, còn HBr và nhất là HI có tính khử mạnh. Axit sunfuric đặc bị HBr khử đến SO2 và bị HI khử đến H2S:
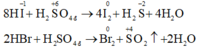
Các đơn chất Cl2, Br2, I2
A. là chất khí ở điều kiện thường
B. chỉ thể hiện tính oxi hóa
C. tác dụng mạnh với nước
D. vừa có tính oxi hóa vừa có tính khử
Dãy đơn chất nào sau đây vừa có tính oxi hóa vừa có tính khử?
A. Cl2 , O3, S.
B. S, Cl2, Br2.
C. Na, F2, S.
D. Br2, O2, Ca.
So sánh tc oxi hóa của các đơn chất F2. Cl2. Br2. I2. Dẫn ra pthh minh họa