hòa tan a gam kim loại canxi thì cần 200ml d CH3COOH 1mol:
a) viết PTHH
b) tính thể tích khí thu được ở ĐKTC
c) tính a.
Ai giúp mk vs mai mk thi r ...
hòa tan a gam kim loại canxi thì cần 200ml d CH3COOH 1mol:
a) viết PTHH
b) tính thể tích khí thu được ở ĐKTC
c) tính a.
Ai giúp mk vs mai mk thi r ...
Câu 5
A là dung dịch HCl. B là dung dịch Ba(OH)2.
Trộn 50 ml dung dịch A với 50 ml dung dịch B thu được dung dịch D có dư A. Để trung hòa hết lượng dư A trong D người ta phải dùng hết 50 ml dung dịch KOH 0,1M.
Trộn 50 ml dung dịch A với 150 ml dung dịch B thì thu được dung dịch E có dư B. Trung hòa hết lượng B dư trong E người ta phải dùng hết 350 ml dung dịch HNO3 0,1M. Tính nồng độ mol/lit của các dung dịch A, dung dịch B.
HELP ME!
Đặt nồng độ HCl trong dung dịch A là x
Đặt nồng độ Ba(OH)2 trong dung dịch B là y
- Khi trộn 50ml dung dịch A với 50ml dung dịch B thì HCl dư, ta có:
2HCl + Ba(OH)2 → BaCl2 + 2H2O (1)
0,1y← 0,05y mol
HCl + NaOH → NaCl + H2O (2)
0,005←0,005 mol
Ta có: 2.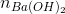 + nNaOH = nHCl
+ nNaOH = nHCl
0,1y + 0,005 = 0,05x
x– 2y = 0,1 (*)
- Khi trộn 50 ml dung dịch A với 150ml thì Ba(OH)2 dư, ta có:
2HCl + Ba(OH)2 → BaCl2 + 2H2O (3)
0,05x→0,025x mol
2HNO3 + Ba(OH)2 → Ba(NO3)2 + H2O (4)
0,035→ 0,0175 mol
Ta có: 2.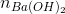 = (nHCl +
= (nHCl + 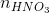 )
)
0,15y = 0,025x + 0,0175
x– 6y = - 0,7 (**)
Giải hệ pt:
x– 6y = -0,7
x– 2y = 0,1
=>x = 0,5; y= 0,2
=>CM của HCl = 0,5M
CM của Ba(OH)2 = 0,2M
Câu 1
a. Có một hỗn hợp rắn gồm KHCO3 và K2CO3, hòa tan hỗn hợp này vào nước được dung dịch A chứa x mol KHCO3 và y mol K2CO3.
- Nếu cho thêm (x+y) mol BaCl2 vào dung dịch A thu được m1 gam kết tủa.
- Nếu cho thêm (x+y) mol Ba(OH)2 vào dung dịch A thu được m2 gam kết tủa.
Hãy so sánh m1 và m2. Giải thích.
1/ Cho 200 ml dd Al(NO3)3 0.5M tác dụng với dd KOH 1M.Sau phản ứng thu được 3.9g chất rắn và dd A
a) V dd KOH cần dùng
b) Tính CM của dd A (Cho V dd không đổi
2) Nêu hiện tượng viết PTHH xảy ra khi cho từ từ dd Ba(OH)2 lần lượt vào ống nghiệm
a) dd CuSO4
b)dd AlCl3
bài 2, a, Ba(OH)2 + CuSO4--> Cu(OH)2 + BaSO4
xuất hiện kết tủa trắng sau khi kết thúc PỨ
b, 3Ba(OH)2 + 2AlCl3 --> 3BaCl2 + 2Al(OH)3
Sau khi kết thúc PỨ xuất hiện keo trắng rồi tan dần
Bài 2;
a. Ba(OH)2 + CuSO4 -> Cu(OH)2 + BaSO4
HT: xuất hiện kết tủa trắng
b. 3Ba(OH)2 + 2AlCl3 -> 3BaCl2 + 2Al(OH)3
Có thể: Ba(OH)2 dư + 2Al(OH)3 -> Ba(AlO2)2 + 4H2O
HT: Xuất hiện kết tủa trắng keo Al(OH)3, sau đó kết tủa tan trong dung dịch Ba(OH)2 dư
Bài 1:
a) nAl(NO3)3 = 0,5. (200/1000)= 0,1(mol)
PTHH: Al(NO3)3 + 3 KOH -> 3 KNO3 + Al(OH)3
- Chất rắn sau p.ứ là Al(OH)3
=> mAl(OH)3 = m(rắn) = 3,9(g)
=> nAl(OH)3 = 3,9/78= 0,05(mol)
=> nKOH= nKNO3= 3.0,05= 0,15(mol)
=> VddKOH= 0,15: 1= 0,15(l)=150(ml)
b) VddA= 200+150=350(ml)=0,35(l)
=> CMddA=CMddKNO3=0,15/0,35\(\approx0,429\left(M\right)\)