Nguyên tố R ó công thức cao nhất trong hợp chất với oxi là R 2 O 7 . Công thức hợp chất khí với hidro là
A. HR.
B. RH 4 .
C. H 2 R .
D. RH 3 .
Nguyên tố R ó công thức cao nhất trong hợp chất với oxi là R 2 O 7 . Công thức hợp chất khí với hidro là
A. HR.
B. RH 4 .
C. H 2 R .
D. RH 3 .
Oxit cao nhất của một nguyên tố có dạng R2O5 . Hợp chất khí với hidro của nguyên tố R có công thức phân tử là: * 4 điểm RH2 RH3 RH4 RH
Nguyên tố R có công thức hợp chất khí với Hidro là RH3. Trong công thức oxit cao nhất của nó có chứa 56,34% Oxi về khối lượng. Xác định nguyên tố R; công thức hợp chất khí với Hidro; hợp chất với oxi.
Gọi CTHH của R với oxi là: R2O3
Theo đề, ta có: \(\%_{O_{\left(R_2O_3\right)}}=\dfrac{16.3}{NTK_R.2+16.3}.100\%=56,34\%\)
=> \(NTK_R\approx19\left(đvC\right)\)
=> R là flo (F)
=> CTHH của R và H là: FH3
CTHH của R và O là: F2O3
Một nguyên tố có công thức oxit cao nhất là R2O7, nguyên tố này tạo với hiđro một chất khí trong đó hiđro chiếm 0,78% về khối lượng. Xác định nguyên tố R; công thức hợp chất khí với Hidro; hợp chất với oxi.
Nguyên tố R thuộc nhóm A, nguyên tố R có công thức oxit cao nhất R2O7, công thức hợp chất khí của nguyên tố R với hiđro là :
A. RH
B. RH2
C. RH3.
D. RH4.
Đáp án A
Oxit cao nhất là R2O7 => Hóa trị cao nhất của R là 7 => Hóa trị của R trong hợp chất khí với hiđro = 8 - 7= 1 => Công thức hợp chất khí của R với hiđro là RH
Nguyên tố R có công thức hợp chất khí với hidro là RH4. Oxit cao nhất của R có công thức.
Vì R có công thức hợp chất khí với Hidro là RH4 nên R có hóa trị 4
Vậy: Oxit cao nhất của R có công thức là \(R_2O_4=RO_2\)
Nguyên tố R tạo thành hợp chất khí với hiđro có công thức hoá học chung là RH 4 . Trong hợp chất có hoá trị cao nhất với oxi thì O chiếm 72,73% khối lượng. Viết công thức hoá học các hợp chất của nguyên tố R với oxi và hiđro.
Công thức hoá học các hợp chất với oxi và hiđro là CO 2 và CH 4
Nguyên tố R có công thức oxit cao nhất là R2O7. Trong hợp chất khí với Hiđrô khối lượng của nguyên tố R chiếm 97,26%. Nguyên tố R có số hiệu nguyên tử là
CTHH hợp chất với hidro là RH
Có \(\dfrac{M_R}{M_R+1}.100\%=97,26\%\)
=> MR = 35,5(Cl)
=> R là Cl, có số hiệu nguyên tử là 17
Nguyên tố R tạo hợp chất khí với hiđro có công thức RH3. Mặt khác trong công thức oxit cao nhất R chiếm 43,66% về khối lượng. R là:
A. Si = 28.
B. P = 31.
C. S = 32.
D. N = 14.
Chọn B.
Công thức với H là RH3 nên công thức oxit cao nhất là R2O5.
Ta có: %R = 43,66% => %O = 56,34%. Do đó:
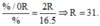
Vậy R là P (photpho).
Nguyên tố R tạo thành hợp chất khí với hiđro có công thức hoá học chung là RH 4 . Trong hợp chất có hoá trị cao nhất với oxi thì O chiếm 72,73% khối lượng. Hãy xác định tên nguyên tố R.
Nguyên tố R tạo thành hợp chất khí với hiđro có công thức là RH 4 sẽ tạo thành hợp chất oxit cao nhất là RO 2 có phần trăm khối lượng của nguyên tô R :
100% - 72,73% = 27,27%
72,73% phân tử khối của RO 2 ứng với 16 x 2 = 32 (đvC).
27,27% phân tử khối của RO 2 ứng với nguyên tử khối của nguyên tố R là :
32x27,27/72,73 = 12 (đvC) => R là cacbon (C)