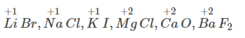Hãy so sánh hoá trị của các kim loại trong các hợp chất :NaCl, CaF 2

Những câu hỏi liên quan
Hãy cho biết số oxi hoá của các kim loại trong các hợp chất sau đây :
LiBr, NaCl, KI, MgCl 2 , CaO, BaF 2
Hãy so sánh hoá trị của oxi (O) và của nitơ (N) trong các hợp chất : H 2 O ; NH 3 )
Trong các hợp chất H 2 O ; NH 3 , nitơ có cộng hoá trị lớn hơn cộng hoá trị của oxi
Đúng 0
Bình luận (0)
Nguyên tố A có số nguyên tử là 11 hãy cho biết: a) Cấu tạo nguyên tử của nguyên tố A, vị trí của A trong bản tuần hoàn các Nguyên Tố Hoá Học b) Dự đoán: Tính chất của A làm kim loại hay phi kim c) So sánh tính chất hoá học của A với các nguyên tố lân cận
a: Cấu tạo nguyên tử của A là 11 proton và 11 electron
Cấu hình: \(1s^22s^22p^63s^1\)
Vị trí: Chu kì 3, nhóm IA
b: A là kim loại vì có 1 e lớp ngoài cùng
Đúng 0
Bình luận (0)
Điện hoá trị của các nguyên tố O, S trong các hợp chất với các nguyên tổ kim loại kiềm đều là
A. 2 -
B. 2+
C. 6 -
D. 6+
1. Một hợp chất X có công thức M2SO4, trong đó M là 1 kim loại chưa biết, phân tử X nặng bằng 71 lần phân tử H2. Hãy xác định kim loại M và hoá trị của kim loại M trong hợp chất.
Đọc tiếp
1. Một hợp chất X có công thức M2SO4, trong đó M là 1 kim loại chưa biết, phân tử X nặng bằng 71 lần phân tử H2. Hãy xác định kim loại M và hoá trị của kim loại M trong hợp chất.
\(M_X=71.2=142\left(amu\right)\)
<=> \(2M+96=142\Rightarrow M=23\)
Kim loại M là sodium, hóa trị của M trong hợp chất là hóa trị I
Đúng 1
Bình luận (0)
\(M_X=71\cdot2=142\left(\dfrac{g}{mol}\right)\)
\(\Rightarrow2M+32+16\cdot4=142\)
\(\Rightarrow M=23\)
M là : Na và có hóa trị I trong hợp chất X
Đúng 1
Bình luận (0)
Câu 3:
1. Một hợp chất X có công thức M2SO4, trong đó M là 1 kim loại chưa biết, phân tử X nặng bằng 71 lần phân tử H2. Hãy xác định kim loại M và hoá trị của kim loại M trong hợp chất.
Đọc tiếp
Câu 3:
1. Một hợp chất X có công thức M2SO4, trong đó M là 1 kim loại chưa biết, phân tử X nặng bằng 71 lần phân tử H2. Hãy xác định kim loại M và hoá trị của kim loại M trong hợp chất.
Bài 2. Viết sơ đồ giải thích sự hình thành liên kết ion trong các hợp chất sau: NaCl, CaO , K2O, MgCl2. Xác định điện hoá trị của các nguyên tố Na, Ca, Mg, O, Cl trong các hợp chất trên
Hãy thực hiện các yêu cầu sau :
a) Tìm hoá trị của Sắt ( Fe ) trong hợp chất FeO
b) Tìm hoá trị của Lưu huỳnh ( S ) trong hợp chất SO3
a. Gọi hóa trị của Fe là a ta có 1 x a = 1 x II ( Theo quy tắc hóa trị )
Suy ra a = II hay hóa trị của Fe trong hợp chất là II
b. Gọi hóa trị của S là a ta có 1 x a = 3 x II ( Theo quy tắc hóa trị )
Suy ra a= IV hay hóa trị của S trong hợp chất là IV
Đúng 0
Bình luận (2)
a/ Đặt hóa trị của Fe trong hợp chất FeO là a
Vì O trong mọi hợp chất đều có hóa trị là 2
Theo qui tắc hóa trị, ta có:
\(1\times a=2\times1\Rightarrow a=2\)
Vậy hóa trị của Fe trong hợp chất FeO là 2
b/ Đặt hóa trị của S trong hợp chất SO3 là x
Vì O trong mọi hợp chất đều có hóa trị là 2
Theo qui tắc hóa trị ta có:
\(1\times x=2\times3\)
=> x = 6
Vậy hóa trị của S trong hợp chất SO3 là 6
Đúng 0
Bình luận (5)
Đặt a là hoá trị của Fe.
Ta có công thức Fe^aO^II
Áp dụng quy tắc hoá trị ax = by ta có: a.1= II.1
=> a=II.1/1=II.
Hoá trị của Fe là II
Tương tự của S sẽ là VI
Đúng 0
Bình luận (0)
Xem thêm câu trả lời
Câu 3: 1. Một hợp chất X có công thức M2SO4, trong đó M là 1 kim loại chưa biết, phân tử X nặng bằng 71 lần phân tử H2. Hãy xác định kim loại M và hoá trị của kim loại M trong hợp chất.SOS
Đọc tiếp
Câu 3:
1. Một hợp chất X có công thức M2SO4, trong đó M là 1 kim loại chưa biết, phân tử X nặng bằng 71 lần phân tử H2. Hãy xác định kim loại M và hoá trị của kim loại M trong hợp chất.
SOS
\(M_X=71\cdot M_{H_2}=71\cdot2=142\)
=>\(2\cdot M+64+4\cdot16=142\)
=>\(2M=14\)
=>M=7
=>M là Li
Hóa trị của Li là I
Đúng 2
Bình luận (1)