Thể tích khí clo cần phản ứng với kim loại M bằng 1,5 lần lượng khí sinh ra khi cho cùng lượng kim loại đó tác dụng hoàn toàn với dung dịch axit HCl dư trong cùng điều kiện. Khối lượng muối clorua sinh ra trong phản ứng với clo gấp 1,2886 lần lượng sinh ra trong phản ứng với axit HCl. Xác định kim loại M

Những câu hỏi liên quan
Khi cho cùng một lượng kim loại M vào dung dịch HNO3 đặc nóng dư và dung dịch H2SO4 loãng dư, phản ứng hoàn toàn thì thể tích khí NO2 (sản phẩm khử duy nhất) thu được gấp 3 lần thể tích khí H2 ở cùng điều kiện nhiệt độ và áp suất. Khối lượng muối sunfat thu được bằng 62,81% khối lượng muối nitrat tạo thành. Xác định kim loại M? A. Zn B. Fe C. Mg D. Ca
Đọc tiếp
Khi cho cùng một lượng kim loại M vào dung dịch HNO3 đặc nóng dư và dung dịch H2SO4 loãng dư, phản ứng hoàn toàn thì thể tích khí NO2 (sản phẩm khử duy nhất) thu được gấp 3 lần thể tích khí H2 ở cùng điều kiện nhiệt độ và áp suất. Khối lượng muối sunfat thu được bằng 62,81% khối lượng muối nitrat tạo thành. Xác định kim loại M?
A. Zn
B. Fe
C. Mg
D. Ca
Gọi n, m là hóa trị của R khi tác dụng HNO3 và H2SO4 loãng ( 1≤ m≤ n≤ 3)
Chọn nR= 1 mol
2R + mH2SO4 →R2(SO4)m + mH2↑
1 → 0,5 0,5m
R + 2nHNO3 →R(NO3)n + nNO2 + nH2O
1 1 n
Ta có: n=3.0,5m n=1,5m m=2, n=3 là phù hợp.
Ta có: (R + 96)=(R + 186). 0,6281 R=56 R là Fe.
Đáp án B
Đúng 0
Bình luận (0)
Thể tích khí Cl2 cần phản ứng với kim loại M bằng 1,5 lần lượng khí Cl2 sinh ra khi cho cùng
lượng kim loại đó tác dụng hoàn toàn với dung dịch HCl dư trong cùng điều kiện . Khối lượng muối
sinh ra trong phản ứng với Cl2 gấp 1, 2886 lần lượng sinh ra trong phản ứng với axit HCl . M là kim loại
nào sau đây.
a. Al b. Cr c. Fe d. K
\(M+mHCl\rightarrow MCl_m+\frac{m}{2}H_2\)
\(M+\frac{n}{2}Cl_2\rightarrow MCl_n\)
Giải hệ PT:
\(\left\{{}\begin{matrix}\frac{n}{2}+1,5\frac{m}{2}\\n,m=1,2,3\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}n=3\\m=2\end{matrix}\right.\)
\(M+106,5=1,2886\left(M+71\right)\)
\(\Rightarrow M=52\left(Cr\right)\)
Đáp án đúng B
Đúng 0
Bình luận (0)
Cho hỗn hợp bột các kim loại FA là kim loại có hóa trị n hòa tan bằng dung dịch HCl vừa đủ thì thu được 7,84 lít khí ở điều kiện tiêu chuẩn hỗn hợp trên tác dụng với 8,4 lít khí Clo điều kiện tiêu chuẩn thì phản ứng xảy ra hoàn toàn biết rằng hỗn hợp đêm trộn 1:4a) xác định hóa trị và thanh kim loại a biết khối lượng a bằng 5,4 gamb) tính thể tích khí clo để hòa hợp với kim loại a và khối lượng dung dịch HCl 36% Cần cho phản ứng trên
Đọc tiếp
Cho hỗn hợp bột các kim loại FA là kim loại có hóa trị n hòa tan bằng dung dịch HCl vừa đủ thì thu được 7,84 lít khí ở điều kiện tiêu chuẩn hỗn hợp trên tác dụng với 8,4 lít khí Clo điều kiện tiêu chuẩn thì phản ứng xảy ra hoàn toàn biết rằng hỗn hợp đêm trộn 1:4
a) xác định hóa trị và thanh kim loại a biết khối lượng a bằng 5,4 gam
b) tính thể tích khí clo để hòa hợp với kim loại a và khối lượng dung dịch HCl 36% Cần cho phản ứng trên
Bài 1: Cho các kim loại Zn,Al,Để lần lượt tác dụng với dung dịch axit HCl
a, Viết các PTHH của phản ứng
b, Cho cùng 1 khối lượng các kim loại trên tác dụng với axit dư thì kim loại nào cho nhiều khí H² nhất?
c, Nếu thu được cùng 1 thể tích khí H² thì khối lượng của kim loại nào đã phản ứng là nhỏ nhất?
Bài 2: Cho 11,2g Fe tác dụng với dung dịch loãng có chứa 9,8g axit H²SO⁴
a, Chất nào còn dư sau phản ứng và dư bao nhiêu g?
b, Tính thể tích khí H² thu được ở đktc
- Xác định nguyên tố kim loại
Đọc tiếp
Bài 1: Cho các kim loại Zn,Al,Để lần lượt tác dụng với dung dịch axit HCl
a, Viết các PTHH của phản ứng
b, Cho cùng 1 khối lượng các kim loại trên tác dụng với axit dư thì kim loại nào cho nhiều khí H² nhất?
c, Nếu thu được cùng 1 thể tích khí H² thì khối lượng của kim loại nào đã phản ứng là nhỏ nhất?
Bài 2: Cho 11,2g Fe tác dụng với dung dịch loãng có chứa 9,8g axit H²SO⁴
a, Chất nào còn dư sau phản ứng và dư bao nhiêu g?
b, Tính thể tích khí H² thu được ở đktc
- Xác định nguyên tố kim loại
Bài 1:
a, PT: \(Zn+2HCl\rightarrow ZnCl_2+H_2\) (1)
\(2Al+6HCl\rightarrow2AlCl_3+3H_2\) (2)
b, Giả sử: mZn = mAl = a (g)
\(\Rightarrow\left\{{}\begin{matrix}n_{Zn}=\dfrac{a}{65}\left(mol\right)\\n_{Al}=\dfrac{a}{27}\left(mol\right)\end{matrix}\right.\)
Theo PT: \(\left\{{}\begin{matrix}n_{H_2\left(1\right)}=n_{Zn}=\dfrac{a}{65}\left(mol\right)\\n_{H_2\left(2\right)}=n_{Al}=\dfrac{a}{27}\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow n_{H_2\left(1\right)}< n_{H_2\left(2\right)}\)
Vậy: Al cho nhiều khí H2 hơn.
c, Giả sử: nH2 (1) = nH2 (2) = b (mol)
Theo PT: \(\left\{{}\begin{matrix}n_{Zn}=n_{H_2\left(1\right)}=b\left(mol\right)\\n_{Al}=n_{H_2\left(2\right)}=b\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}m_{Zn}=65b\left(g\right)\\m_{Al}=27b\left(g\right)\end{matrix}\right.\)
\(\Rightarrow m_{Zn}>m_{Al}\)
Vậy: Khối lượng Al đã pư nhỏ hơn.
Bài 2:
PT: \(Fe+H_2SO_4\rightarrow FeSO_4+H_2\)
a, Ta có: \(n_{Fe}=\dfrac{11,2}{56}=0,2\left(mol\right)\)
\(n_{H_2SO_4}=\dfrac{9,8}{98}=0,1\left(mol\right)\)
Xét tỉ lệ: \(\dfrac{0,2}{1}>\dfrac{0,1}{1}\), ta được Fe dư.
Theo PT: \(n_{Fe\left(pư\right)}=n_{H_2SO_4}=0,1\left(mol\right)\)
\(\Rightarrow n_{Fe\left(dư\right)}=0,1\left(mol\right)\Rightarrow m_{Fe\left(dư\right)}=0,1.56=5,6\left(g\right)\)
b, Theo PT: \(n_{H_2}=n_{H_2SO_4}=0,1\left(mol\right)\)
\(\Rightarrow V_{H_2}=0,1.22,4=2,24\left(l\right)\)
Bạn tham khảo nhé!
Đúng 2
Bình luận (2)
Khi hoà tan hoàn toàn m gam kim loại M trong dung dịch HNO3 dư thu được V lít NO duy nhất. Mặt khác, hoà tan hoàn toàn m gam M trong dung dịch HCl dư cũng thu được V lít khí, khối lượng muối clorua thu được bằng 52,48% khối lượng muối nitrat thu được ở trên. Các khí đo ở cùng điều kiện, M là: A. Mn. B. Cr. C. Fe. D. Al.
Đọc tiếp
Khi hoà tan hoàn toàn m gam kim loại M trong dung dịch HNO3 dư thu được V lít NO duy nhất. Mặt khác, hoà tan hoàn toàn m gam M trong dung dịch HCl dư cũng thu được V lít khí, khối lượng muối clorua thu được bằng 52,48% khối lượng muối nitrat thu được ở trên. Các khí đo ở cùng điều kiện, M là:
A. Mn.
B. Cr.
C. Fe.
D. Al.
cho 32,4 gam kim loại nhôm tác dụng với 23,7984 lít khí oxi (đkt)
a.chất nào còn dư sau phản ứng
b.tính khối lượng nhôm oxit tạo thành sau phản ứng
c.cho toàn bộ lượng khí kim loại nhôm ở trên vào dung dịch axit HCL .Sau khi phản ứng sảy ra hoàn toàn thu đc bao nhiêu lít khí H2 ở (đkt)
n Al=\(\dfrac{32,4}{27}\)=1,2 mol
n O2=\(\dfrac{23,7984}{22,4}\)=1,062mol
4Al+3O2-to>2Al2O3
1,2---------------0,6 mol
O2 dư
=>m Al2O3=0,6.102=61,2g
2Al+6HCl->2AlCl3+3H2
1,2-----------------------1,8 mol
=>VH2=1,8.22,4=40,32l
Đúng 3
Bình luận (0)
Câu 3: Cho kim loại Nhôm (Al) tác dụng với dung dịch axit Clo hidric (HCl) sau phản ứng thu được muối Nhôm Clorua (AlCl3) và 6,72 lít khí Hidro (H2) ở đktc.a. Tính khối lượng axit Clo hidric (HCl) tham gia.b. Tính khối lượng Nhôm tham gia phản ứng.
Đọc tiếp
Câu 3: Cho kim loại Nhôm (Al) tác dụng với dung dịch axit Clo hidric (HCl) sau phản ứng thu được muối Nhôm Clorua (AlCl3) và 6,72 lít khí Hidro (H2) ở đktc.
a. Tính khối lượng axit Clo hidric (HCl) tham gia.
b. Tính khối lượng Nhôm tham gia phản ứng.
a, PT: \(2Al+6HCl\rightarrow2AlCl_3+3H_2\)
Ta có: \(n_{H_2}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\)
Theo PT: \(n_{HCl}=2n_{H_2}=0,6\left(mol\right)\)
\(\Rightarrow m_{HCl}=0,6.36,5=21,9\left(g\right)\)
b, Theo PT: \(n_{Al}=\dfrac{2}{3}n_{H_2}=0,2\left(mol\right)\)
\(\Rightarrow m_{Al}=0,2.27=5,4\left(g\right)\)
Đúng 2
Bình luận (0)
nH2=6.72/22,4=0,3(mol)
PTHH: 2Al + 6HCl --> 2AlCl3 + 3H2
bài ra: 0,2 <-- 0,6 <-- 0,2 <-- 0,3 /mol
a) mHCl = 0,6.36,5=21,9(g)
b) mAl = 0.2.24 = 4,8(g)
Đúng 0
Bình luận (1)
Câu 3: Cho kim loại Nhôm (Al) tác dụng với dung dịch axit Clo hidric (HCl) sau phản ứng thu được muối Nhôm Clorua (AlCl3) và 6,72 lít khí Hidro (H2) ở đktc.a. Tính khối lượng axit Clo hidric (HCl) tham gia.b. Tính khối lượng Nhôm tham gia phản ứng.
Đọc tiếp
Câu 3: Cho kim loại Nhôm (Al) tác dụng với dung dịch axit Clo hidric (HCl) sau phản ứng thu được muối Nhôm Clorua (AlCl3) và 6,72 lít khí Hidro (H2) ở đktc.
a. Tính khối lượng axit Clo hidric (HCl) tham gia.
b. Tính khối lượng Nhôm tham gia phản ứng.
\(PTHH:2Al+6HCl->2AlCl_3+3H_2\)
0,2<--0,6<----------0,2<------0,3 (mol)
\(n_{H_2\left(dktc\right)}=\dfrac{V}{22,4}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\)
\(m_{HCl}=n\cdot M=0,6\cdot\left(1+35,5\right)=21,9\left(g\right)\)
\(m_{AlCl_3}=n\cdot M=0,2\cdot\left(27+35,5\cdot3\right)=26,7\left(g\right)\)
Đúng 0
Bình luận (0)
a, PT: 2Al+6HCl→2AlCl3+3H2
Ta có: nAl=23nH2=0,2(mol)
⇒mAl=0,2.27=5,4(g)
Đúng 0
Bình luận (0)
a, PT: 2Al+6HCl→2AlCl3+3H2
Ta có: nAl=23nH2=0,2(mol)
⇒mAl=0,2.27=5,4(g)
Đúng 0
Bình luận (0)
Cho các kim loại kẽm, nhôm, sắt lần lượt tác dụng với dung dịch axit sunfuric loãng. a) Viết các phương trình phản ứng. b) Cho cùng một khối lượng các kim loại trên tác dụng hết với axit sunfuric? Kim loại nào cho nhiều khi hiđro nhất? c) Nếu thu được cùng một thể tích khí hiđro thì khối lượng kim loại nào nhỏ nhất?
Đọc tiếp
Cho các kim loại kẽm, nhôm, sắt lần lượt tác dụng với dung dịch axit sunfuric loãng.
a) Viết các phương trình phản ứng.
b) Cho cùng một khối lượng các kim loại trên tác dụng hết với axit sunfuric? Kim loại nào cho nhiều khi hiđro nhất?
c) Nếu thu được cùng một thể tích khí hiđro thì khối lượng kim loại nào nhỏ nhất?
a) Phương trình phản ứng:
Zn + H2SO4 → ZnSO4 + H2
Fe + H2SO4loãng → FeSO4 + H2
2Al+ 3H2SO4 → Al2(SO4)3 + 3H2
b) Giả sử cho cùng một khối lượng là a g kim loại kẽm sắt và nhôm
Zn + H2SO4 → ZnSO4 + H2 (1)
Fe + H2SO4loãng → FeSO4 + H2 (2)
2Al+ 3H2SO4 → Al2(SO4)3 + 3H2 (3)
Ta có 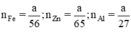
Theo pt nH2 (1) = nZn = 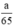 mol
mol
nH2 (2) = nFe = 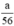 mol
mol
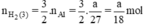
Như vậy ta nhận thấy 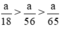 ⇒ nH2 (3) > nH2 (2) > nH2 (1)
⇒ nH2 (3) > nH2 (2) > nH2 (1)
Như vậy cho cùng một lượng kim loại tác dụng với axit H2SO4 loãng dư thì nhôm cho nhiều khí hidro hơn, sau đó đến sắt và ít nhất là kẽm
c) Nếu thu được cùng một lượng khí hidro thì khối lượng kim loại ít nhất là nhôm, sau đó đến sắt, cuối cùng là kẽm.
Đúng 1
Bình luận (0)



















