hòa tan mg kim loại kiềm M vào 7.8g nước được dd A có nồng độ 40%và 1.12l h2 kim loại M là

Những câu hỏi liên quan
Hòa tan hoàn toàn m gam một kim loại kiềm R vào nước , sau phản ứng thu được 3,36 lít H2 và 200gam dd chứa một chất tan X có nồng độ là 6% . Xác định kim loại R
Xem chi tiết
R + H2O -> ROH + 1/2 H2
nH2= 0,15(mol)
=> nROH=0,3(mol)
mROH= 6%.200=12(g)
=> M(ROH)= 12/0,3=40(g/mol)
Mà: M(ROH)=M(R)+17
=>M(R)+17=40
=>M(R)=23(g/mol) => R là Natri (Na=23)
Đúng 2
Bình luận (0)
Hòa tan hết 5,85g kim loại kiềm M vào 78,3ml H2O. Sau phản ứng thu được dd A có nồng độ 10%. Kim loại M là:
Đọc tiếp
Hòa tan hết 5,85g kim loại kiềm M vào 78,3ml H2O. Sau phản ứng thu được dd A có nồng độ 10%. Kim loại M là:
PTHH: A+H2O→AOH+1\2H2
1 (mol) ........................ 0.5 (mol)
Theo đề, ta có:
nH2=0.15\2=0.075(mol)
Mặt khác, theo phương trình:
nM=2.nH2=2.0.075=0.15(mol)
⇒M=5.85\0.15=39(đvC)
Vậy M là Kali (K).
Đúng 2
Bình luận (0)
Hòa tan hoàn toàn 2,9g hỗn hợp gồm kim loại M và oxit của nó vào nước , thu được 500ml dd chứa một chất tan có nồng độ 0,04M, và 0,224l khí H2 (đktc). Kim loại M là A. K B. Na C. Ba D. Ca
Đọc tiếp
Hòa tan hoàn toàn 2,9g hỗn hợp gồm kim loại M và oxit của nó vào nước , thu được 500ml dd chứa một chất tan có nồng độ 0,04M, và 0,224l khí H2 (đktc). Kim loại M là
A. K
B. Na
C. Ba
D. Ca
Đáp án C
M : x mol ; M2On : y mol
M + H2O → M(OH)n + n/2 H2
x x n 2 x
=> n 2 x = 0,01 => nx = 0,02
M2On + nH2O →2M(OH)n
y 2y
⇒ n M(OH)n = x + 2y = 0,02
+) n = 1 (KL kiềm ) ⇒x = 0,02 ; y = 0 ⇒ B. loại
+) n = 2 (KL kiềm thổ) ⇒ x = 0,01 , y = 0,05
⇒ mhh = 0,01.M + 0,05.(2M + 16.2) = 2,9
⇒ M = Ba
Đúng 0
Bình luận (0)
Hòa tan hoàn toàn 2,9g hỗn hợp gồm kim loại M và oxit của nó vào nước , thu được 500ml dd chứa một chất tan có nồng độ 0,04M và 0,224l khí H2 (đktc). Kim loại M là: A. K B. Na C. Ba D. Ca
Đọc tiếp
Hòa tan hoàn toàn 2,9g hỗn hợp gồm kim loại M và oxit của nó vào nước , thu được 500ml dd chứa một chất tan có nồng độ 0,04M và 0,224l khí H2 (đktc). Kim loại M là:
A. K
B. Na
C. Ba
D. Ca
Đáp án B
M : x mol ; M2On : y mol
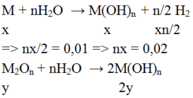
⇒ n M(OH)n = x + 2y = 0,02
+) n = 1 (KL kiềm ) ⇒ x = 0,02 ; y = 0 ⇒ loại
+) n = 2 (KL kiềm thổ) ⇒ x = 0,01 , y = 0,005
⇒ mhh = 0,01.M + 0,005.(2M + 16.2) = 2,9
⇒ M = Ba
Đúng 0
Bình luận (0)
Bài 6: Hòa tan 36,6 hỗn hợp A (Na và Ba) vào 167,2g nước sau phản ứng thu được dung dịch kiềm B và 8,96 lít H2(ĐKTC).
a) Tính thành phần% khối lượng hhA kim loại .
b) Tính nồng độ % của dd kiềm B ?
a,\(n_{H_2}=\dfrac{8,96}{22,4}=0,4\left(mol\right)\)
PTHH: 2Na + 2H2O → 2NaOH + H2
Mol: x 0,5x
PTHH: Ba + 2H2O → Ba(OH)2 + H2
Mol: y y
Ta có: \(\left\{{}\begin{matrix}23x+137y=36,6\\0,5x+y=0,4\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}x=0,4\\y=0,2\end{matrix}\right.\)
\(\%m_{Na}=\dfrac{0,4.23.100\%}{36,6}=25,17\%;\%m_{Ba}=100-25,17=74,83\%\)
b,
PTHH: 2Na + 2H2O → 2NaOH + H2
Mol: 0,4 0,4
PTHH: Ba + 2H2O → Ba(OH)2 + H2
Mol: 0,2 0,2
mdd sau pứ = 36,6+167,2-0,4.2 = 203 (g)
\(C\%_{ddNaOH}=\dfrac{0,4.40.100\%}{203}=7,88\%\)
\(C\%_{ddBa\left(OH\right)_2}=\dfrac{0,2.171.100\%}{203}=16,85\%\)
Đúng 1
Bình luận (0)
hòa tan hoàn toàn 9,2 gam hỗn hợp X gồm hai kim loại kiềm vào 400ml dung dịch HCl 0,5 M thu được dd Y chứa 4 chất tan có nồng độ mol bằng nhau , hai kim loại đó là gì?
nếu HCl dư=> chỉ có 3 chất tan
Nếu HCl đủ=> chỉ có 2 chất tan
=> HCl thiếu => 2 muối và 2 dd kiềm
thay vào để giải nghiệm thì chỉ có Li và K thỏa mãn=> 2 kim loại cần tìm là Liti vs Kali
Đúng 0
Bình luận (0)
hòa tan 14,4 g kim loại kiềm thổ M vào 182,5 ml đd Hcl (d=1,2g/ml) thu được 13,44 lit khí (dktc) và đd b
a) tìm tên kim loại
b) xác định nồng độ % của chất tan trong dd b?
$a)PTHH:M+2HCl\to MCl_2+H_2$
$n_{H_2}=\dfrac{13,44}{22,4}=0,6(mol)$
Theo PT: $n_M=n_{H_2}=0,6(mol)$
$\Rightarrow M_M=\dfrac{14,4}{0,6}=24(g/mol)$
Vậy M là Mg
$b)m_{dd_{HCl}}=182,5.1,2=219(g)$
Theo PT: $n_{MgCl_2}=n_{Mg}=0,6(mol)$
$\Rightarrow C\%_{MgCl_2}=\dfrac{0,6.95}{14,4+219-0,6.2}.100\%=24,55\%$
Đúng 2
Bình luận (0)
Hòa tan 3,68 g một kim loại kiềm M hòa tan vào nước dư, thu được 1,792 lit khí H, (đktc) và 200 ml dung dịch X. a-Xác định tên kim loại kiểm. b-Tính nồng độ moll của dung dịch X.
Gọi M là khối lượng mol trung bình của 2 nguyên tố
nH2=6.72/22.4=0.3 mol
M + H2O --> MOH + 1/2 H2
0.6mol---------------------0.3mol
-> M=20.2/0.3=67.3333
-->M1<67.33<M2
mà 2 kim loại này thuộc hai chu kì liên tiếp nhau
--> Kim loại đó là KI và Rb
Đúng 1
Bình luận (0)
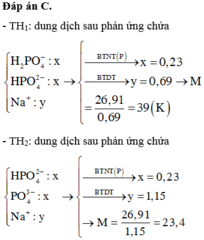
Hòa tan hết 26,91 gam kim loại kiềm M vào nước (dư), thu được dung dịch X. Cho 32,66 gam P2O5 tác dụng hết với X, thu được dung dịch chỉ chứa hai muối có cùng nồng độ mol. Kim loại M là A. Li. B. Na. C. K. D. Rb.
Đọc tiếp
Hòa tan hết 26,91 gam kim loại kiềm M vào nước (dư), thu được dung dịch X. Cho 32,66 gam P2O5 tác dụng hết với X, thu được dung dịch chỉ chứa hai muối có cùng nồng độ mol. Kim loại M là
A. Li.
B. Na.
C. K.
D. Rb.