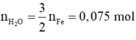Hoà tan m gam nhôm bằng lượng dư dd NAOH thủ được 1,12 lít khí ( đktc).Giá trị m là

Những câu hỏi liên quan
Hoà tan hoàn toàn m gam Cu trong dd HNO3 thu được 1,12 lít hỗn hợp khí NO và NO2 (đktc) có tỉ khối hơi đối với H2 là 16,6. Giá trị của m là: A. 8,32 B. 4,16 C. 3,90 D. 6,40
Đọc tiếp
Hoà tan hoàn toàn m gam Cu trong dd HNO3 thu được 1,12 lít hỗn hợp khí NO và NO2 (đktc) có tỉ khối hơi đối với H2 là 16,6. Giá trị của m là:
A. 8,32
B. 4,16
C. 3,90
D. 6,40
M (trung bình NO và NO2) = 16,6.2 = 33.2 gam. n (NO và NO2) = 0.05 (mol)
Gọi x = số mol NO, y = số mol NO2.
Ta có hệ phương trình:
x + y = 0.05
( 30x + 46y )/ (x + y) = 33.2
Giải hệ phương trình => x = 0.04, y = 0.01
Số mol HNO3 phản ứng = 0,04 . 4 + 0,01 . 2 = 0.18 mol.
3 Cu ........ + ..... 8HNO3 ------> ........
0.0675.................0.18 => m Cu = 0.0675 . 64 = 4.32 gam.
=> Đáp án B
Đúng 0
Bình luận (0)
Hoà tan a gam hỗn hợp bột Mg, Al bằng dung dịch HCl thu được 17,92 lit khí H2 (ở đktc). Cùng lượng hỗn hợp trên hoà tan trong dung dịch NaOH dư thu được 13,44 lít khí H2 (ở đktc). Giá trị của a là A. 3,9 B. 7,8 C. 11,7 D. 15,6
Đọc tiếp
Hoà tan a gam hỗn hợp bột Mg, Al bằng dung dịch HCl thu được 17,92 lit khí H2 (ở đktc). Cùng lượng hỗn hợp trên hoà tan trong dung dịch NaOH dư thu được 13,44 lít khí H2 (ở đktc). Giá trị của a là
A. 3,9
B. 7,8
C. 11,7
D. 15,6
Đáp án D
• a gam Mg (x mol), Al (y mol) + HCl → 0,8 mol H2↑
→ x + 3/2y = 0,8 (*)
• a gam Mg, Al + NaOH dư → 0,6 mol H2↑
→ 3/2y = 0,6 → y = 0,4 mol → x = 0,2 mol
→ a = mMg + mAl = 0,2 × 24 + 0,4 × 27 = 15,6 gam
Đúng 0
Bình luận (0)
Hoà tan 23,7 hỗn hợp kim loại gồm Mg , Al , Ag bằng dd HCl (lấy dư) thu được dd X ; 14,56 lít khí H2 (đktc) và 10,8g chất rắn Y . Cô cạn dd X thu được m gam muối . Giá trị của m là
10,8 g chất rắn đó là Ag không tan trong dd HCl
=> mMg + mAl = 23,7 - 10,8 = 12,9 (g)
nH2 = 14,56/22,4 = 0,65 (mol)
PTHH:
Mg + 2HCl -> MgCl2 + H2
2Al + 6HCl -> 2AlCl3 + 3H2
Theo 2 PTHH trên: nHCl = 2nH2 = 2 . 0,65 = 1,3 (mol)
Áp dụng ĐLBTKL, ta có:
mAl + mMg + mHCl = m(muối) + mH2
=> m(muối) = 12,9 + 36,5 . 1,3 - 0,65 . 2 = 59,05 (g)
Đúng 1
Bình luận (1)
Khử hoàn toàn một lượng Fe2O3 bằng H2 dư, thu được chất rắn X và m gam H2O. Hòa tan hết X trong dung dịch HCl dư, thu được 1,12 lít khí H2 (đktc). Giá trị của m là A. 1,80. B. 1,35. C. 0,90. D. 4,00.
Đọc tiếp
Khử hoàn toàn một lượng Fe2O3 bằng H2 dư, thu được chất rắn X và m gam H2O. Hòa tan hết X trong dung dịch HCl dư, thu được 1,12 lít khí H2 (đktc). Giá trị của m là
A. 1,80.
B. 1,35.
C. 0,90.
D. 4,00.
Đáp án B.
Có:
n F e = n H 2 = 1 , 12 22 , 4 = 0 , 05 m o l ⇒ n H 2 O = 3 2 n F e = 0 , 075 m o l ⇒ m = 18 . 0 , 075 = 1 , 35 g
Đúng 0
Bình luận (0)
Khử hoàn toàn một lượng Fe2O3 bằng H2 dư, thu được chất rắn X và m gam H2O. Hòa tan hết X trong dung dịch HCl dư, thu được 1,12 lít khí H2 (đktc). Giá trị của m là A. 1,80. B. 1,35. C. 0,90. D. 4,00.
Đọc tiếp
Khử hoàn toàn một lượng Fe2O3 bằng H2 dư, thu được chất rắn X và m gam H2O. Hòa tan hết X trong dung dịch HCl dư, thu được 1,12 lít khí H2 (đktc). Giá trị của m là
A. 1,80.
B. 1,35.
C. 0,90.
D. 4,00.
Khử hoàn toàn một lượng Fe2O3 bằng H2 dư, thu được chất rắn X và m gam H2O. Hòa tan hết X trong dung dịch HCl dư, thu được 1,12 lít khí H2 (đktc). Giá trị của m là A. 1,35 B. 4,00 C. 0,90 D. 1,80
Đọc tiếp
Khử hoàn toàn một lượng Fe2O3 bằng H2 dư, thu được chất rắn X và m gam H2O. Hòa tan hết X trong dung dịch HCl dư, thu được 1,12 lít khí H2 (đktc). Giá trị của m là
A. 1,35
B. 4,00
C. 0,90
D. 1,80
Đáp án A
Ta có: n(H2) = n( Fe) = 0,05.
BTNT→ Fe2O3 là 0,025 → n(H2O) = 0,025.3 = 0,075 → m = 1,35
Đúng 0
Bình luận (0)
Kim loại M có hóa trị n và m (n; m 1; 2 hoặc 3). Hoà tan hoà toàn a gam M bằng dd HCl dư, thu được muối MCln và V lít H2 (đktc). Mặt khác hoà tan hoàn toàn a gam M bằng dd HNO3 loãng, thu được muối M(NO3)m, H2O và cũng V lít khí NO duy nhất (đktc).a/ Viết PTHH của 2 phản ứng trên.b/ So sánh n và m.c/ Hỏi M là kim loại nào? Biết rằng khối lượng muối nitrat tạo thành gấp 1,905 lần khối lượng muối clorua.
Đọc tiếp
Kim loại M có hóa trị n và m (n; m = 1; 2 hoặc 3). Hoà tan hoà toàn a gam M bằng dd HCl dư, thu được muối MCln và V lít H2 (đktc). Mặt khác hoà tan hoàn toàn a gam M bằng dd HNO3 loãng, thu được muối M(NO3)m, H2O và cũng V lít khí NO duy nhất (đktc).
a/ Viết PTHH của 2 phản ứng trên.
b/ So sánh n và m.
c/ Hỏi M là kim loại nào? Biết rằng khối lượng muối nitrat tạo thành gấp 1,905 lần khối lượng muối clorua.
a)Gọi hóa trị của M trong muối clorua là n
Gọi hóa trị của M trong muối nitrat là m
2M + 2nHCl -----> 2MCln + nH2
_1___________________\(\dfrac{n}{2}\)
3M + 4mHNO3 -----> 3M(NO3)m + mNO + 2mH2O
_1_________________________\(\dfrac{m}{3}\)_
Ta có: VH2 = VNO => nH2 = nNO
\(\dfrac{m}{3}=\dfrac{n}{2}\) --> \(\dfrac{n}{m}=\dfrac{2}{3}\) => n = 2; m = 3
Vậy hóa trị của M trong muối clorua < hóa trị của M trong muối nitrat
b,
mM(NO3)m = 1,905m.MCln
M + 62m = 1,905x(M + 35,5n)
<=> 0,905M + 67,6275n = 62m
<=> M = \(\dfrac{62m-67,6275n}{0,905}\)
Thay n = 2; m = 3 vào ta được
M = 56 (Fe)
Đúng 2
Bình luận (0)
a)
2M + 2nHCl --> 2MCln + nH2
3M + 4mHNO3 --> 3M(NO3)m + mNO + 2mH2O
b)
\(n_M=\dfrac{a}{M_M}\left(mol\right)\)
PTHH: 2M + 2nHCl --> 2MCln + nH2
\(\dfrac{a}{M_M}\)--------------------->\(\dfrac{an}{2.M_M}\)
3M + 4mHNO3 --> 3M(NO3)m + mNO + 2mH2O
\(\dfrac{a}{M_M}\)-------------------------->\(\dfrac{am}{3.M_M}\)
=> \(\dfrac{an}{2.M_M}=\dfrac{am}{3.M_M}\)
=> \(\dfrac{n}{m}=\dfrac{2}{3}< 1\)
=> n < m
c)
Có: n = 2; m = 3
Giả sử số mol M là k (mol)PTHH: M + 2HCl --> MCl2 + H2 k------------->k M + 4HNO3 --> M(NO3)3 + NO + 2H2O k------------------>k=> \(\left\{{}\begin{matrix}m_{MCl_2}=k\left(M_M+71\right)\left(g\right)\\m_{M\left(NO_3\right)_3}=k\left(M_M+186\right)\left(g\right)\end{matrix}\right.\)=> \(\dfrac{M_M+186}{M_M+71}=1,905\)=> MM = 56 (g/mol)=> M là FeKim loại M có hóa trị n và m (n; m 1; 2 hoặc 3). Hoà tan hoà toàn a gam M bằng dd HCl dư, thu được muối MCln và V lít H2 (đktc). Mặt khác hoà tan hoàn toàn a gam M bằng dd HNO3 loãng, thu được muối M(NO3)m, H2O và cũng V lít khí NO duy nhất (đktc).a/ Viết PTHH của 2 phản ứng trên.b/ So sánh n và m.c/ Hỏi M là kim loại nào? Biết rằng khối lượng muối nitrat tạo thành gấp 1,905 lần khối lượng muối clorua.
Đọc tiếp
Kim loại M có hóa trị n và m (n; m = 1; 2 hoặc 3). Hoà tan hoà toàn a gam M bằng dd HCl dư, thu được muối MCln và V lít H2 (đktc). Mặt khác hoà tan hoàn toàn a gam M bằng dd HNO3 loãng, thu được muối M(NO3)m, H2O và cũng V lít khí NO duy nhất (đktc).
a/ Viết PTHH của 2 phản ứng trên.
b/ So sánh n và m.
c/ Hỏi M là kim loại nào? Biết rằng khối lượng muối nitrat tạo thành gấp 1,905 lần khối lượng muối clorua.
a)
2M + 2nHCl --> 2MCln + nH2
3M + 4mHNO3 --> 3M(NO3)m + mNO + 2mH2O
b)
\(n_M=\dfrac{a}{M_M}\left(mol\right)\)
PTHH: 2M + 2nHCl --> 2MCln + nH2
\(\dfrac{a}{M_M}\)------------------->\(\dfrac{an}{2.M_M}\)
3M + 4mHNO3 --> 3M(NO3)m + mNO + 2mH2O
\(\dfrac{a}{M_M}\)---------------------------->\(\dfrac{am}{3.M_M}\)
=> \(\dfrac{an}{2.M_M}=\dfrac{am}{3.M_M}\)
=> \(\dfrac{n}{m}=\dfrac{2}{3}\)
=> n < m
c) Chọn n = 2; m = 3
PTHH: M + 2HCl --> MCl2 + H2
\(\dfrac{a}{M_M}\)--------->\(\dfrac{a}{M_M}\)
M + 4HNO3 --> M(NO3)3 + NO + 2H2O
\(\dfrac{a}{M_M}\)----------->\(\dfrac{a}{M_M}\)
=> \(\left\{{}\begin{matrix}m_{MCl_2}=\dfrac{a}{M_M}\left(M_M+71\right)\\m_{M\left(NO_3\right)_3}=\dfrac{a}{M_M}\left(M_M+186\right)\end{matrix}\right.\)
=> \(\dfrac{M_M+186}{M_M+71}=1,905\)
=> MM = 56 (g/mol)
=> M là Fe
Đúng 6
Bình luận (0)
X gồm Ba và Al. Cho m gam X vào nước dư, sau khi các phản ứng xảy ra hoàn toàn, thu được 8,96 lít khí H2 (đktc). Mặt khác, hòa tan hoàn toàn m gam X bằng dd NaOH, thu được 15,68 lít khí H2 (đktc). Giá trị của m là A. 19,1 B. 29,9 C. 24,5 D. 16,4
Đọc tiếp
X gồm Ba và Al. Cho m gam X vào nước dư, sau khi các phản ứng xảy ra hoàn toàn, thu được 8,96 lít khí H2 (đktc). Mặt khác, hòa tan hoàn toàn m gam X bằng dd NaOH, thu được 15,68 lít khí H2 (đktc). Giá trị của m là
A. 19,1
B. 29,9
C. 24,5
D. 16,4
Đáp án : A
Ba + 2H2O -> Ba(OH)2 + H2
Ba(OH)2 + 2Al + H2O -> Ba(AlO2)2 + 3H2
=> nH2 = 4nBa = 0,4 mol => nBa = 0,1 mol
Vì X +NaOH tạo nH2 = 0,7 mol > 0,4 mol => chứng tỏ Al dư ở thí nghiệm đầu
=> nH2 do Al = nH2 (2) – nH2(1) = 0,3 mol
=> nAl = 2/3 nh2 do Al = 0,2 mol
=> mX = 19,1g
Đúng 0
Bình luận (0)