Đốt cháy 150kg than trong không khí dư sau phản ứng có 224m3 khí CO2 thoát ra. Tính hàm lượng C chứa trong loại than trên.
đốt cháy 1kg than trong khí o2, biết than có 10% tạp chất không cháy tính:
- thể tích oxi(đktc) cần thiết để đốt cháy 1kg than trên
-khối lượng co2(đktc) sinh ra trong phản ứng trên
Cnguyên chất = (100%-10%).1000 = 900 (g)
\(n_C=\dfrac{900}{12}=75\left(mol\right)\)
PTHH: C + O2 ---to→ CO2
Mol: 75 75
\(V_{O_2}=75.22,4=1680\left(l\right)\)
\(m_{CO_2}=75.44=3300\left(g\right)\)
Đốt cháy than đá trong khí Oxi, biết trong than đá chứa 7% tạp chất không cháy, sau phản ứng thu được 25 kg khí Cacbônic thì lượng than đá đem dùng là bao nhiêu? Biết hiệu suất phản ứng là 85%
\(n_{CO_2}=\dfrac{25}{44}\left(kmol\right)\)
PTHH: C + O2 --to--> CO2
\(\dfrac{25}{44}\)<---------------\(\dfrac{25}{44}\)
\(n_C=\dfrac{\dfrac{25}{44}}{85\%}=\dfrac{125}{187}\left(kmol\right)\\ m_{than}=\dfrac{\dfrac{125}{187}.12}{100\%-7\%}=8,625\left(kg\right)\)
Đốt cháy 8,96 lít khí CH4 trong không khí đến khi phản ứng xảy ra hoàn toàn.
a, Tính thể tích khí CO2 thoát ra ở đktc
b, Nếu cho 8,96 lít khí CH4 trên vào bình chứa 8,96 lít khí O2 đktc nung hỗn hợp để phản ứng xảy ra hoàn toàn. Tính thể tích khí CO2 thu được ở đktc
a) \(n_{CH_4}=\dfrac{8,96}{22,4}=0,4\left(mol\right)\)
PTHH: CH4 + 2O2 --to--> CO2 + 2H2O
0,4---------------->0,4
=> \(V_{CO_2}=0,4.22,4=8,96\left(l\right)\)
b) \(n_{O_2}=\dfrac{8,96}{22,4}=0,4\left(mol\right)\)
Xét tỉ lệ \(\dfrac{0,4}{1}>\dfrac{0,4}{2}\) => CH4 dư, O2 hết
PTHH: CH4 + 2O2 --to--> CO2 + 2H2O
0,4-------->0,2
=> \(V_{CO_2}=0,2.22,4=4,48\left(l\right)\)
Đốt cháy 1 tấn than trong khí oxygen, biết trong than có chứa 90% Carbon, biết hiệu suất đạt 80%
a. Lập PTHH của phản ứng
b. Tính khối lượng CO2 sinh ra
\(m_C=1000\cdot90\%=900\left(kg\right)\)
\(n_C=\dfrac{900}{12}=75\left(kmol\right)\)
\(C+O_2\underrightarrow{^{^{t^o}}}CO_2\)
\(75............75\)
\(m_{CO_2}=75\cdot44=3300\left(kg\right)\)
\(m_{CO_2\left(tt\right)}=3300\cdot80\%=2640\left(kg\right)=2.64\left(\text{tấn}\right)\)
Đốt một mẫu than chì chứa tạp chất lưu huỳnh trong oxi. Cho hỗn hợp khí thoát ra tác dụng với lượng dư dung dịch brom, thấy có 0,32 g brom đã phản ứng. Cho khí thoát ra khỏi dung dịch brom tác dụng với lượng dư nước vôi trong, thu được 10,00 g kết tủa.
1. Viết phương trình hoá học của các phản ứng xảy ra.
2. Xác định phần trăm khối lượng của cacbon trong mẫu than chì.
Đốt cháy 1 kg than trong khí oxi, biết trong than có 5% tạp chất không cháy. Tính thể tích khí cacbonic (đktc) sinh ra trong phản ứng.
Lượng than nguyên chất:
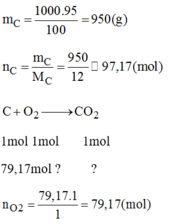
n C O 2 = n O 2 = 79,17(mol) → V C O 2 = V O 2 = 1773,4(l)
Đốt cháy 1 kg than trong khí oxi , biết trong than có 5 % tạp chất ko cháy.
a) Tính thể tích khí oxi (dktc) cần thiết để đốt cháy 1 kg than trên?
b) Tính thể tich khí cacbonic (dktc) sinh ra trong phản ứng ?
a)
n C = (1000 - 1000.5%)/12 = 475/6 mol
C + O2 --to--> CO2
n O2 = n C = 475/6 mol
=> V O2 = 22,4 . 475/6 = 1773,33(lít)
b) V CO2 = V O2 = 1773,33(lít)
cho 14,3 gam hỗn hợp X gồm 3 kim loại Cu , Al , Fe vào dung dịch HCl dư sau phản ứng thấy có 6,72 lít khí thoát ra ở đktc . đốt cháy hoàn toàn 0,6 mol hỗn hợp X thấy có 44,8 lít không khí đktc tham gia phản ứng tính % khối lượng các kim loại có trong X
TN1: Gọi (nCu, nAl, nFe) = (a,b,c)
=> 64a + 27b + 56c = 14,3 (1)
\(n_{H_2}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\)
PTHH: 2Al + 6HCl --> 2AlCl3 + 3H2
b----------------------->1,5b
Fe + 2HCl --> FeCl2 + H2
c----------------------->c
=> 1,5b + c = 0,3 (2)
TN2: Gọi (nCu, nAl, nFe) = (ak,bk,ck)
=> ak + bk + ck = 0,6 (3)
\(n_{O_2}=\dfrac{44,8}{22,4}.20\%=0,4\left(mol\right)\)
PTHH: 2Cu + O2 --to--> 2CuO
ak--->0,5ak
4Al + 3O2 --to--> 2Al2O3
bk--->0,75bk
3Fe + 2O2 --to--> Fe3O4
ck-->\(\dfrac{2}{3}ck\)
=> 0,5ak + 0,75bk + \(\dfrac{2}{3}ck\) = 0,4 (4)
(1)(2)(3) => \(\left\{{}\begin{matrix}a=0,05\left(mol\right)\\b=0,1\left(mol\right)\\c=0,15\left(mol\right)\\k=2\end{matrix}\right.\)
=> \(\left\{{}\begin{matrix}\%m_{Cu}=\dfrac{0,05.64}{14,3}.100\%=22,38\%\\\%m_{Al}=\dfrac{0,1.27}{14,3}.100\%=18,88\%\\\%m_{Fe}=\dfrac{0,15.56}{14,3}.100\%=58,74\%\end{matrix}\right.\)
Đốt cháy 10,8g nhôm trong không khí đến khi phản ứng xảy ra hoàn toàn.
a, Tính khối lượng nhôm oxit thu được sau phản ứng
b, Nếu nung 10,8g nhôm trên trong bình chứa 3,36 lít khí oxi đktc đến khi phản ứng xảy ra hoàn toàn. Chất nào dư? Dư bao nhiêu? Tính khối lượng nhôm oxi thu được sau phản ứng?
\(a,PTHH:4Al+3O_2\underrightarrow{t^o}2Al_2O_3\\ n_{Al}=\dfrac{m}{M}=\dfrac{10,8}{27}=0,4\left(mol\right)\\ Theo.PTHH:n_{Al_2O_3}=\dfrac{1}{2}.n_{Al}=\dfrac{1}{2}.0,4=0,2\left(mol\right)\\ m_{Al_2O_3}=n.M=0,2.102=20,4\left(g\right)\)
\(b,n_{O_2}=\dfrac{V_{\left(đktc\right)}}{22,4}=\dfrac{3,36}{22,4}=0,15\left(mol\right)\\ Lập.tỉ.lệ:\dfrac{n_{Al}}{4}>\dfrac{n_{O_2}}{3}\Rightarrow Al.dư\\ Theo.PTHH:n_{Al\left(pư\right)}=\dfrac{4}{3}.n_{O_2}=\dfrac{4}{3}.0,2\left(mol\right)\\ n_{Al\left(dư\right)}=n_{Al\left(bđ\right)}-n_{Al\left(pư\right)}=0,4-0,2=0,2\left(mol\right)\\ Theo.PTHH:n_{Al_2O_3}=\dfrac{1}{2}.n_{Al}=\dfrac{1}{2}.0,2=0,1\left(mol\right)\\ m_{Al_2O_3}=n.M=0,1=102=10,2\left(g\right)\)