Hoà tan 3,1 gam Na2O vào trong nước thu được 1000 ml dung dịch NaOH.Nồng độ của dung dịch NAOH thu được là:
(1 Điểm)
0,005M
0,1M
0,05M
0,01M
Hoà tan 4 gam NaOH vào nước để được 400 ml dung dịch. Nồng độ mol của dung dịch thu được là *
\(n_{NaOH}=\dfrac{4}{40}=0,1\left(mol\right)\\ C_{M_{NaOH}}=\dfrac{0,1}{0,4}=0,25\left(M\right)\)
n NaOH= \(\dfrac{4}{40}\)=0,1(mol)
C MnaoH=\(\dfrac{0,1}{0,4}\)=0,25(M)
Hòa tan 3,1 gam N a 2 O vào nước được 2 lít dung dịch. Nồng độ mol của dung dịch thu được là
A. 0,05 M
B. 0,1 M
C. 0,3M
D. 0,4M
Hoà tan hoàn toàn m gam A1C13 vào nước được dung dịch X. Nếu cho 480 ml dung dịch NaOH 1M vào X thì thu được 4a gam kết tủa. Mặt khác, nếu cho 170 ml dung dịch NaOH 3M vào X thì thu được 3a gam kết tủa. Giá trị của m là
A. 14,685.
B. 21,36.
C. 20,025.
D. 16,02.
Đáp án C
nNaOH (1) = 0,48 mol
nNaOH (2) = 0,51 mol
Gọi số mol A13+ trong m gam A1C13 là X
Coi 4a, 3a là số mol của Al(OH)3

Hoà tan hoàn toàn m gam AlCl3 vào nước được dung dịch X. Nếu cho 480 ml dung dịch NaOH 1M vào X thì thu được 4a gam kết tủa. Mặt khác, nếu cho 170 ml dung dịch NaOH 3M vào X thì thu được 3a gam kết tủa. Giá trị của m là
A. 14,685
B. 21,36
C. 20,025
D. 16,02
TH1: Khi cho 0,48 mol NaOH thì chỉ tạo 1 phần kết tủa, khi cho 0,51 mol NaOH thì tạo kết tủa tối đa vào 1 phần bị tan
Trường hợp cho 0,51 mol NaOH
TH2: cả 2 lần đều tạo kết tủa tối đa và hòa tan 1 phần
Chênh lệch số mol kết tủa ở 2 trường hợp:
4
a
78
-
3
a
78
=
0
,
51
-
0
,
48
=
⇒
a
78
=
0
,
03
Trường hợp cho 0,48 mol NaOH
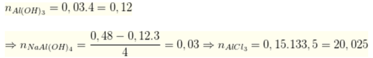
=>Đáp án C
Hoà tan hết m gam Al 2 SO 4 3 vào nước được dung dịch X. Cho 360 ml dung dịch NaOH 1M vào X, thu được 2a gam kết tủa (TN1). Mặc khác, nếu cho 400 ml dung dịch NaOH 1M vào X, thu được a gam kết tủa (TN2). Các phản ứng xảy ra hoàn toàn, giá trị của m là:
A. 18,81
B. 15,39
C. 20,52
D. 19,665
Đáp án A
Từ giả thiết suy ra : Ở TN2 đã có hiện tượng hòa tan kết tủa. Còn ở TN1 thì có thể có hiện tượng hòa tan kết tủa hoặc chưa. Ta đặt :
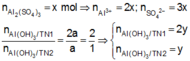
● Nếu cả TN1 và TN2 đều có hiện tượng hòa tan kết tủa, áp dụng bảo toàn điện tích cho các dung dịch sau phản ứng, ta có :
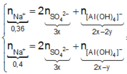
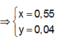
![]() thỏa mãn
thỏa mãn
Suy ra : ![]()
● Nếu TN1 chưa có hiện tượng hòa tan kết tủa, áp dụng bảo toàn điện tích cho các dung dịch sau phản ứng, ta có :
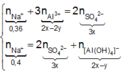
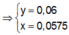
![]() (loại)
(loại)
a. Hòa tan 3,1 gam Na2O vào 50 gam nước. Tính C% của dung dịch thu được?
b. Hòa tan hoàn toàn 4,6 gam Na vào 95,6 gam nước. Tính C% của dung dịch thu được ?
a, \(Na_2O+H_2O\rightarrow2NaOH\)
Ta có: \(n_{Na_2O}=\dfrac{3,1}{62}=0,05\left(mol\right)\)
Theo PT: \(n_{NaOH}=2n_{Na_2O}=0,1\left(mol\right)\)
m dd sau pư = 3,1 + 50 = 53,1 (g)
\(\Rightarrow C\%_{NaOH}=\dfrac{0,1.40}{53,1}.100\%\approx7,53\%\)
b, \(2Na+2H_2O\rightarrow2NaOH+H_2\)
Ta có: \(n_{Na}=\dfrac{4,6}{23}=0,2\left(mol\right)\)
Theo PT: \(\left\{{}\begin{matrix}n_{NaOH}=n_{Na}=0,2\left(mol\right)\\n_{H_2}=\dfrac{1}{2}n_{Na}=0,1\left(mol\right)\end{matrix}\right.\)
Ta có: m dd sau pư = 4,6 + 95,6 - 0,1.2 = 100 (g)
\(\Rightarrow C\%_{NaOH}=\dfrac{0,2.40}{100}.100\%=8\%\)
hoà tan hoàn toàn 11,2 gam KOH vào nước thu được 150 ml dung dịch .nồng độ mol của dung dịch thu được là bao nhiêu?
$n_{KOH} = \dfrac{11,2}{56} = 0,2(mol)$
$C_{M_{KOH}} = \dfrac{0,2}{0,15} = 1,33M$
Hoà tan hết m gam Al2(SO4)3 vào nước được dd A. Cho 300 ml dung dịch NaOH 1M vào A, thu được a gam kết tủa. Mặc khác, nếu cho 400 ml dung dịch NaOH 1M vào A, cũng thu được a gam kết tủa. Giá trị của m là
A. 21.375
B. 42.75
C. 17.1
D. 22.8
Bài 3.
a. Hòa tan hết 16 gamCuSO4 vào 184 gam nước thu được dung dịch CuSO4. Tính nồng độ % của dung dịch CuSO4 ?
b. Hòa tan hết 20 gam NaOH vào nước thu được 4000 ml dung dịch NaOH. Tính nồng độ mol của dung dịch NaOH ?
a)
C% CuSO4 = 16/(16 + 184) .100% = 8%
b)
n NaOH = 20/40 = 0,5(mol)
CM NaOH = 0,5/4 = 0,125M
\(a.\)
\(m_{dd_{CuSO_4\:}}=16+184=200\left(g\right)\)
\(C\%_{CuSO_4}=\dfrac{16}{200}\cdot100\%=8\%\)
\(b.\)
\(n_{NaOH}=\dfrac{20}{40}=0.5\left(mol\right)\)
\(C_{M_{NaOH}}=\dfrac{0.5}{4}=0.125\left(M\right)\)
a) \(m_{dmCUSO4}\) = 16+184 = 200g
C% = \(\dfrac{16}{200}\) x 100% =8 %
b) \(n_{NaOH}\) = \(\dfrac{20}{40}\) = 0,5 (Mol)
\(C_M\) = \(\dfrac{0.5}{4}\) = 0,125 (M) Vì 4000ml= 4l