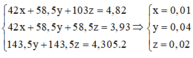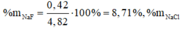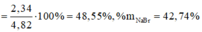hỗn hợp gồm NaCl, NaBr , trong đó NaBr chiếm 10% về khối lượng. Hòa tan hỗn hợp vào nước rồi cho khí clo lội qua dd cho đến dư. Làm bay hơi dd cho đến khi thu được muối khan. Khối lượng hỗn hợp đầu đã thay đổi bao nhiêu% ?

Những câu hỏi liên quan
Hòa tan toàn 13,76 gam hỗn hợp X gồm hai muối NaCl và NaBr vào nước thu được dung hoàn dịch X. Cho khí clo lội từ từ cho đến dư qua dung dịch X thu được dung dịch Y. Làm bay hơi dung dịch Y cho tới khi thu được 12,87 gam muối khan B. Khối lượng của NaCl trong hỗn hợp X là A. 11,7 B. 5,85 C. 8,77 D. 9,3
Đọc tiếp
Hòa tan toàn 13,76 gam hỗn hợp X gồm hai muối NaCl và NaBr vào nước thu được dung hoàn dịch X. Cho khí clo lội từ từ cho đến dư qua dung dịch X thu được dung dịch Y. Làm bay hơi dung dịch Y cho tới khi thu được 12,87 gam muối khan B. Khối lượng của NaCl trong hỗn hợp X là
A. 11,7
B. 5,85
C. 8,77
D. 9,3
Có hỗn hợp gồm NaI và NaBr. Hòa tan hỗn hợp vào nước. Cho Br dư vào dung dịch, làm khô sản phẩm, thì thấy khối lượng của sản phẩm nhỏ hơn khối lượng hỗn hợp ban đầu là m (g). Lại hòa tan sản phẩm vào nước và clo lội qua cho đến dư. Làm bay hơi dung dịch và làm khô chất còn lại người ta thấy khối lượng chất thu được lại nhỏ hơn khối lượng muối phản ứng là m gam. Thành phần phần trăm về khối lượng của NaBr trong hỗn hợp đầu là? A. 3,7%. B. 7,3%. C. 5,7%. D. 20%.
Đọc tiếp
Có hỗn hợp gồm NaI và NaBr. Hòa tan hỗn hợp vào nước. Cho Br dư vào dung dịch, làm khô sản phẩm, thì thấy khối lượng của sản phẩm nhỏ hơn khối lượng hỗn hợp ban đầu là m (g). Lại hòa tan sản phẩm vào nước và clo lội qua cho đến dư. Làm bay hơi dung dịch và làm khô chất còn lại người ta thấy khối lượng chất thu được lại nhỏ hơn khối lượng muối phản ứng là m gam. Thành phần phần trăm về khối lượng của NaBr trong hỗn hợp đầu là?
A. 3,7%.
B. 7,3%.
C. 5,7%.
D. 20%.
Gọi a, b lần lượt là số mol của NaI và NaBr ban đầu, ta có : Sơ đồ phản ứng:
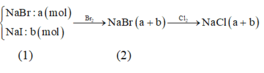

Đáp án A
Đúng 0
Bình luận (0)
Hòa tan 42,6g hh muối NaCl, NaBr vào nước thu được 200g dd A. Cho nước Clo tác dụng vừa đủ với dd A. Sau phản ứng làm bay hơi dd thu được thì khối lượng muối khan giảm 13,35g so với ban đầu. Tính thành phần % theo khối lượng mỗi muối trong hỗn hợp ban đầu và C% dd A.
\(2NaBr+Cl_2\rightarrow2NaCl+Br_2\left(1\right)\\ m_{giảm}=m_{Br_2}-m_{Cl_2}\\ \Leftrightarrow n_{NaCl\left(1\right)}=n_{NaBr\left(1\right)}=\dfrac{13,35}{160-71}=0,15\left(mol\right)\\ \Rightarrow\%m_{NaBr}=\dfrac{103.0,15}{42,6}.100\approx36,268\%\\ \Rightarrow\%m_{NaCl}\approx63,732\%\)
Đúng 1
Bình luận (0)
Bổ sung:
\(C\%_{ddNaBr\left(trongA\right)}=\dfrac{0,15.103}{200}.100=7,725\%\\ C\%_{ddNaCl\left(trongA\right)}=\dfrac{42,6-0,15.103}{200}.100=13,575\%\)
Đúng 1
Bình luận (0)
Giúp emHòa tan hỗn hợp gồm NaBr và NaI vào nước được dung dịch A. Cho brom dư vào dung dịch khuấy kĩ cho phản ứng xong, cô cạn dung dịch thu được chất rắn khan có khối lượng giảm m gam so với hỗ hợp bạn đầu. Hòa tan chất rắn vào nước, sau đó dẫn khí clo dư đi qua. Lại làm bay hơi nước thấy khối lượng chất rắn khan thu được lại giảm m gam nữa so với hỗn hợp ban đầu. Tính phần trăm khối lượng của NaBr trong hỗn hợp ban đầu
Đọc tiếp
Giúp em
Hòa tan hỗn hợp gồm NaBr và NaI vào nước được dung dịch A. Cho brom dư vào dung dịch khuấy kĩ cho phản ứng xong, cô cạn dung dịch thu được chất rắn khan có khối lượng giảm m gam so với hỗ hợp bạn đầu. Hòa tan chất rắn vào nước, sau đó dẫn khí clo dư đi qua. Lại làm bay hơi nước thấy khối lượng chất rắn khan thu được lại giảm m gam nữa so với hỗn hợp ban đầu. Tính phần trăm khối lượng của NaBr trong hỗn hợp ban đầu
NaBr xmol NaI ymol+Br2
2NaI+Br2=>2NaBr +I2
=>y=m/(127-80)=m/47 mol
NaBr (x+y )mol +Cl2=>NaCl+Cl2
=>x+y=m/(80-35.5)=m/44.5=>x=5m/4183
=>mNaBr=515m/4183 mNaI=150m/47 =>%NaBr=3.71%
Đúng 0
Bình luận (1)
NaBr xmol NaI ymol+Br2
2NaI+Br2=>2NaBr +I2
=>y=m/(127-80)=m/47 mol
NaBr (x+y )mol +Cl2=>NaCl+Cl2
=>x+y=m/(80-35.5)=m/44.5=>x=5m/4183
=>mNaBr=515m/4183 mNaI=150m/47 =>%NaBr=3.71%
Đúng 0
Bình luận (1)
Một hỗn hợp X gồm NaCl và NaBr chiếm 10% về khối lượng. Hòa tan hoàn toàn hỗn hợp vào nước rồi dẫn từ từ khí clo từ từ đến dư qua dung dịch. Làm bay hơi dung dịch thu được muối khan Y. Tính tỷ lệ giữa khối lượng của X với Y.
Hòa tan 37,125 gam hỗn hợp các muối NaCl và NaI vào nước. Cho vừa đủ khí clo đi qua dd rồi cô cạn. Nung chất rắn thu được cho đến khi màu tím bay ra hết. Bã rắn còn lại sau khi nung có khối lượng 23,4gam. % khối lượng mỗi muối trong hỗn hợp ban đầu là:
A. 39,4% và 60,6%. B. 30% và 70%
C. 40,4% và 59,6% D. 60,4% và 39,6%
Gọi số mol NaCl, NaI là a, b (mol)
=> 58,5a + 150b = 37,125 (1)
PTHH: 2NaI + Cl2 --> 2NaCl + I2
b------------>b
=> nNaCl(sau pư) = a + b = \(\dfrac{23,4}{58,5}=0,4\left(mol\right)\) (2)
(1)(2) => a = 0,25 (mol); b = 0,15 (mol)
=> \(\left\{{}\begin{matrix}\%m_{NaCl}=\dfrac{58,5.0,25}{37,125}.100\%=38,4\%\\\%m_{NaI}=\dfrac{0,15.150}{37,125}.100\%=60,6\%\end{matrix}\right.\)
=> A
Đúng 4
Bình luận (0)
Gọi \(\left\{{}\begin{matrix}n_{NaCl}=x\left(mol\right)\\n_{NaI}=y\left(mol\right)\end{matrix}\right.\)\(\Rightarrow58,5x+150y=37,125\left(1\right)\)
\(n_{NaCl}=\dfrac{23,4}{58,5}=0,4mol\)
\(\Rightarrow x+y=0,4\left(2\right)\)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}x=0,25mol\\y=0,15mol\end{matrix}\right.\)
\(\%m_{NaCl}=\dfrac{0,25\cdot58,5}{37,125}\cdot100\%=39,4\%\)
\(\%m_{NaI}=100\%-39,4\%=60,6\%\)
Chọn A
Đúng 4
Bình luận (0)
có một hh gồm NaCl và NabBr trong đó NaBr chiếm 10% khối lượng. Hòa tan hh vào nước rồi cho khí clo lội qua đến dư. Làm bay hơi dd thì thu được muối khan, hỏi khối lượng hh đã thay đổi như thế nào.
Coi mhh=100g
⇒mNaBr=10.mNaCL=90(g)
Cl2+2NaBr→2NaCl+Br2
\(\frac{10}{103}\rightarrow\frac{10}{103}\rightarrow\frac{5}{103}\)
⇒mNaCl tạo thành =\(\frac{10}{103}\).58,5=5,68(g)
Có: mBr2 sau phản ứng = 7,767
⇒ m sau phản ứng =90+5,68+7,767=103,45(g)
Vậy sau phản ứng m tăng lên 3,45g và tăng 3,45% so với ban đầu
Một hỗn hợp X gồm ba muối NaF, NaCl, NaBr nặng 4,82 gam. Hòa tan hoàn toàn X trong nước được dung dịch A. Sục khí clo dư vào dung dịch A rồi cô cạn hoàn toàn dung dịch sau phản ứng thu được 3,93 gam muối khan. Lấy một nửa lượng muối khan này hòa tan vào nước rồi cho phản ứng với dung dịch AgNO3 dư thì thu được 4,305 gam kết tủa Z. Tính phần trăm khối lượng mỗi muối trong hỗn hợp ban đầu. A. 14,29% NaF, 57,14% NaCl, 28,57% NaB B. 57,14% NaF, 14,29% NaCl, 28,57% NaBr C. 8,71% NaF, 48,55% NaCl, 4...
Đọc tiếp
Một hỗn hợp X gồm ba muối NaF, NaCl, NaBr nặng 4,82 gam. Hòa tan hoàn toàn X trong nước được dung dịch A. Sục khí clo dư vào dung dịch A rồi cô cạn hoàn toàn dung dịch sau phản ứng thu được 3,93 gam muối khan. Lấy một nửa lượng muối khan này hòa tan vào nước rồi cho phản ứng với dung dịch AgNO3 dư thì thu được 4,305 gam kết tủa Z. Tính phần trăm khối lượng mỗi muối trong hỗn hợp ban đầu.
A. 14,29% NaF, 57,14% NaCl, 28,57% NaB
B. 57,14% NaF, 14,29% NaCl, 28,57% NaBr
C. 8,71% NaF, 48,55% NaCl, 42,74% NaBr
D. 48,55% NaF, 42,74% NaCl, 8,71% NaBr
Hòa tan toàn 13,76 gam hỗn hợp X gồm hai muối NaCl và NaBr vào nước thu được dung
hoàn dịch X. Cho khí clo lội từ từ cho đến dư qua dung dịch X thu được dung dịch Y. Làm bay
hơi dung dịch Y cho tới khi thu được 12,87 gam muối khan B. Khối lượng của NaCl trong hỗn
hợp X là bao nhiêu
help me
#mã mã #