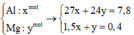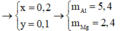Hòa tan 7,8 gam hỗn hợp gồm Al, Mg bằng dd HCl dư. Sau phản ứng khối lượng dd axit tăng thêm 7 gam.
Xác định khối lượng mỗi kim loại trong hh ban đầu.

Những câu hỏi liên quan
Hoà tan 7,8 gam hỗn hợp gồm Al và Mg bằng dung dịch HCl dư. Sau phản ứng khối lượng dung dịch axit tăng thêm 7 gam. Khối lượng Al và Mg trong hỗn hợp ban đầu là:
A. 1,2 gam và 6,6 gam
B. 5,4 gam và 2,4 gam
C. 1,7 gam và 3,1 gam
D. 2,7 gam và 5,1 gam
Hoà tan 7,8 gam hỗn hợp gồm Al và Mg bằng dung dịch HCl dư. Sau phản ứng khối lượng dung dịch axit tăng thêm 7 gam. Khối lượng Al và Mg trong hỗn hợp ban đầu là A. 1,2 gam và 6,6 gam B. 5,4 gam và 2,4 gam C. 1,7 gam và 3,1 gam D. 2,7 gam và 5,1 gam
Đọc tiếp
Hoà tan 7,8 gam hỗn hợp gồm Al và Mg bằng dung dịch HCl dư. Sau phản ứng khối lượng dung dịch axit tăng thêm 7 gam. Khối lượng Al và Mg trong hỗn hợp ban đầu là
A. 1,2 gam và 6,6 gam
B. 5,4 gam và 2,4 gam
C. 1,7 gam và 3,1 gam
D. 2,7 gam và 5,1 gam
Hoà tan 7,8 gam hỗn hợp gồm Al và Mg bằng dung dịch HCl dư. Sau phản ứng khối lượng dung dịch axit tăng thêm 7 gam. Khối lượng Al và Mg trong hỗn hợp ban đầu là: A. 1,2 gam và 6,6 gam B. 5,4 gam và 2,4 gam C. 1,7 gam và 3,1 gam D. 2,7 gam và 5,1 gam
Đọc tiếp
Hoà tan 7,8 gam hỗn hợp gồm Al và Mg bằng dung dịch HCl dư. Sau phản ứng khối lượng dung dịch axit tăng thêm 7 gam. Khối lượng Al và Mg trong hỗn hợp ban đầu là:
A. 1,2 gam và 6,6 gam
B. 5,4 gam và 2,4 gam
C. 1,7 gam và 3,1 gam
D. 2,7 gam và 5,1 gam
Đáp án B
m dd tăng = mKL – mH2 => lượng H2 sinh ra
Lập hệ 2 phương trình với ẩn là số mol của Al và Mg:
- Phương trình về khối lượng hỗn hợp
- Phương trình bảo toàn e
m dd tăng = mKL – mH2 => mH2 = mKL – m dd tăng = 7,8 – 7 = 0,8 gam => nH2 = 0,4 mol
Khối lượng hỗn hợp là 7,8 gam => 27nAl + 24nMg = 7,8 (1)
Bảo toàn e: 3nAl + 2nMg = 3nH2 = 0,8 (2)
Giải (1) và (2) thu được nAl = 0,2 mol và nMg = 0,1 mol
=> mAl = 5,4 gam và mMg = 2,4 gam
Đúng 0
Bình luận (0)
Hòa tan 7,8 gam hỗn hợp gồm Al và Mg bằng dung dịch HCl dư . Sau phản ứng , thấy khối lượng dung dịch tăng thêm 7 gam
a,Viết phương trình phản ứng xảy ra
b,Tính thành phần % khối lượng mỗi kim loại trong hỗn hợp đầu
a, PT: \(2Al+6HCl\rightarrow2AlCl_3+3H_2\)
\(Mg+2HCl\rightarrow MgCl_2+H_2\)
b, Gọi: \(\left\{{}\begin{matrix}n_{Al}=x\left(mol\right)\\n_{Mg}=y\left(mol\right)\end{matrix}\right.\) ⇒ 27x + 24y = 7,8 (1)
Ta có: m dd tăng = mKL - mH2 ⇒ mH2 = 7,8 - 7 = 0,8 (g)
\(\Rightarrow n_{H_2}=\dfrac{0,8}{2}=0,4\left(mol\right)\)
Theo PT: \(n_{H_2}=\dfrac{3}{2}n_{Al}+n_{Mg}=\dfrac{3}{2}x+y=0,4\left(mol\right)\left(2\right)\)
\(\Rightarrow\left\{{}\begin{matrix}x=0,2\left(mol\right)\\y=0,1\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}\%m_{Al}=\dfrac{0,2.27}{7,8}.100\%\approx69,23\%\\\%m_{Mg}\approx30,77\%\end{matrix}\right.\)
Đúng 1
Bình luận (0)
Bài 3. Cho 7,8 gam hỗn hợp hai kim loại Mg, Al tác dụng với dd H2SO4 loãng dư khi phản ứng kết thúc thấy khối lượng dd tăng thêm 7g.
a/ Tính khối lượng mỗi kim loại có trong hỗn hợp ban đầu.
b/ Tính % về khối lượng mỗi kim loại có trong hỗn hợp ban đầu.
c/ Tính khối lượng muối tạo thành.
\(a,Mg+H_2SO_4\rightarrow MgSO_4+H_2\\ 2Al+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2\\ m_{tăng}=m_{hhMg,Al}-m_{H_2}\\ \Leftrightarrow7=7,8-m_{H_2}\\ \Leftrightarrow m_{H_2}=0,8\left(g\right)\\ \Rightarrow n_{H_2}=\dfrac{0,8}{2}=0,4\left(mol\right)\\ Đặt:a=n_{Al}\left(mol\right);n_{Mg}=b\left(mol\right)\left(a,b>0\right)\\ \Rightarrow\left\{{}\begin{matrix}24b+27a=7,8\\b+1,5a=0,4\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}a=0,2\\b=0,1\end{matrix}\right.\\m_{Mg}=24.0,1=2,4\left(g\right);m_{Al}=0,2.27=5,4\left(g\right)\\ \Rightarrow\%m_{Al}=\dfrac{0,2.27}{7,8}.100\approx69,231\%\\ \Rightarrow\%m_{Mg}\approx30,769\%\\ c,m_{muối}=m_{MgSO_4}+m_{Al_2\left(SO_4\right)_3}=120b+342.0,5a=120.0,1+342.0,5.0,2=46,2\left(g\right)\)
Đúng 2
Bình luận (2)
Hoà tan hoàn toàn 7,8 gam hỗn hợp gồm Mg, Al trong dung dịch HCl dư. Sau phản ứng thấy khối lượng dung dịch tăng thêm 7 gam. Khối lượng của Al có trong hỗn hợp ban đầu là ?
Cho vào 7,8 g đáng lẽ khối lượng dung dịch sẽ tăng 7,8 gam nhưng chỉ tăng 7g chứng tỏ có 0,8 g chất khí thoát ra đó chính là khối lượng H2
Mg+2HCl\(\rightarrow\)MgCl2+H2
2Al+6HCl\(\rightarrow\)2AlCl3+3H2
\(n_{H_2}=\dfrac{0,8}{2}=0,4mol\)
Gọi số mol Mg là x, số mol Al là y.Ta có hệ phương trình:
24x+27y=7,8
x+1,5y=0,4
Giải ra x=0,1, y=0,2
mAl=27x=0,2.27=5,4 gam
Đáp án B
Đúng 2
Bình luận (1)
Hoà tan 7,8 gam hỗn hợp bột Al và Mg trong dung dịch HCl dư. Sau phản ứng khối lượng dung dịch tăng thêm 7,0 gam so với dung dịch HCl ban đầu. Khối lượng Al và Mg trong hỗn hợp đầu là A. 5,8 gam và 3,6 gam B. 1,2 gam và 2,4 gam C. 5,4 gam và 2,4 gam D. 2,7 gam và 1,2 gam
Đọc tiếp
Hoà tan 7,8 gam hỗn hợp bột Al và Mg trong dung dịch HCl dư. Sau phản ứng khối lượng dung dịch tăng thêm 7,0 gam so với dung dịch HCl ban đầu. Khối lượng Al và Mg trong hỗn hợp đầu là
A. 5,8 gam và 3,6 gam
B. 1,2 gam và 2,4 gam
C. 5,4 gam và 2,4 gam
D. 2,7 gam và 1,2 gam
Hòa tan 20,65 gam hỗn hợp kim loại Al, Fe bằng dd axit H2SO4 loãng dư thu được 16,24 lít khí hidro (đktc). Xác định thành phần phần trăm khối lượng của mỗi kim loại trong hỗn hợp, tính khối lượng axit đã phản ứng và khối lượng muối sinh ra
n Al = a(mol) ; n Fe = b(mol)
=> 27a + 56b = 20,65(1)
2Al + 3H2SO4 → Al2(SO4)3 + 3H2
a...........1,5a............0,5a............1.5a..(mol)
Fe + H2SO4 → FeSO4 + H2
b...........b..............b............b......(mol)
=> n H2 = 1,5a + b = 0,725(2)
Từ 1,2 suy ra a = 0,35 ; b = 0,2
Suy ra :
%m Al = 0,35.27/20,65 .100% = 45,76%
%m Fe = 100% -45,76% = 54,24%
m H2SO4 = (1,5a + b).98 = 71,05 gam
m muối = m kim loại + m H2SO4 -m H2 = 20,65 + 71,05 -0,725.2 = 90,25 gam
Đúng 1
Bình luận (0)
Hoà tan 7,8 gam hỗn hợp bột Al và Mg trong dung dịch HCl dư. Sau phản ứng khối lượng dung dịch axit tăng thêm 7,0 gam. Khối lượng nhôm và magie trong hỗn hợp đầu là
A. 4,86 và 2,94.
B. 2,4 và 5,4.
C. 5,4 và 2,4.
D. 2,94 và 4,86.