Cho 1,2g Mg kim loại phản ứng hoàn toàn với m gam đơn chất halogen X² thu được 4,75g hợp chất muối halogenua. Tính m và xác định nguyên tố halogen X.

Những câu hỏi liên quan
cho 144 gam một đơn chất halogen tác dụng vừa đủ với nhóm đun nóng, thu được x gam muối nhôm halogenua. Hòa tan hoàn toàn một nữa khối lượng muối nhóm halogenua ở phản ứng trên vào nước thu được 150ml dung dịch X có nồng độ 16,6879% ( với khối lượng riêng của muối là 3,28 em"). Tìm công thúc đem chất halogen? Giúp e đi ạ
Cho 8,1 gam kim loại Al phản ứng vừa đủ với một đơn chất halogen thu được 40,05 gam muối. Xác định tên halogen
2Al+3X2-->2AlX3
0,3---------------0,3mol
nAl=8,1\27=0,3 mol
=>40,05=0,3.(27+X.3)=>x=35,5 (Cl)
cho 11,2g Fe tác dụng với đơn chất halogen, sau phản ứng thu được 32,5g muối sắt halogenua. Xác định tên gọi của đơn chất halogen.
Gọi tên của đơn chất halogen là X
\(Fe+3X\underrightarrow{t^o}FeX_3\)
ta có :\(\dfrac{56}{11,2}=\dfrac{56+3X}{32,5}\) => X = 35,5
Vậy X là Clo ( Cl )
Đúng 0
Bình luận (2)
nFe = 0,2 mol
Fe + 3M → FeM3
0,2..................0,2
⇒ \(\dfrac{32,5}{56+3M}\) = 0,2
⇔ 32,5 = 11,2 + 0,6M
⇔ 21,3 = 0,6M
⇔ M = 35,5 (Cl)
Vậy M là clo
Đúng 1
Bình luận (1)
Cho 12 gam magie phản ứng với đơn chất halogen vừa đủ thu được 47,5 g muối magie halogenua. Tìm tên của đơn chất halogen.
giúp mình với ạ, mình cảm ơn :3
Gửi
Xem chi tiết
Mg+X2---->MgX2
n Mg=12/24=0,5(mol)
n MgX2=\(\frac{47,5}{24+2X}\left(mol\right)\)
Theo pthh
n Mg=n MgX2
-->\(\frac{47,5}{24+2X}=0,5\Leftrightarrow47,5=12+X\)
-->X=35,5(Cl)
Vậy .......
Cho 4,65 gam hỗn hợp A gồm
M
g
X
2
và
M
g
Y
2
(X, Y là 2 nguyên tố halogen ở 2 chu kỳ kế tiếp,
M
X
M
Y
) phản ứng hoàn toàn với dd
A
g
N
O
3
dư, thu được 11,05 gam kết tủa. Xác định hai nguyên tố X, Y và tính khối lượng mỗi muối trong hỗn hợp A?
Đọc tiếp
Cho 4,65 gam hỗn hợp A gồm M g X 2 và M g Y 2 (X, Y là 2 nguyên tố halogen ở 2 chu kỳ kế tiếp, M X < M Y ) phản ứng hoàn toàn với dd A g N O 3 dư, thu được 11,05 gam kết tủa. Xác định hai nguyên tố X, Y và tính khối lượng mỗi muối trong hỗn hợp A?
Cho một lượng đơn chất halogen tác dụng với Mg thu được 19g magie halogenua. Cũng lượng đơn chất halogen đó tác dụng với nhôm tạo 17,8g nhôm halogen. Xác định tên và khối lượng đơn chất halogen nói trên.
a) Phương trình hóa học của phản ứng: Gọi X là kí hiệu nguyên tử khối của halogen.
Mg + X2 → MgX2
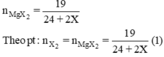
2Al + 3X2 → 2AlX3.
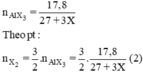
Cho (1) = (2). Giải ta rút ra X = 35,5 (Cl)
b) Thay X = 35,5 vào (1) ⇒ nCl2 = 0,2 mol ⇒ mCl2 = 14,2g.
Đúng 0
Bình luận (1)
Cho 6,56 gam hỗn hợp A gồm NaX và NaY (X, Y là 2 nguyên tố halogen ở 2 chu kỳ kế tiếp, M X < M Y ) phản ứng hoàn toàn và vừa đủ với 50 ml dd A g N O 3 1 M, thu được kết tủa. Xác định hai nguyên tố X, Y.
Cho 4,26g đơn chất Halogen X2 tác dụng vừa đủ với kim loại R thuộc nhóm IIA thu được 6,66g muối Halogen . Xác định X và R ?
Xem chi tiết
Bảo toàn khối lượng ta có: $m_{R}=2,4(g)$$R+X_2\rightarrow RX_2$
Ta có: $\frac{2,4}{R}=\frac{4,26}{2X}$
Lập bảng biện luận thông qua halogen tìm được X và R lần lượt là Cl và Ca
Đúng 1
Bình luận (3)
nX2 = nRX2 ⇒ \(\dfrac{4,26}{2X}=\dfrac{6,66}{R+2X}\)
⇒ 4,26R + 8,52X = 13.32X
⇒ 4,26R = 4,8X
⇒ \(\dfrac{X}{R}=\dfrac{80}{71}=\dfrac{40}{35,5}\)
⇒ X là Ca còn R là Cl
Đúng 0
Bình luận (0)
Cho 0,24 gam kim loại Mg tác dụng vừa đủ với khí Halogen X2,sau phản ứng thu được 1,84 gam muối khan.Xác định công thức và tên của muối Halogen thu được?
Xem chi tiết
PTHH: \(Mg+X_2\rightarrow MgX_2\)
Ta có: \(\dfrac{0,24}{24}=\dfrac{1,84}{24+2\cdot M_X}\) \(\Rightarrow M_X=80\)
Vậy Halogen cần tìm là Brom
Muối thu được là Magie Bromua
Đúng 2
Bình luận (0)























