Điện phân nóng chảy một muối 11,7 g halogenua NaX. người ta thu được 2,24 lít khí (đktc)
a. xác định nguyên tố X
b. tính thể tích khí HX thu được khi người ta cho X tác dụng với 4,48 lít khí H2 ( đktc )
c. tính tỉ lệ % các khí sau phản ứng
Câu 13: Cho 24g CuO tác dụng với khí H2 khi đun nóng. Thể tích khí H2 (đktc) cho phản ứng trên là:
A. 11,2 lít B. 13,44 lít C. 6,72 lít D. 2,24 lít
Câu 14: Cho khí H2 tác dụng với Fe2O3 đun nóng thu được 5,6g Fe
Khối lượng Fe2O3 đã tham gia phản ứng là:
A. 12g B.13g C.15g D.16g
điện phân nóng chảy một muối 11,7g NaX người ta thu được 2,24 lít khí (đktc)
a) Xác định nguyên tố X?
b) tính thể tích khí HX thu đc khi người ta cho X tác dụng với 4,48 lít H2 ở đktc
c tính tỷ lệ % các khí sau phản ứng
\(2NaX\rightarrow2Na+X_2\)
46+2X 1
11,7 0,1
=> (46+2X)0,1=11,7
<=>4,6+0,2X=11,7
<=> 0,2X=7,1
<=> X=35,5(Cl)
b, \(Cl_2+H_2\rightarrow2HCl\)
1 1 2
0,1 0,2
0,1 0,1 0,2
0 0,1 0
\(n_{H_2dư}=0,1\left(mol\right)\)
Cho 4,48 lít khí SO2 tác dụng với 2,24 lít khí O2. Thêm xúc tác và nung nóng cho phản ứng xảy ra. Sau khi phản ứng kết thúc, ta thu được 5,6 lít hỗn hợp khí gồm SO2, O2, SO3. Tính thể tích mỗi khí có trong hỗn hợp sau phản ứng và tính hiệu suất của phản ứng. Biết các khí đo ở đktc
Gọi hiệu suất phản ứng là a
$2SO_2 + O_2 \xrightarrow{t^o,V_2O_5} 2SO_3$
Ta thấy :
V SO2 / 2 = V O2 nên hiệu suất tính theo số mol của SO2 hoặc O2
V SO2 phản ứng = 4,48a(lít)
V O2 phản ứng = 2,24a(lít)
V SO3 = V SO2 pư = 4,48a(lít)
Sau phản ứng, khí gồm :
SO2 : 4,48 - 4,48a(lít)
O2 : 2,24 - 2,24a(lít)
SO3 : 4,48a(lít)
Suy ra :
4,48 - 4,48a + 2,24 - 2,24a + 4,48a = 5,6
=> a = 0,5 = 50%
Hỗn hợp khí gồm :
SO2 : 4,48 -4,48.0,5 = 2,24 lít
O2 : 2,24 - 2,24.0,5 = 1,12 lít
SO3 : 4,48.0,5 = 2,24 lít
Điện phân nóng cháy một muối 11,7g halogenua Nã người ta thu đc 2,24 lít khí ( đktc)
a) xác định nguyên tố X
b) tính thể tích khí HK thu được khi người ta cho X tác dụng với 4,48 lí H2 ở đktc
c) tính tỷ lệ % các khí sau phản ứng
Người ta dùng H2 (dư) tác dụng hết với x gam Fe2O3 nung nóng thu được y gam Fe. Cho lượng sắt này tác dụng với dung dịch H2SO4 loãng dư thì thu được 6,72 lít khí H2 (đktc). Tính giá trị x và y.
PTHH: \(Fe_2O_3+3H_2\underrightarrow{t^o}2Fe+3H_2O\)
\(Fe+H_2SO_4\rightarrow FeSO_4+H_2\uparrow\)
Ta có: \(n_{H_2}=\dfrac{6,72}{22,4}=0,3\left(mol\right)=n_{Fe}\)
\(\Rightarrow n_{Fe_2O_3}=0,15\left(mol\right)\) \(\Rightarrow m_{Fe_2O_3}=x=0,15\cdot160=24\left(g\right)\)
Một hỗn hợp X gồm 1 ankan A và 1 ankin B có cùng số nguyên tử cacbon. Trộn X với H2 (vừa đủ) để được hỗn hợp Y. Khi cho Y qua Pt, xúc tác thì thu được khí Z có tỉ khối đối với CO2 bằng 1 (phản ứng cộng H2 hoàn toàn). Biết rằng V X = 6 , 72 lít và V H 2 = 4 , 48 lít . Xác định công thức phân tử và số mol của A, B trong hỗn hợp X. Các thể tích khí được đo ở đktc.
A. C3H8, C3H4, 0,2 mol C3H8, 0,1 mol C3H4
B. C3H8, C3H4, 0,1 mol C3H8, 0,2 mol C3H4
C. C2H6, C2H2, 0,1 mol C2H6, 0,2 mol C2H2
D. C2H6, C2H2, 0,2 mol C2H6, 0,2 mol C2H2
Chọn A
C3H8, C3H4, 0,2 mol C3H8, 0,1 mol C3H4
Một hỗn hợp X gồm 1 ankan A và 1 ankin B có cùng số nguyên tử cacbon. Trộn X với H2 (vừa đủ) để được hỗn hợp Y. Khi cho Y qua Pt xúc tác thì thu được khí Z có tỉ khối đối với CO2 bằng 1 (phản ứng cộng H2 hoàn toàn). Biết rằng VX =6,72 lít và VH = 4,48 lít. Xác định công thức phân tử và số mol của A, B trong hỗn hợp X. Các thể tích khí được đo ở đktc
A. 0,2 mol C3H8 và 0,1 mol C3H4
B. 0,2 mol C2H6 và 0,2 mol C2H2
C. 0,1 mol C2H6 và 0,2 mol C2H2
D. 0,1 mol C3H8 và 0,2 mol C3H4
Có phản ứng: ![]()
Vì lượng H2 vừa đủ để phản ứng và phản ứng cộng xảy ra hoàn toàn nên Z thu được chỉ chứa ankan. Mặt khác A và B có cùng số nguyên tử C nên trong Z chỉ chứa ankan ![]() .
.
Do đó ![]()
Suy ra A là C3H8 và B là C3H4.
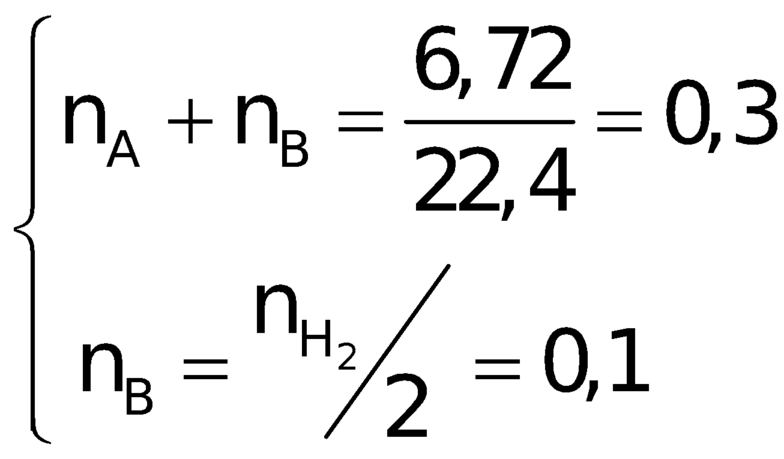
Đáp án A.
Cho sắt tác dụng với dung dịch H2SO4 loãng thu được V lít khí H2 (đktc), dung dịch thu được cho bay hơi thu được tinh thể FeSO4.7H2O có khối lượng là 55,6 gam. Thể tích khí H2(đktc) được giải phóng là :
A. 8,19 lít.
B. 7,33 lít.
C. 4,48 lít.
D. 6,23 lít.
Đáp án C.
Cứ 278 g FeSO4.7H2O có 152 g FeSO4
→ 55,6 g FeSO4.7H2O có x (g) FeSO4
Khối lượng FeSO4 là 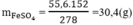
Số mol FeSO4: 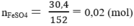
Fe + H2SO4 → FeSO4 + H2
nH2 = nFeSO4 = 0,2 (mol) ⇒ VH2 = 0,2.22,4 = 4,48 (lit)
Đốt cháy sắt trong khí clo, người ta thu được 32,5 gam muối. Thể tích khí clo (đkc) đã tham gia phản ứng là *
67,2 lít.
7,437 lít.
4,48 lít.
2,24 lít.
$2Fe + 3Cl_2 \xrightarrow{t^o} 2FeCl_3$
$n_{FeCl_3} = \dfrac{32,5}{162,5} = 0,2(mol)$
$n_{Cl_2} = \dfrac{3}{2}n_{FeCl_3} = 0,3(mol)$
$V_{Cl_2} = 0,3.22,4 = 6,72(lít)$