Công thức hóa học của nước có trong 0.5 mol nước là bao nhiêu?

Những câu hỏi liên quan
Công thức hóa học của đường là C12H22O11.
a) Có bao nhiêu mol nguyên tử C, H, O trong 1,5 mol đường?
b) Tính khối lượng mol đường.
c) Trong 1 mol đường có bao nhiêu gam các nguyên tố C, H, O.
a) Trong 1 mol phân tử C12H22O11 có 12 mol nguyên tử C, 22 mol nguyên tử H, 11 mol nguyên tử O. Do đó trong 1,5 mol phân tử C12H22O11 có số mol các nguyên tử của nguyên tố là:
nC = 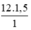 = 18 mol nguyên tử cacbon.
= 18 mol nguyên tử cacbon.
nH = 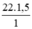 = 33 mol nguyên tử H.
= 33 mol nguyên tử H.
nO = 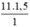 = 16,5 mol nguyên tử O.
= 16,5 mol nguyên tử O.
b) Khối lượng mol đường:
MC12H22O11 =12.MC + 22.MH + 11.MO = 12.12 + 1.22 +16.11= 342 g/mol.
c) Trong 1 mol phân tử C12H22O11 có khối lượng các nguyên tố.
mC = 12 . 12 = 144g.
mH = 1 . 22 = 22g.
mO = 16 . 11 = 176g.
Đúng 1
Bình luận (1)
Phân đạm ure có công thức hóa học là C O N H 2 2 . Hãy xác định: Trong 2 mol phân tử ure có bao nhiêu mol nguyên tử của mỗi nguyên tố.
Trong 2 mol phân tử C O N H 2 2 có:
Nguyên tố C: 2x1 = 2 mol nguyên tử C.
Nguyên tố O: 2x1 = 2 mol nguyên tử O.
Nguyên tố N: 2x2 = 4 mol nguyên tử N.
Nguyên tố H: 2x4 = 8 mol nguyên tử H.
Đúng 0
Bình luận (0)
Bài 5: Công thức hóa học của saccarozơ C12H22O11
a) Có bao nhiêu mol mỗi nguyên tử C, H, O trong 1,5 mol saccarozơ.
b) Trong 1,5 mol saccarozơ có bao nhiêu gam mỗi nguyên tố C, H, O.
\(a,n_C=1,5.12=18(mol)\\n_H=1,5.22=33(mol)\\n_O=1,5.11=16,5(mol)\\ b,m_C=18.12=216(g)\\m_H=33.1=33(g)\\m_O=16,5.16=264(g)\)
Đúng 3
Bình luận (0)
Câu 8. Chất nào là đơn chất trong các chất sau.A. Sắt có công thức hóa học là Fe.B. Sulfur đioxide có công thức hóa học là SO2C. Soda có công thức hóa học là Na2CO3D. Nước vôi trong có công thức hóa học là Ca(OH)2Câu 9. Chất nào là hợp chất trong các chất sau.A. Ozon có công thức hóa học là O3B. Bột nhôm có công thức hóa học là AlC. Khí chlorine có công thức hóa học là ClD. Có 1 phân tử oxygen trong phân tử dinitrogen pentaoxide.
Đọc tiếp
Câu 8. Chất nào là đơn chất trong các chất sau.
A. Sắt có công thức hóa học là Fe.
B. Sulfur đioxide có công thức hóa học là SO2
C. Soda có công thức hóa học là Na2CO3
D. Nước vôi trong có công thức hóa học là Ca(OH)2
Câu 9. Chất nào là hợp chất trong các chất sau.
A. Ozon có công thức hóa học là O3
B. Bột nhôm có công thức hóa học là Al
C. Khí chlorine có công thức hóa học là Cl
D. Có 1 phân tử oxygen trong phân tử dinitrogen pentaoxide.
Câu 8 : A
B C D sai vì được cấu tạo từ hai nguyên tố hóa học trở lên
Câu 9 : D ( được cấu tạo từ hai nguyên tố hóa học là N và O)
Đúng 0
Bình luận (0)
31. Biết công thức hóa học của chất X là NaHCO3. a/ Hỏi có bao nhiêu mol nguyên tử Na, H, C và O trong 1,5 mol chất X? b/ Tính khối lượng của 0,05 mol chất X? c/ Tính khối lượng của từng nguyên tố có trong 0,36 mol chất X? d/ Tính số nguyên tử của từng nguyên tố trong 0,25 mol chất X?
Công thức hóa học của caxniphotphat: Ca3(PO4)2
a, Tính số mol nguyên tử của mỗi nguyên tố có trong 0,25 mol hợp chất trên?
b, Trong hợp chất trên có bao nhiêu gam O?
CÁC HIỀN NHÂN CÍU EM VỚI
Công thức hóa học của caxniphotphat: Ca3(PO4)2
a, Tính số mol nguyên tử của mỗi nguyên tố có trong 0,25 mol hợp chất trên?
=> n Ca=0,25.3=0,75 mol
n P=0,25.2=0,5 mol
n O=0,25.4.2=2 mol
b, Trong hợp chất trên có bao nhiêu gam O?
=> m O=2.16=32g
Đúng 1
Bình luận (0)
Để đốt cháy hết 16 g hợp chất X cần 44,8 lít khí oxi (điều kiện tiêu chuẩn) . Sau khi kết thúc phản ứng chỉ thu được CO2 và hơi nước theo tỉ lệ số mol là 1 : 2 . Xác định công thức hóa học của x biết công thức đơn giản chính là công thức hóa học
Gọi số mol CO2, H2O là a, b
=> 2a = b
\(n_{O_2}=\dfrac{44,8}{22,4}=2\left(mol\right)\)
Theo ĐLBTKL: 44a + 18b = 16 + 2.32 = 80
=> a = 1; b = 2
Bảo toàn C: nC = 1(mol)
Bảo toàn H: nH = 4 (mol)
Xét mC + mH = 1.12 + 4.1 = 16(g)
=> X chỉ chứa C và H
nC : nH = 1 : 4
=> CTPT: CH4
Đúng 4
Bình luận (0)
Công thức hóa học của nước, biết trong phân tử có 2H,1O là:
A. HO.
B. H2O2.
C. H2O.
D. HO2.
Công thức hóa học của nước, biết trong phân tử có 2H,1O là:
A. HO.
B. H2O2.
C. H2O.
D. HO2.
Đúng 0
Bình luận (0)
1) tính khối lượng vôi tôi Ca(OH)2 có thể thu được khi cho 140kg vôi sóng CaO tác dụng với nước. Biết rằng trong vôi sống chứa 10% tạp chất.2) Hãy xách định công thức hóa học của những chất có thành phần như sau ( theo khối lượng ). Biết rằng phân tử mỗi chất chỉ có 1 nguyên tử S. %Cu 40%, %S20% , %O40%3) cho 13g kẽm vào 1 dung dịch chứa 0.5 mol HCl.a) Tính thể tích H2 thu được nếu hiệu suất phản ứng là 90%b) Sau phản ứng còn thừa chất nào? Khối lượng là bao nhiêu?
Đọc tiếp
1) tính khối lượng vôi tôi Ca(OH)2 có thể thu được khi cho 140kg vôi sóng CaO tác dụng với nước. Biết rằng trong vôi sống chứa 10% tạp chất.
2) Hãy xách định công thức hóa học của những chất có thành phần như sau ( theo khối lượng ). Biết rằng phân tử mỗi chất chỉ có 1 nguyên tử S. %Cu= 40%, %S=20% , %O=40%
3) cho 13g kẽm vào 1 dung dịch chứa 0.5 mol HCl.
a) Tính thể tích H2 thu được nếu hiệu suất phản ứng là 90%
b) Sau phản ứng còn thừa chất nào? Khối lượng là bao nhiêu?
3) Zn+2HCl->ZnCl2+H2
a) \(n_{Zn}=\frac{13}{65}=0,2mol\)
Vì: \(\frac{0,2}{1}< \frac{0,5}{2}\)=> Zn hết, HCl dư.
\(n_{H_2}=n_{Zn}=0,2mol\)
\(V_{H_2}=0,2.22,4=4,48l\)
H=90%=> VH2 thu được là:4,032l
b) HCl dư: 0,5-(0,2.2)=0,1mol
mHCl=0,1.36,5=3,65g
Đúng 0
Bình luận (0)
Khối lượng CaO
140-140.10%=126(kg)
CaO + \(H_2\)O \(\rightarrow\)Ca(OH)2
56(g)...................68(g)
126(kg)...............?
Khối lượng Ca(OH)2
\(\frac{126.68}{56}\)=153(kg)
Đúng 0
Bình luận (0)
1)Khối lượng CaO
140-140.10%=126(kg)
CaO + \(H_2\)O \(\rightarrow\)Ca(OH)2
56(g).................74(g)
126(kg)..............?
Khối lương Ca(OH)2
\(\frac{126.74}{56}\)=166,5(kg)
Đúng 0
Bình luận (0)
Xem thêm câu trả lời























