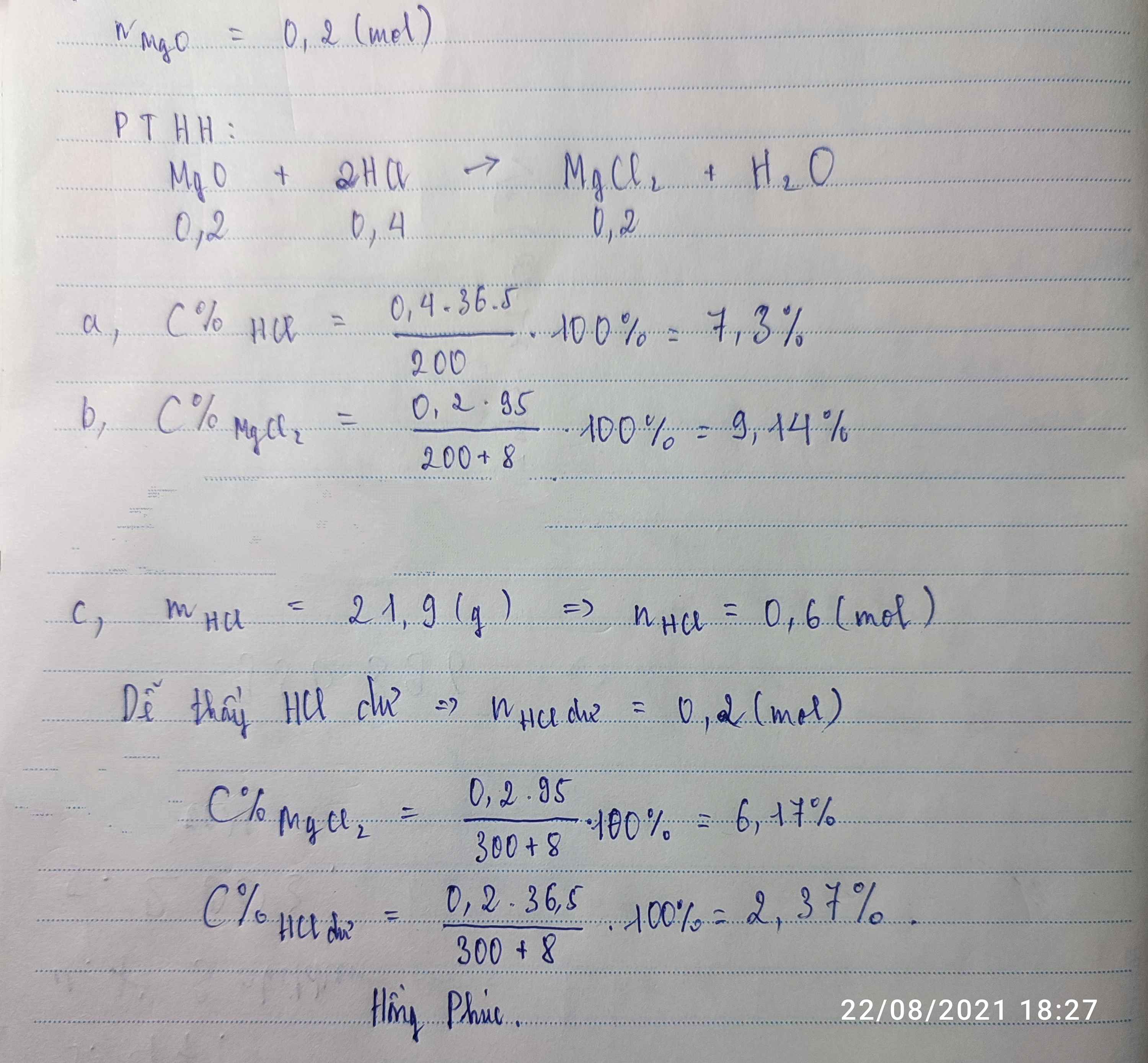Tính số hạt nguyên tử của MgO có trong 300g MgO

Những câu hỏi liên quan
a) Trong 24g MgO có bao nhiêu mol, bao nhiêu phân tử MgO? Phải lấy bao nhiêu gam HCl để có số phân tử HCl nhiều gấp 2 lần số phân tử MgO?
b) Một mẫu kim loại sắt có số nguyên tử nhiều gấp 5 lần số nguyên tử của 12,8 g kim loại đồng. Tìm khối lượng của mẫu kim loại sắt trên.
c) Cần phải lấy bao nhiêu gam NaOH để có số phân tử gấp đôi số phân tử của 7,3g HCl?
a, n\(_{MgO}\)=\(\dfrac{24}{40}\)=0,6 mol (đpcm)
=>ptử MgO = 0,6.6.10\(^{23}\)=3,6.10\(^{23}\)(đpcm)
+ ptu HCl = 2.3,6.10\(^{23}\)=7,6.10\(^{23}\)
n\(_{_{HCL}}\)=\(\dfrac{7,6.10^{23}}{6.10^{23}}\) \(\approx1,27\)mol
m\(_{HCl}\)=1,27.36,5\(\approx\)46,4g( dpcm)
Đúng 0
Bình luận (0)
Hòa tan hoàn toàn 8g MgO vào 200 g dd HCl vừa đủ tạo dd A.a)Tính C% của dd HCl đã dùng. b)Tính C% của dd tạo thành sau phản ứng.c)Nếu đem hòa tan lượng MgO ở trên trong 300g dung dịch HCl 7,3%. Tìm C% của các chất có trong dung dịch A.Hòa tan hoàn toàn 8g MgO vào 200 g dd HCl vừa đủ tạo dd A.a)Tính C% của dd HCl đã dùng. b)Tính C% của dd tạo thành sau phản ứng.c)Nếu đem hòa tan lượng MgO ở trên trong 300g dung dịch HCl 7,3%. Tìm C% của các chất có trong dung dịch A.
Đọc tiếp
Hòa tan hoàn toàn 8g MgO vào 200 g dd HCl vừa đủ tạo dd A.
a)Tính C% của dd HCl đã dùng. b)Tính C% của dd tạo thành sau phản ứng.
c)Nếu đem hòa tan lượng MgO ở trên trong 300g dung dịch HCl 7,3%. Tìm C% của các chất có trong dung dịch A.Hòa tan hoàn toàn 8g MgO vào 200 g dd HCl vừa đủ tạo dd A.
a)Tính C% của dd HCl đã dùng. b)Tính C% của dd tạo thành sau phản ứng.
c)Nếu đem hòa tan lượng MgO ở trên trong 300g dung dịch HCl 7,3%. Tìm C% của các chất có trong dung dịch A.
hòa tan 40g Mgo vào 300g dd H2SO4 98%. Tính nồng độ phần trăm các chất trong dd sau phản ứng
PTHH: \(MgO+H_2SO_4\rightarrow MgSO_4+H_2O\)
Ta có: \(\left\{{}\begin{matrix}n_{MgO}=\dfrac{40}{40}=1\left(mol\right)\\n_{H_2SO_4}=\dfrac{300\cdot98\%}{98}=3\left(mol\right)\end{matrix}\right.\) \(\Rightarrow\) Axit còn dư
\(\Rightarrow\left\{{}\begin{matrix}n_{MgSO_4}=1\left(mol\right)\\n_{H_2SO_4\left(dư\right)}=2\left(mol\right)\end{matrix}\right.\) \(\Rightarrow\left\{{}\begin{matrix}C\%_{MgSO_4}=\dfrac{120}{300+40}\cdot100\%\approx35,3\%\\C\%_{H_2SO_4\left(dư\right)}=\dfrac{2\cdot98}{300+40}\cdot100\%\approx57,65\%\end{matrix}\right.\)
Đúng 2
Bình luận (0)
dẫn một luồng khí H2 nóng đi qua các ống mắc nối tiếp chứa lần lượt các chất sau: MgO, CuO, Fe2O3, BaO. Viết các PTHH xảy ra ở mỗi ống( nếu có)
b. Tính số nguyên tử của mỗi nguyên tố có trong 68,4g Al2(SO4)3
\(CuO+H_2\underrightarrow{^{^{t^0}}}Cu+H_2O\)
\(Fe_2O_3+3H_2\underrightarrow{^{^{t^0}}}2Fe+3H_2O\)
\(b.\)
\(n_{Al_2\left(SO_4\right)_3}=\dfrac{68.4}{342}=0.2\left(mol\right)\)
Số nguyên tử Al :
\(0.2\cdot2\cdot6\cdot10^{23}=2.4\cdot10^{23}\left(pt\right)\)
Số nguyên tử S :
\(0.2\cdot3\cdot6\cdot10^{23}=3.6\cdot10^{23}\left(pt\right)\)
Số nguyên tử O :
\(0.2\cdot12\cdot6\cdot10^{23}=14.4\cdot10^{23}\left(pt\right)\)
Đúng 3
Bình luận (0)
I. Phần trắc nghiệm (3 điểm): Hãy chọn đáp án đúng trong các câu sau:Câu 1. Cho các chất có công thức hóa học sau: O2, Al2O3, N2, Al, H2O, MgO. Số đơn chất làA. 2.B. 3. C. 4.D. 5.Câu 2. Trong nguyên tử, những hạt mang điện làA. Electron, nơtron.B. Proton, nơtron.C. Electron, proton, nơtron.D. Electron, proton.Câu 3. Cho phản ứng: Sắt cháy trong oxi tạo ra oxit sắt từ. Chất tham gia phản ứng làA. sắt.B. oxit sắt từ.C. oxi.D. sắt và oxi.Câu 4. Trong các hiện tượng sau, hiện tượng nào là hiện tượn...
Đọc tiếp
![]()
I. Phần trắc nghiệm (3 điểm): Hãy chọn đáp án đúng trong các câu sau:
Câu 1. Cho các chất có công thức hóa học sau: O2, Al2O3, N2, Al, H2O, MgO. Số đơn chất là
A. 2. | B. 3. | C. 4. | D. 5. |
Câu 2. Trong nguyên tử, những hạt mang điện là
A. Electron, nơtron. | B. Proton, nơtron. |
C. Electron, proton, nơtron. | D. Electron, proton. |
Câu 3. Cho phản ứng: Sắt cháy trong oxi tạo ra oxit sắt từ. Chất tham gia phản ứng là
A. sắt. | B. oxit sắt từ. | C. oxi. | D. sắt và oxi. |
Câu 4. Trong các hiện tượng sau, hiện tượng nào là hiện tượng hóa học?
A. Cô cạn dung dịch muối ăn. | B. Sắt để lâu ngoài không khí ẩm bị gỉ. |
C. Nước hoa bay hơi. | D. Hơi nước ngưng tụ. |
Câu 5. Tỉ khối của khí SO2 so với khí H2 là
A. 32. | B. 16. | C. 64. | D. 8. |
Câu 6. Có PTHH: 4Na + O2 → 2Na2O. Tỉ lệ số nguyên tử, số phân tử trong phương trình hóa học là
A. 1 : 2: 1. | B. 4 :2 : 2. | C. 2: 2 :2. | D. 4: 1: 2. |
Câu 1 : B 3
Câu 2 : D Electroron , proton
Câu 3 : D sắt và oxi
Câu 4 : B sắt để lâu ngoài không khí bị gỉ
Câu 5 : A 32
Câu 6 : D 4 : 1 : 2
Chúc bạn học tốt
Đúng 0
Bình luận (0)
a,hoàn thành PTHH sau và cho biết tỉ lệ số nguyên tử (phân tử) các chất trong phản ứng hóa học sau
- Mg + O2 ---> MgO
- Fe + O2 ---> Fe2O3
b, -Tính khối lượng mol của Al2O3
- Số mol của 20,4g Al2O3, 2,24 lít CO2 (đktc)
a,hoàn thành PTHH sau và cho biết tỉ lệ số nguyên tử (phân tử) các chất trong phản ứng hóa học sau
- 2Mg + O2 --to-> 2MgO
=>2:1:2
- 4Fe +3 O2 -to--> 2Fe2O3
4:3:2
b, -Tính khối lượng mol của Al2O3
=>MAl2O3=102đvC
- Số mol của 20,4g Al2O3, 2,24 lít CO2 (đktc)
=>n Al2O3=2mol
n CO2=0,1 mol
Đúng 2
Bình luận (0)
Tính số nguyên tử và phân tử có trong mỗi lượng chất 1,5 mol phân tử h2o
Đốt cháy hết 9g magnesium (mg) trong không khí thu được 15g hợp chất magnesium oxide ( mgo) biết rằng magnesium cháy là xảy ra phản ứng với khí oxygen ( 02) trong không khí
A) viết biểu thức về khối lượng của phản ứng xảy ra
B) tính khối lượng của khí oxygen đã phản ứng
Tính tỉ khối
A) khí carbon dioxide co2 nặng hơn hay nhẹ hơn khí hydrogen h2 bao nhiêu lần?
B) khí methane ( ch4) nặng hay nhẹ hơn không khí bao nhiêu l...
Đọc tiếp
Tính số nguyên tử và phân tử có trong mỗi lượng chất 1,5 mol phân tử h2o Đốt cháy hết 9g magnesium (mg) trong không khí thu được 15g hợp chất magnesium oxide ( mgo) biết rằng magnesium cháy là xảy ra phản ứng với khí oxygen ( 02) trong không khí A) viết biểu thức về khối lượng của phản ứng xảy ra B) tính khối lượng của khí oxygen đã phản ứng Tính tỉ khối A) khí carbon dioxide co2 nặng hơn hay nhẹ hơn khí hydrogen h2 bao nhiêu lần? B) khí methane ( ch4) nặng hay nhẹ hơn không khí bao nhiêu lần? Tính nồng độ A) hòa tan 20g nacl vào 140g nước tính nồng độ của dung dịch thu được B) tính nồng độ mol của 350 g dung dịch chứa 74,2g na2co3 Ở 20 độ c , khi tan 40g potasium nitrate vào 95 g nước thì thu được dung dịch bão hòa . Vậy ở 20 độ c, độ tan của potasium nitrate là bao nhiêu? Cho khối lượng của fe là 5,6g phản ứng với dung dịch hydrochlorio acid hcl . a . Tính khối lượng của muối iron ( III) chloride fecl2 tạo thành Tính thể tích khí hydrogen h2 sinh ra ở điều kiện chuẩn ( 25°c và 1bar) ?
a) Tính số mol và số nguyên tữ có trong 14 gam Fe
b) Phải lấy bao nhiêu MgO để số phân tử MgO nhiều hơn gấp 2,5 lần số phân tử có trong 32 gam Fe2O3 ?
c) Viết phương trình hóa học khi cho Fe2O3 tác dụng axit clohidric HCl tạo muối ( hợp chất gồm sắt và clo) và khí hidro
Cho: H= 1; C=12; N=14; O=16; Mg=24; K= 39; Fe=56
Nguyên tử của nguyên tố A có tổng số hạt không mang điện bằng 15/26 tổng số hạt mang điện. trong 1 phân tử của A có 3 nguyên tử A và Oxi. biết phân tử khối là 232 và tổng số hạt có trong phan tử là 342.
a) tính số hạt mỗi loại trong phân tử
b) tính số hạt p, e, n có trong nguyên tử của nguyên tố A. Từ đó xác định nguyên tố A