Cho 9.1023 phân tử Na2CO3
a) Hãy tính số mol của Na2CO3 . Từ đó suy ra số mol của các nguyên tử Na , C , O
b) Hãy tính số phân tử Na2CO3 , số nguyên tử Na , C , O
Bài 1: a) Hãy cho biết số phân tử có mặt trong 2 mol phân tử FeO b) Tính số mol nguyên tử của 24.1023 nguyên tử Na c) Tính khối lượng của 0,05 mol phân tử đường glucozơ C6H12O6 d) Tính thể tích khí được đo ở đktc của 1,2 mol N2O5
Hợp chất A mạch hở (chứa C, H, O). Lấy cùng 1 số mol A cho tác dụng với Na2CO3 hoặc Na (đều dư) thì nCO2=3/4 nH2. Biết MA=192, trong A có số nguyên tử O <8. A không bị oxh bởi CuO/ t˚ và có tính đối xứng. Số đồng phân A thỏa mãn là:
A. 4
B. 3
C. 1
D. 2
Bài 6: Hãy tính số mol của các lượng chất sau:
a/ 14 g canxi oxit ( CaO )
b/ 3.1023 nguyên tử cacbon ( C )
c/ 9.1023 phân tử nước ( H2O )
d/ 16 g khí Oxi ( O2 )
Biết C = 12 ; O = 16 ; Ca = 40 ; H = 1
\(a,n_{CaO}=\dfrac{14}{40}=0,35(mol)\\ b,n_{C}=\dfrac{3.10^{-23}}{6.10^{-23}}=0,5(mol)\\ c,n_{H_2O}=\dfrac{9.10^{-23}}{6.10^{-23}}=1,5(mol)\\ d,n_{O_2}=\dfrac{16}{32}=0,5(mol)\)
Cho phương trình Na + O2 ===> Na2O
a) Hãy cân bằng phương trình trên
b) Cho biết chất phản ứng , sản phẩm , điều kiện phản ứng
c) Cho biết tỉ lệ số phân tử , nguyên tử của các cặp chất
d) Tìm số phân tử O2 cần dùng và số nguyên tử Na2O sinh ra khi đốt cháy hoàn toàn 40 nguyên tử Na
e) Tính khối lượng oxi cần dùng để đốt cháy 46g O2
a) 4Na + O2 -> 2Na2O ( 1 )
b) chất phản ứng : Na tác dụng với O2
Sản phẩm : Na2O
Điều kiện : nhiệt độ
c) Số nguyên tử Na : Số phân tử O2 : Số phân tử Na2O = 4 : 1 : 2
d) ....
e) nNa = 46 : 23 = 2 mol
Từ pt(1) => nO2 = \(\frac{1}{4}nNa=\frac{1}{4}2=\frac{1}{2}\)=0,5mol
=> mO2 = 0,5 . 32 = 16g
Hãy tìm số mol nguyên tử hoặc số mol phân tử của những lượng chất sau :
a) 0,6 N nguyên tử O
b) 1,8 N phân tử N2
c) 0,66.1023 phân tử C12H22O11 (đường).
a) Số mol:0,1 (mol)
b) 0,3 mol
c) 0,11 mol
Câu 11 :Cho biết số nguyên tử, phân tử có trong 1,5 mol H2O là :
A. 6.1023 nguyên tử B. 9.1023 phân tử
C. 9.1023 nguyên tử D. 3.1023 phân tử
Câu 11 :Cho biết số nguyên tử, phân tử có trong 1,5 mol H2O là :
A. 6.1023 nguyên tử B. 9.1023 phân tử
C. 9.1023 nguyên tử D. 3.1023 phân tử
Số phân tử có trong 1,5 mol H2O là: \(1,5.6.10^{23}=9.10^{23}\) phân tử
=> Đáp án B
Cho biết thành phần theo khối lượng của một số hợp chất, hãy tìm công thức hóa học của chúng:
- Hợp chất A: 0,2 mol hợp chất có chứa 4,6g Na và 7,1g Cl.
- Hợp chất B: 0,03 mol hợp chất có chứa 0,36g C và 0,96g O.
- Hợp chất C: 0,02 mol hợp chất có chứa 4,14g Pb và 0,32g O.
- Hợp chất D: 0,04 mol hợp chất có chứa 0,08 mol nguyên tử Fe và 0,12 mol nguyên tử O.
- Hợp chất E: 0,02 mol hợp chất có 0,04 mol nguyên tử Na, 0,02mol nguyên tử C và 0,06 mol nguyên tử O.
- Hợp chất A:
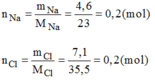
Cứ 0,2 mol hợp chất A có chứa 0,2 mol Na và 0,2 mol Cl.
Suy ra 1 mol hợp chất A có chứa 1 mol Na và 1 mol Cl.
Vậy công thức hóa học đơn giản của A là NaCl.
- Hợp chất B:
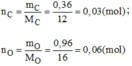
Vậy 0,03mol phân tử B có chứa 0,03 mol phân tử C và 0,06 mol nguyên tử O.
Suy ra 1 mol phân tử B có chứa 1 mol nguyên tử C và 2 mol nguyên tử O.
→Công thức hóa học của B là C O 2
- Hợp chất C:
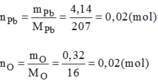
Vậy 0,02 mol phân tử C có chứa 0,02 mol nguyên tử Pb và 0,02 mol nguyên tử O.
Suy ra 1 mol phân tử C có chứa 1 mol nguyên tử Pb và 1 mol nguyên tử O.
→Công thức của phân tử C là: PbO.
- Hợp chất D:
Theo đề bài: 0,04 mol phân tử D có 0,08 mol Fe và 3 mol O.
Vậy 1 mol phân tử D có: 2 mol Fe và 0,12 mol O.
→ Công thức hóa học của D là F e 2 O 3
- Hợp chất E:
Cho biết: 0,02 mol phân tử E có 0,04 mol Na kết hợp 0,02 mol C và 0,06 mol nguyên tử O.
Vậy 1 mol phân tử E co 2 mol Na kết hợp 1 mol C và 3 mol O.
Công thức hóa học của E là N a 2 C O 3 .
Hãy tìm số mol nguyên tử hoặc số mol phân tử của những lượng chất sau: 0,6N nguyên tử O; 1,8N nguyên tử N 2 ; 0,9N nguyên tử H; 1,5N phân tử H 2 ; 0,15N phân tử O 2 ; 0,05N nguyên tử C
0,6N nguyên tử O = 0,6 mol nguyên tử O.
1,8N phân tử N 2 = 1,8 mol phân tử N 2 .
0,9N nguyên tử H = 0,9 mol nguyên tử H.
1,5N phân tử H 2 = 1,5 mol phân tử H 2 .
0,15N phân tử O2 = 0,15 mol phân tử O 2 .
0,05N nguyên tử C = 0,05 mol nguyên tử C.