Nguyên tử X có tổng số hạt bằng 28 Số khối nhỏ hơn 20 .Xác định thành phần cấu tạo của nguyên tử X

Những câu hỏi liên quan
nguyên tử X có tổng số hạt cơ bản X là 28. số khối nhỏ hơn 20 xác định kí hiệu nguyên tử X
\(\left\{{}\begin{matrix}P+N+E=28\\P=E=Z\\P\le N\le1,5P\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}2P+N=28\\P\le N\le1,5P\end{matrix}\right.\\ \Leftrightarrow\left\{{}\begin{matrix}N=28-2P\\P\le28-2P\le1,5P\end{matrix}\right.\\ \Leftrightarrow\left\{{}\begin{matrix}N=28-2P\\3P\le28\le3,5P\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}N=28-2P\\8\le P\le9\end{matrix}\right.\\ TH1:\left\{{}\begin{matrix}P=E=Z=8\\N=12\end{matrix}\right.\Rightarrow A=Z+N=8+12=20\left(đ.v.C\right)\left(loại\right)\\ TH2:\left\{{}\begin{matrix}P=E=Z=9\\N=10\end{matrix}\right.\Rightarrow A=Z+N=9+10=19\left(đ.v.C\right)\left(19< 20\right)\left(Nhận\right)\\ \Rightarrow KH:^{19}_9F\)
Đúng 1
Bình luận (0)
Nguyên tử X có tổng số các loại hạt bằng 52, trong đó hạt mang điện nhiều hơn số hạt không mang điện là 16 hạt. a) Xác định thành phần các hạt cấu tạo nên nguyên tử X b) Viết kí hiệu nguyên tử X
a: Theo đề, ta có:
2Z+N=52 và 2Z-N=16
=>2Z=34 và N=18
=>N=18 và Z=17
Vậy: e=p=17 và n=18
b:
Số khối là 17+18=35
Kí hiệu nguyên tử là:
\(^{35}_{17}X\)
Đúng 1
Bình luận (1)
Tổng số hạt của nguyên tử x là 82 ,trong đó tổng số hạt mang điện nhiều hơn số hạt không mang điện là 22 .hãy xác định thành phần cấu tạo của nguyên tử x
\(\left\{{}\begin{matrix}P+N+E=82\\\left(P+E\right)-N=22\\P=E\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}2P+N=82\\2P-N=22\end{matrix}\right.\\ \Leftrightarrow\left\{{}\begin{matrix}P=E=26\\N=30\end{matrix}\right.\)
Đúng 1
Bình luận (1)
Ta có: p + e + n = 82 hay 2p + n = 82 (do p = e)
Mà p+e-n=22=> n=2p- 22
=> 4p=104=> p=26
=> e=p=26 và n=2p-22=30
Đúng 1
Bình luận (0)
Tổng số hạt proton, nơtron và electron trong 1 nguyên tử nguyên tố X là 82:
p + e + n = 82 hay 2p + n = 82 (do p = e) (1)
Số hạt mang điện (p và e) nhiều hơn số hạt không mang điện (n) là 22 hạt
(p+e) – n = 22 hay 2p – n = 22 (2)
Giải (1), (2) ta có p = e = 26; n =30
Số khối của X = Z + N = p + n =56
Đúng 1
Bình luận (1)
Bài 3. Nguyên tử của nguyên tố X có tổng số hạt là 26, trong nguyên tử X số hạt mang điện nhiều hơn số hạt không mang điện 6 hạt. Hãy xác địnha. Xác định thành phần cấu tạo của nguyên tử X ( số p; số e; số n)b. X thuộc nguyên tố hóa học nào? Viết KHHH.c. Phân tử X nặng hay nhẹ hơn và nặng bằng bao nhiêu lần phân tử lưu huỳnh đioxit ( 1S và 2O) ? Viết CTHH của đơn chất X và của hợp chất lưu huỳnh đioxit.
Đọc tiếp
Bài 3. Nguyên tử của nguyên tố X có tổng số hạt là 26, trong nguyên tử X số hạt mang điện nhiều hơn số hạt không mang điện 6 hạt. Hãy xác định
a. Xác định thành phần cấu tạo của nguyên tử X ( số p; số e; số n)
b. X thuộc nguyên tố hóa học nào? Viết KHHH.
c. Phân tử X nặng hay nhẹ hơn và nặng bằng bao nhiêu lần phân tử lưu huỳnh đioxit ( 1S và 2O) ? Viết CTHH của đơn chất X và của hợp chất lưu huỳnh đioxit.
cho mình hỏi bài này làm sao vậy Bài 1 : nguyên tử X có tổng số hạt các loại là 28 hạt . Số notron nhiều hơn số proton 1 hạt a) xác định số hạt mỗi loại ? b) tính số khối của hạt nhân nguyên tử X c) viết cấu hình electron nguyên tử d) nguyên tố X thuộc loại nguyên tố nào ( kim loại , phi kim , khí hiếm ) ?.Bài 2 : nguyên tử của nguyên tố B có tổng số các hạt cấu tạo là 93 . Trong đó số hạt mang điện nhiều hơn không mang điện là 23 hạt .Xác định số hiệu nguyên tử của nguyên tố và viết cấu hình el...
Đọc tiếp
cho mình hỏi bài này làm sao vậy
Bài 1 : nguyên tử X có tổng số hạt các loại là 28 hạt . Số notron nhiều hơn số proton 1 hạt
a) xác định số hạt mỗi loại ?
b) tính số khối của hạt nhân nguyên tử X
c) viết cấu hình electron nguyên tử
d) nguyên tố X thuộc loại nguyên tố nào ( kim loại , phi kim , khí hiếm ) ?.
Bài 2 : nguyên tử của nguyên tố B có tổng số các hạt cấu tạo là 93 . Trong đó số hạt mang điện nhiều hơn không mang điện là 23 hạt .Xác định số hiệu nguyên tử của nguyên tố và viết cấu hình electron nguyên tử của nó .
Bài 3 : nguyên tử của nguyên tố A có tổng số các hạt cấu tạo là 40 . Xác định số hiệu nguyên tử của nguyên tố và viết cấu hình electron nguyên tử của nó .
ta co p+e+n=93 mà p=e=z => 2z+n=93
2z-n=23 ( vì số hạt mang điện nhiều hơn số hạt ko mang điện là 23)
tu 2 pt trên ta có z =29,,n=35
=> số hiệu nguyên tử của B = Z = 29
cấu hình electron
\(1s^22s^22p^63s^23p^64s^23d^9\)
Đúng 0
Bình luận (0)
đối với các dạng bài này , bạn cần nhớ kiến thức như sau :
Tổng số hạt trong nguyên tử = 2p + n ( gồm có 3 loại hạt : n , p, e trong đó p=e)
số hạt mang điện là 2p
số hạt không mang điện là n
số hiệu nguyên tử là Z= p = e = số thứ tự nhóm .
Sau khi xác định được p ,, tức là cũng xác định được e thì
cấu hình viết theo dãy trật tự các mức năng lượng
1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s2 4d10.......
Các nguyên tử có 1, 2, 3e ở lớp ngoài cùng là các nguyên tử kim loại, trừ H, He và B.Các nguyên tử có 5, 6, 7e ở lớp ngoài cùng thường là các nguyên tố phi kim. Các nguyên tử có 4e ở lớp ngoài cùng có thể là nguyên tử kim loại hoặc phi kim
Đúng 0
Bình luận (3)
bài 1 : a/
tacó p+e+n=28
<=> z+z+n=28
> 2z+n=28 1
vì n lớn hơn p là 1 nên ta có pt:
n-z=1hay -z+n=1 2
từ 1 và 2 ta có hệ phương trình
2z+n=28
-z+n=1
=>z= 9,n=10
b/ số khối A = Z + N = 9 + 10 = 19
c/ Cấu hình electron nguyên tử :\(1s^22s^22p^63s^23p^64s^1\)
d/ Nguyên tố X là kim loại cụ thể ở đây là Kali
Đúng 0
Bình luận (3)
Xem thêm câu trả lời
Nguyên tử của nguyên tố X có tổng số hạt là 54.Biết số hạt ở vỏ ít hơn số hạt trong nhân là 20
a) Xác định số hạt mỗi loại
b) Vẽ mô hình cấu tạo nguyên tử X
a, Số electron: (54 - 20) : 2 = 17 (hạt)
Tổng số proton và neutron: 54 - 17 = 37 (hạt)
Ta có: số e = số p = 17
=> số n = 37 - 17 = 20
Đúng 4
Bình luận (0)
Xem thêm câu trả lời
a) Tổng số hạt của X là 10. Xác định thành phần cấu tạo của nguyên tố X b) Nguyên tử A có tổng số hạt là 58. Tính số hạt cơ bản của A
a, Theo đề: p + n + e = 10
Mà: p = e (Do nguyên tử trung hòa về điện)
⇒ 2p + n = 10 ⇒ n = 10 - 2p
Mà: \(1\le\dfrac{n}{p}\le1,5\) \(\Rightarrow1\le\dfrac{10-2p}{p}\le1,5\) \(\Rightarrow2,85\le p\le3,33\)
⇒ p = e = 3, n = 4
Vậy: Nguyên tử nguyên tố X gồm 3 electron, 3 proton và 4 notron.
b, Ta có: p + n = e = 58
Mà: p = e (Do nguyên tử trung hòa về điện)
⇒ 2p + n = 58 ⇒ n = 58 - 2p
Mà: \(1\le\dfrac{n}{p}\le1,5\) \(\Rightarrow1\le\dfrac{58-2p}{p}\le1,5\) \(\Rightarrow16,57\le p\le19,3\)
⇒ p = 19 là thỏa mãn.
Vậy: p = e = 19, n = 20
Đúng 1
Bình luận (0)
Một nguyên tử X có tổng số hạt là 58. Biết rằng nguyên tử khối của X nhỏ hơn 40. Xác định số hạt mỗi loại của nguyên tử X. Cho biết kí hiệu hoá học và tên gọi của X ( coi nguyên tử khối bằng khối lượng hạt nhân).
Một nguyên tử X có tổng số hạt là 58
=> 2Z + N = 58 (1)
=>N = 58 - 2Z
Nguyên tử khối của X nhỏ hơn 40
=> A = Z + N <40
=> Z + 58 - 2Z < 40
=> Z > 18 (1)
Mặt khác : Z ≤ N ≤ 1,5Z
=> Z ≤ 58 - 2Z ≤ 1,5Z
=> 16,57 ≤ Z ≤ 19,33(2)
Từ (1), (2) => Z=P = E = 19 ; N= 20
Z = 19 => X là Kali (K)
Đúng 3
Bình luận (0)
nguyên tử của nguyên tố X có tổng số hạt cơ bản là 28 hạt,trong đó số hạt không mang điện bằng 35,7% tổng số hạt.Xác định cấu tạo của nguyên tử X
N=0,357.28=10
=> P=E=(28-10)/2=9
=> Z=9
=> Cấu tạo nguyên tử:
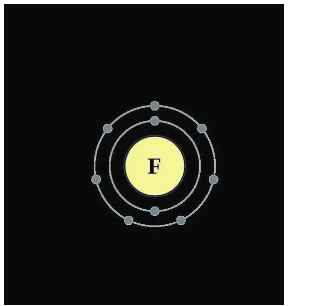
Đúng 2
Bình luận (0)





















