Hòa tan hoàn toàn 5,4g nhôm vào dung dịch H2SO4 1M thu được dung dịch A và V lít H2(đktc). Trung hòa axit dư trong dung dịch A cần 200ml dung dịch NaOH 1M. Gía trị của V và thể tích dung dịch H2SO4 đã dùng là bao nhiêu?

Những câu hỏi liên quan
Hòa tan hoàn toàn 8g CuO vào dung dịch H2SO4 1M. Để trung hòa lượng axit dư trong dung dịch sau phản ứng cần dùng 240ml dung dịch NaOH 0.5M và thu được dung dịch A
a)Thể tích H2SO4 đã dùng?b) Nồng độ mol của các chất trong dung dịch A?
\(n_{CuO}=\dfrac{8}{80}=0.1\left(mol\right)\)
\(CuO+H_2SO_4\rightarrow CuSO_4+H_2O\)
\(0.1...........0.1.........0.1\)
\(n_{NaOH}=0.24\cdot0.5=0.12\left(mol\right)\)
\(2NaOH+H_2SO_4\rightarrow Na_2SO_4+H_2O\)
\(0.12..........0.06\)
\(n_{H_2SO_4}=0.1+0.06=0.16\left(mol\right)\)
\(V_{dd_{H_2SO_4}}=\dfrac{0.16}{1}=0.16\left(l\right)\)
\(C_{M_{H_2SO_4\left(dư\right)}}=\dfrac{0.06}{0.16}=0.375\left(M\right)\)
\(C_{M_{CuSO_4}}=\dfrac{0.1}{0.16}=0.625\left(M\right)\)
Đúng 2
Bình luận (1)
hòa tan hoàn toàn 19,5 gam một kim loại M ( M có hóa trị 2 trong hợp chất ) dung dịch HCl 1M dư thu được dung dịch A và 6,72 lít khí H2 (ở đktc )
a) xác định kim loại M.
b) đẻ trung hòa axits dư trong A cần 200ml dung dịch NaOH 1M. tính thể tích dung dịch HCl 1M đã dùng và nồng độ mol của dung dịch A ( coi thể tích dung dịch A bằng thể tích dung dịch HCl ban đầu )
nH2=\(\frac{6,72}{22,4}=0,3\)mol
PTHH
M+2HCl--> MCl2+H2
0,3mol<---------------0,3mol
=>MM=\(\frac{19,5}{0,3}=64\)
=> km loại là kẽm (Zn)
b) nNaOH=0,2.1=0,2 mol
PTHH
NaOH+HCl-->NaCl + H2O
0,2 mol--> 0,2 mol
---> thể tích HCl 1M đã dùng là V=\(\frac{0,2+0,3}{1}=0,5\)lít
=> CM(ZnCl2)=\(\frac{0,3}{0,5}=0,6M\)
Đúng 0
Bình luận (0)
Hòa tan hoàn toàn m gam hỗn hợp Na, K vào nước dư thu được dung dịch X và 3,36 lít H2 (đktc). Thể tích dung dịch chứa HCl 1M và H2SO4 1M cần dùng để trung hòa hết dung dịch X là A. 150 ml B. 200 ml C. 300 ml D. 100 ml
Đọc tiếp
Hòa tan hoàn toàn m gam hỗn hợp Na, K vào nước dư thu được dung dịch X và 3,36 lít H2 (đktc). Thể tích dung dịch chứa HCl 1M và H2SO4 1M cần dùng để trung hòa hết dung dịch X là
A. 150 ml
B. 200 ml
C. 300 ml
D. 100 ml
Đáp án D
nH2 = 3,36 : 22,4 = 0,15 (mol)
=> nOH- = 2nH2 = 0,3 (mol)
H+ + OH- → H2O
nH + = nOH - = 0,3 (mol)
Mặt khác: nH+ = nHCl + 2nH2SO4 = V + 2V = 3V (mol)
=> 3V = 0,3 => V =0,1 (lít) = 100 (ml)
Đúng 0
Bình luận (0)
Hòa tan hoàn toàn m gam hỗn hợp Na, K vào nước dư thu được dung dịch X và 3,36 lít H2 (đktc). Thể tích dung dịch chứa HCl 1M và H2SO4 1M cần dùng để trung hòa hết dung dịch X là A. 150 ml. B. 200 ml. C. 300 ml. D. 100 ml.
Đọc tiếp
Hòa tan hoàn toàn m gam hỗn hợp Na, K vào nước dư thu được dung dịch X và 3,36 lít H2 (đktc). Thể tích dung dịch chứa HCl 1M và H2SO4 1M cần dùng để trung hòa hết dung dịch X là
A. 150 ml.
B. 200 ml.
C. 300 ml.
D. 100 ml.
Giải thích:
nH2 = 3,36 : 22,4 = 0,15 (mol)
=> nOH- = 2nH2 = 0,3 (mol)
H+ + OH- → H2O
nH + = nOH - = 0,3 (mol)
Mặt khác: nH+ = nHCl + 2nH2SO4 = V + 2V = 3V (mol)
=> 3V = 0,3 => V =0,1 (lít) = 100 (ml)
Đáp án D
Đúng 0
Bình luận (0)
Hòa tan hoàn toàn 12,8g hh A gồm Fe và FeO trong 250 ml dd H2SO4 1M loãng (lấy dư) thu được 2,24l H2 (đktc) và dung dịch B.
a. Tính phần trăm khối lượng mỗi chất trong hh A .
b, Trung hòa dung dịch B cần dùng V ml dung dịch NaOH 1M. Tính giá trị V
a, gọi a= nFe
b= nFeO
=> 56a + 72b= 12,8 (1)
Fe +H2SO4 -> FeSO4 +H2
a b b a
FeO +H2SO4 -> FeSO4 +H2O
b b b
a=nH2 = 2,24/22,4= 0,1 mol
từ (1) => b= 0,1
mFe= 56.0,1=5,6(g)
m FeO = 72.0,1= 7,2(g)
b, nH2SO4 (bđ) = 0,25 mol
nH2SO4 pứ = a+b =0,2 mol
=> nH2SO4 dư = 0,25-0,2=0,05 mol
2NaOH +H2SO4 -> Na2SO4 +2H2O
0,1 0,05
V(NaOH)= 0,1/ 1= 0,1 lit =100ml
Đúng 1
Bình luận (1)
E tham khảo! Anh nãy làm tại câu hỏi bấm lộn xóa

Đúng 2
Bình luận (0)
Hòa tan hoàn toàn a gam hỗn hợp Al và
A
l
2
O
3
vào dung dịch
H
2
S
O
4
loãng, thu được dung dịch X và 1,008 lít khí
H
2
(đktc). Cho từ từ dung dịch NaOH 1M vào X, số mol kết tủa
A
l
O...
Đọc tiếp
Hòa tan hoàn toàn a gam hỗn hợp Al và A l 2 O 3 vào dung dịch H 2 S O 4 loãng, thu được dung dịch X và 1,008 lít khí H 2 (đktc). Cho từ từ dung dịch NaOH 1M vào X, số mol kết tủa A l O H 3 (n mol) phụ thuộc vào thể tích dung dịch NaOH (V lít) được biểu diễn bằng đồ thị dưới đây:
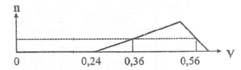
Giá trị của a là
A. 2,34.
B. 7,95.
C. 3,87.
D. 2,43.
Đáp án C
+ Từ đồ thị biểu diễn quá trình phản ứng của dung dịch NaOH với X, ta thấy X chứa HCl và AlCl3.
+ Gọi x là thể tích NaOH dùng để trung hòa HCl và làm kết tủa hết AlCl3 trong X, ta có đồ thị:
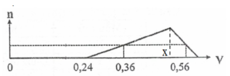
D ự a v à o P T P Ư t a c ó : x - 0 , 36 = 3 . ( 0 , 56 - x ) → x = 0 , 51 n H C l = n N a O H t r u n g h ò a = 0 , 24 , n A l C l 3 = n N a O H t r u n g h ò a 3 = 0 , 51 - 0 , 24 3 = 0 , 09 B T e : n A l = 2 . n H 2 3 = 0 , 03 B T N T A l : n A l 2 O 3 = n A l C l 3 - n A l 2 = 0 , 03 → a = = 3 , 87 g
Đúng 0
Bình luận (0)
Hòa tan hoàn toàn a gam hỗn hợp Al và Al2O3 vào dung dịch H2SO4 loãng thu được dung dịch X và 1,008 lít khí H2 (đktc). Cho từ từ dung dịch NaOH 1M vào X, số mol kết tủa Al(OH)3 (n mol) phụ thuộc vào thể tích dung dịch NaOH (V lít) được biểu diễn bằng đồ thị dưới đây Giá trị của a là A. 2,34 B. 7,95 C. 3,87 D. 2,43
Đọc tiếp
Hòa tan hoàn toàn a gam hỗn hợp Al và Al2O3 vào dung dịch H2SO4 loãng thu được dung dịch X và 1,008 lít khí H2 (đktc). Cho từ từ dung dịch NaOH 1M vào X, số mol kết tủa Al(OH)3 (n mol) phụ thuộc vào thể tích dung dịch NaOH (V lít) được biểu diễn bằng đồ thị dưới đây
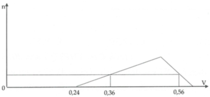
Giá trị của a là
A. 2,34
B. 7,95
C. 3,87
D. 2,43
Hòa tan hoàn toàn a gam hỗn hợp Al và Al2O3 vào dung dịch H2SO4 loãng, thu được dung dịch X và 1,008 lít khí H2 (đktc). Cho từ từ dung dịch NaOH 1M vào X, số mol kết tủa Al(OH)3 (n mol) phụ thuộc vào thể tích dung dịch NaOH (V lít) được biểu diễn bằng đồ thị dưới đây: Giá trị của a là A. 2,34. B. 7,95. C. 3,87. D. 2,43.
Đọc tiếp
Hòa tan hoàn toàn a gam hỗn hợp Al và Al2O3 vào dung dịch H2SO4 loãng, thu được dung dịch X và 1,008 lít khí H2 (đktc). Cho từ từ dung dịch NaOH 1M vào X, số mol kết tủa Al(OH)3 (n mol) phụ thuộc vào thể tích dung dịch NaOH (V lít) được biểu diễn bằng đồ thị dưới đây:
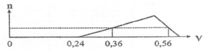
Giá trị của a là
A. 2,34.
B. 7,95.
C. 3,87.
D. 2,43.
1. Hòa tan hoàn toàn 5,4g nhôm cần vừa đủ V(l) dung dịch H2SO4 0,2M sau phản ứng thu được dung dịch B và X (lit) H2(đktc).
a) TÌm V?
b) Tìm X?
c) Tính CM của muối thu được trong dung dịch B?
2. Để hòa tan hoàn toàn m(g) kẽm cần vừa đủ 100(g) dung dịch H2SO4 4,9% .
a) Tìm m?
b) Tìm V lít khí thoát ra ở đktc?
c) Tính C% của muối thu được sau sau phản ứng?
Bài 1 :
Số mol của nhôm
nAl = \(\dfrac{m_{Al}}{M_{Al}}=\dfrac{5,4}{27}=0,2\left(mol\right)\)
Pt : 2Al + 3H2SO4 → Al2(SO4)3 + 3H2\(|\)
2 3 1 3
0,2 0,3 0,3
a) Số mol của dung dịch axit sunfuric
nH2SO4 = \(\dfrac{0,2.3}{2}=0,3\left(mol\right)\)
Thể tích của dung dịch axit sunfuric
CMH2SO4 = \(\dfrac{n}{V}\Rightarrow V=\dfrac{n}{C_M}=\dfrac{0,3}{0,2}=1,5\left(l\right)\)
b) Số mol của khí hidro
nH2 = \(\dfrac{0,3.3}{3}=0,3\left(mol\right)\)
Thể tích của khí hidro ở dktc
VH2 = nH2 . 22,4
= 0,3. 22,4
= 6,72 (l)
Chúc bạn học tốt
Đúng 0
Bình luận (0)
2. Để hòa tan hoàn toàn m(g) kẽm cần vừa đủ 100(g) dung dịch H2SO4 4,9% .
a) Tìm m?
b) Tìm V lít khí thoát ra ở đktc?
c) Tính C% của muối thu được sau sau phản ứng?
---
a) mH2SO4=4,9%.100=4,9(g) -> nH2SO4=4,9/98=0,05(mol)
PTHH: Zn + H2SO4 -> ZnSO4 + H2
Ta có: nZn=nZnSO4=nH2=nH2SO4=0,05(mol)
m=mZn=0,05.65=3,25(g)
b) V(H2,đktc)=0,05.22,4=1,12(l)
c) mZnSO4=0,05. 161=8,05(g)
mddZnSO4=mZn + mddH2SO4 - mH2= 3,25+100 - 0,05.2=103,15(g)
=> C%ddZnSO4= (8,05/103,15).100=7,804%
Đúng 1
Bình luận (0)
Bài 2 :
Khối lượng của axit sunfuric
C0/0H2SO4 = \(\dfrac{m_{ct}.100}{m_{dd}}\Rightarrow m_{ct}=\dfrac{C.m_{dd}}{100}=\dfrac{4,9.100}{100}=4,9\left(g\right)\)
Số mol của axit sunfuric
nH2SO4 = \(\dfrac{m_{H2SO4}}{M_{H2SO4}}=\dfrac{4,9}{98}=0,05\left(mol\right)\)
Pt : Zn + H2SO4 → ZnSO4 + H2\(|\)
1 1 1 1
0,05 0,05 0,05 0,05
a) Số mol của kẽm
nZn = \(\dfrac{0,05.1}{1}=0,05\left(mol\right)\)
Khối lượng của kẽm
mZn = nZn . MZn
= 0,05 . 65
= 3,25 (g)
b) Số mol của khí hidro
nH2 = \(\dfrac{0,05.1}{1}=0,05\left(mol\right)\)
Thể tích của khí hidro ở dktc
VH2 = nH2 . 22,4
= 0,05 . 22,4
= 1,12 (l)
c) Số mol của muối kẽm clorua
nZnCl2 = \(\dfrac{0,05.1}{1}=0,05\left(mol\right)\)
Khối lượng của muối kẽm sunfat
mZnSO4 = nZnSO4 . MZnSO4
= 0,05 . 161
= 8,05 (g)
Khối lượng của dung dịch sau phản ứng
mdung dịch sau phản ứng = mZn + mH2SO4 - mH2
= 3,25 + 100 - (0,05 . 2)
= 103,15 (g)
Nồng độ phàn trăm của muối kẽm sunfat
C0/0ZnSO4= \(\dfrac{m_{ct}.100}{m_{dd}}=\dfrac{8,05.100}{103,15}=7,8\)0/0
Chúc bạn học tốt
Đúng 0
Bình luận (0)
















