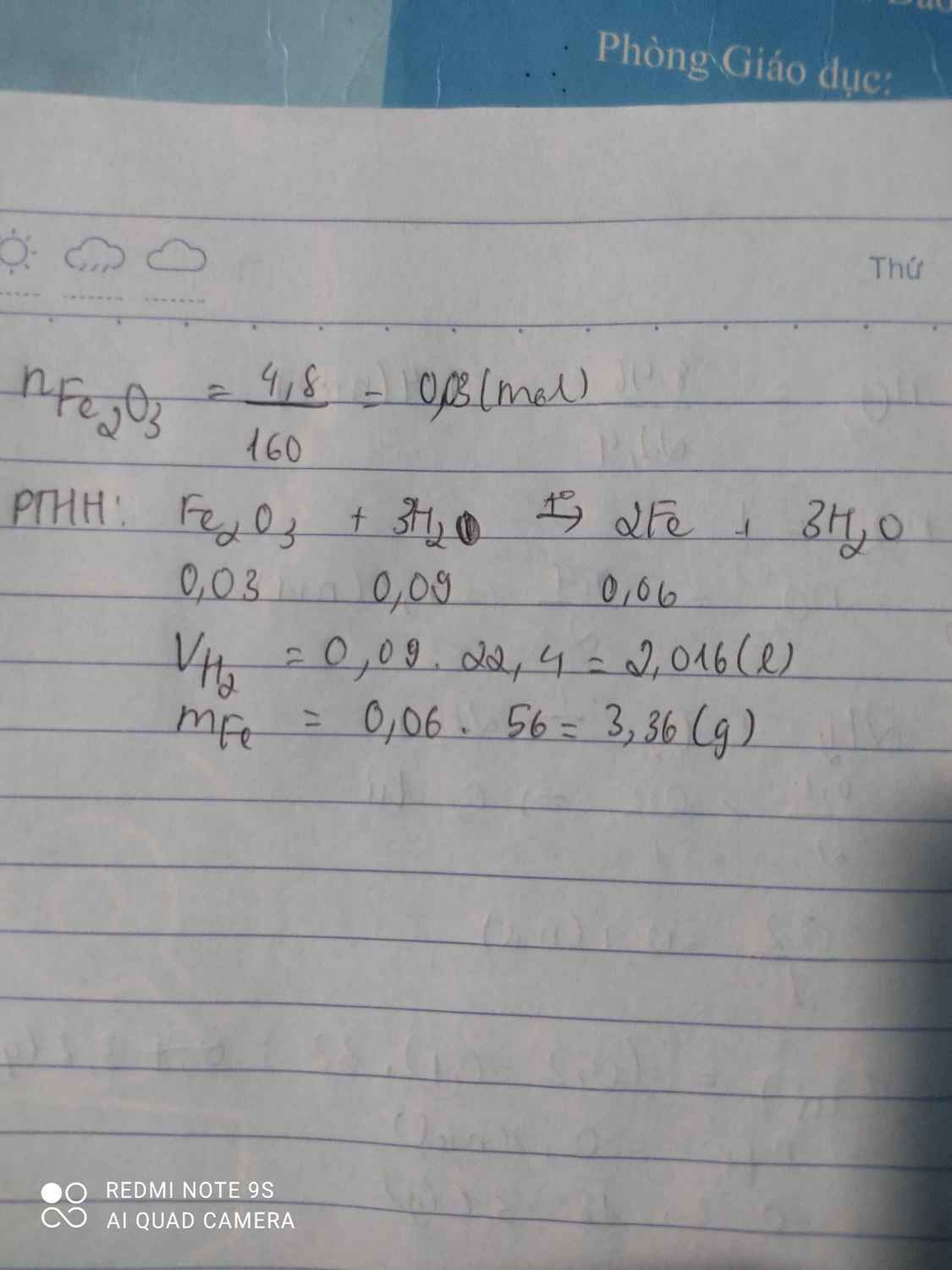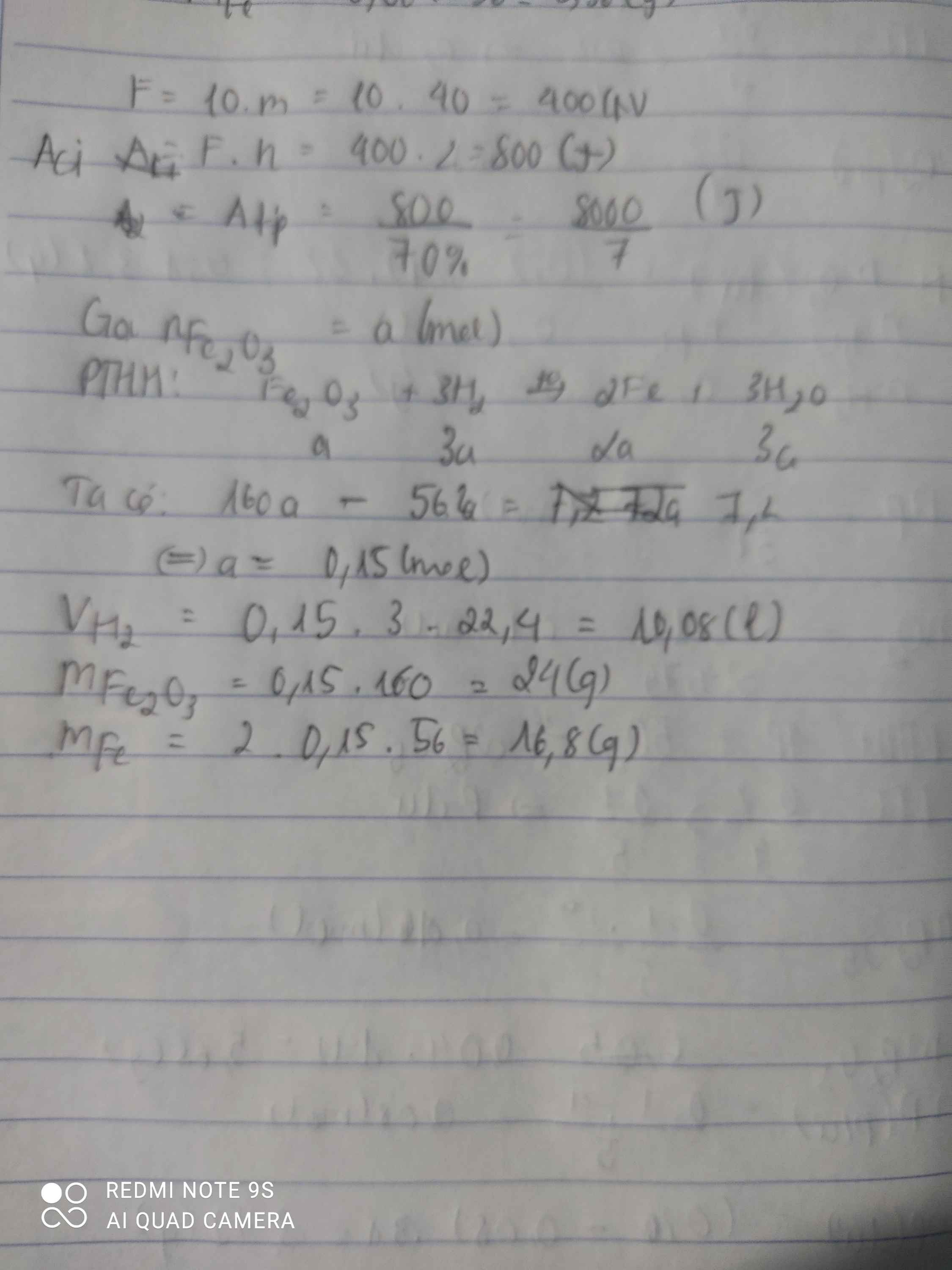Dẫn 13,44l H2 (điều kiện tiêu chuẩn) qua ống đựng 20g Fe2O3 thu được chất rắn A. Tính khối lượng chất rắn A?

Những câu hỏi liên quan
- Giúp mình với :)))
1) Đốt cháy hoàn toàn hỗn hợp gồm 12g Mg và 16g Cu trong Oxi sau phản ứng thu được MgO và CuO
a) Thể tích O trong phản ứng ở điều kiện tiêu chuẩn.
b) Khối lượng CuO , MgO thu được.
2) Fe2O3 + CO -> Fe + CO2
Dẫn 13,44l khí CO đ.k.t.c qua ống đựng 40g Fe2O3 nung nóng thu được chất rắn A.
Tính khối lượng chất rắn A.
theo đề bài:
nMg=12/24=0,5mol
nCu=16/64=0,25mol
PTPU:
2Mg+O2->2MgO
0,5.......0,25....0,5(mol)
2Cu+O2->2CuO
0,25...0,125.....0,25(mol)
nO2=0,375mol
VO2=0,375.22,4=8,4(lít)
b)nMgO=0,5mol=>mMgO=0,5.40=20g
nCuO=0,25mol=>mCuO=0,25.80=20g
câu 2:
nCO=13,44/22,4=0,6mol
nFe2O3=40/160=0,25mol
PTPU:
\(Fe_2O_3+CO->2Fe+2CO_2\)
0,25.................0,25....0,5.........0,5(mol)
nFe=0,5mol=>mFe=0,5.56=28g
Đúng 0
Bình luận (5)
Xem thêm câu trả lời
Hỗn hợp X gồm FeO Fe2O3 Fe304 cho một luồng khí CO đi qua ống sứ đựng m gam hỗn hợp X đun nóng. Sau khi kết thúc thí nghiệm thu được 64 gam chất rắn A trong ống sứ và 11,2 llít khí B ở điều kiện tiêu chuẩn có tỉ khối so với H2 là 20,4. Tính giá trị m Giải bài này hộ e chi tiết xíu :))
\(n_{CO}=a\left(mol\right),n_{CO_2}=b\left(mol\right)\)
\(n_B=a+b=0.5\left(mol\right)\)
\(m_B=20.4\cdot2\cdot0.5=20.4\left(g\right)\)
\(\Leftrightarrow28a+44b=20.4\)
\(KĐ:a=0.1,b=0.4\)
\(n_{CO\left(pư\right)}=n_{CO_2}=0.4\left(mol\right)\)
\(BTKL:\)
\(m=0.4\cdot44+64-0.4\cdot28=70.4\left(g\right)\)
Đúng 3
Bình luận (0)
Cho V l hỗn hợp gồm H2 và CO ở điều kiện tiêu chuẩn qua ống sứ đựng m gam Fe2 O3 đun nóng chất rắn a còn lại trong ống gồm fe304 và feo có khối lượng m - 2,24 g hòa tan chất rắn A bằng một lượng dung dịch HCl 1,9 m vừa đủ thấy cần 800 ml Viết các phương trình phản ứng có thể xảy ra và Tính m, v
Xem chi tiết
PTHH :
\(Fe_2O_3 +3H_2 \xrightarrow{t^o} 2FeO + H_2O\\ 3Fe_2O_3 + CO \xrightarrow{t^o} 2Fe_3O_4 + CO_2\\ FeO + 2HCl \to FeCl_2 + H_2O\\ Fe_3O_4 + 8HCl \to FeCl_2 + 2FeCl_3 + 4H_2O \)
\(m_{giảm} = m_{O\ pư} = m - (m-2,24) = 2,24\\ \Rightarrow n_{O\ pư} = \dfrac{2,24}{16} = 0,14(mol)\\ H_2 + O_{oxit} \to H_2O\\ CO + O_{oxit} \to CO_2\\ n_{H_2} + n_{CO} = n_{O\ pư} = 0,14(mol)\\ \Rightarrow V = 0,14.22,4 = 3,136(lít)\\ n_{H^+} = n_{HCl} = 0,8.1,9 = 1,52(mol)\\ 2H^+ + O^{2-} \to H_2O\\ \Rightarrow n_{O(trong\ A)} = \dfrac{n_{H^+}}{2} = 0,76(mol)\\ \Rightarrow n_{O(trong\ Fe_2O_3} = 0,76 + 0,14 = 0,9(mol)\\ \)
\(n_{Fe_2O_3} = \dfrac{n_O}{3} = 0,3(mol)\\ \Rightarrow m = 0,3.160 = 48\ gam\)
Đúng 1
Bình luận (0)
: Dẫn 11,2 lít H2 (ĐKTC) qua ống nghiệm đựng 80 gam Fe2O3 rồi nung nóng. Sau phản ứng, chất nào còn dư? Chất nào đã hết? Tính khối lượng chất rắn thu được (Fe = 56; O = 16; H = 1)
\(n_{H_2}=\dfrac{11,2}{22,4}=0,5\left(m\right)\);\(n_{Fe_2O_3}=\dfrac{80}{160}=0,5\left(m\right)\)
\(PTHH:Fe_2O_3+3H_2\xrightarrow[]{t^o}2Fe+3H_2O\)
ta có tỉ lệ:\(\dfrac{0,5}{1}>\dfrac{0,5}{3}\)=>\(Fe_2O_3\) dư
H2 phản ứng hết
\(PTHH:Fe_2O_3+3H_2\xrightarrow[]{t^o}2Fe+3H_2O\)
tỉ lệ :1 3 2 3
số mol :0,17 0,5 0,3 0,5
\(m_{Fe_2O_3}=0,3.160=48\left(g\right)\)
Đúng 2
Bình luận (0)
Cho luồng khí CO đi qua ống sứ đựng m gam hỗn hợp gồm Fe FeO Fe2 O3 nung nóng sau khi kết thúc thí nghiệm thu được 6,4 g chất rắn a và 11,2 lít khí B ở điều kiện tiêu chuẩn có tỉ khối so với H2 là 20,4 Tính m
B gồm CO(a mol) ; CO2( b mol)
Ta có:
\(n_B = a + b = \dfrac{11,2}{22,4}=0,5(mol)\\ m_B = 28a + 44b = 0,5.2.20,4 = 20,4(gam)\\ \Rightarrow a = 0,1 ; b = 0,4\\ CO + O_{oxit} \to CO_2\\ n_O = n_{CO_2} = 0,4(mol)\\ \Rightarrow m = m_A + m_{O\ pư} = 6,4 + 0,4.16 = 12,8(gam)\)
Đúng 1
Bình luận (0)
Các phản ứng khử sắt oxit có thể có:
3Fe2O3 + CO --> 2Fe3O4 + CO2 (1)
Fe3O4 + CO --> 3FeO + CO2 (2)
FeO + CO --> Fe + CO2 (3)
Như vậy chất rắn A có thể gồm 3 chất Fe, FeO, Fe3O4 hoặc ít hơn, điều đó không quan trọng và việc cân bằng các phương trình trên cũng không cần thiết, quan trọng là số mol CO phản ứng bao giờ cũng bằng số mol CO2 tạo thành. nB = 11,2/22,5 = 0,5 mol
Gọi x là số mol của CO2 ta có phương trình về khối lượng của B:
44x + 28(0,5 x) = 0,5 x 20,4 x 2 = 20,4
nhận được x = 0,4 mol và đó cũng chính là số mol CO tham gia phản ứng.
Theo ĐLBTKL ta có:
mX + mCO = mA + mCO2
--> m = 64 + 0,4 x 44 - 0,4 x 28 = 70,4 gam.
Đúng 0
Bình luận (1)
dẫn khí H2 dư qua m gam bột Fe2O3 khi phản ứng xảy ra hoàn toàn lấy chất rắn cân lại thấy khối lượng giảm 4,8 g
a Tính thể tích H2 cần dùng ở điều kiện tiêu chuẩn
b Tính m và khối lượng sắt thu được lm nhnh giúp mik vs ạ T_T
mik cảm ơn
a) Gọi số mol H2 phản ứng là a (mol)
PTHH: Fe2O3 + 3H2 --to--> 2Fe + 3H2O
mgiảm = mO(mất đi) = 4,8 (g)
=> nO(mất đi) = \(\dfrac{4,8}{16}=0,3\left(mol\right)\)
=> \(n_{H_2O}=0,3\left(mol\right)\)
=> \(n_{H_2}=0,3\left(mol\right)\)
=> \(V_{H_2}=0,3.22,4=6,72\left(l\right)\)
b) \(n_{Fe}=0,2\left(mol\right)\)
=> \(m_{Fe}=0,2.56=11,2\left(g\right)\)
\(n_{Fe_2O_3}=0,1\left(mol\right)\)
=> \(m_{Fe_2O_3}=0,1.160=16\left(g\right)\)
Đúng 3
Bình luận (3)
dẫn hidro nóng dư đi qua ống chứa 24g hỗn hợp CuO và Fe2O3 cho đến khi phản ứng kết thúc lấy chất rắn còn lại trong ống sứ cho tác dụng với dung dịch HCl dư có 4,48 lít khí thoát ra ở điều kiện tiêu chuẩn. Tính khối lượng mỗi chất có trong hỗn hợp ban đầu.
GIÚP TỚ VÓI Ạ, CẦN GẤP Ạ!!
PT: \(CuO+H_2\underrightarrow{t^o}Cu+H_2O\)
\(Fe_2O_3+3H_2\underrightarrow{t^o}2Fe+3H_2O\)
\(Fe+2HCl\rightarrow FeCl_2+H_2\)
Ta có: \(n_{H_2}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\)
Theo PT: \(n_{Fe}=n_{H_2}=0,2\left(mol\right)\)
\(n_{Fe_2O_3}=\dfrac{1}{2}n_{Fe}=0,1\left(mol\right)\)
\(\Rightarrow m_{Fe_2O_3}=0,1.160=16\left(g\right)\)
⇒ mCuO = 24 - 16 = 8 (g)
Đúng 3
Bình luận (1)
Dẫn luồng khí H2 dư đi qua ống nghiệm chứa 16 gam CuO nung nóng .Sau một thời gian thu được chất rắn A. Hòa tan hoàn toàn A bằng một lượng vừa đủ dung dịch H2SO4 đặc nóng thu được dung dịch B và 3,36 lít( điều kiện tiêu chuẩn) khí không màu mùi xốc.
a. tính phần trăm khối lượng cho đã bị khử
b. cho dung dịch B phản ứng với dung dịch Ba(OH)2 dư. Sau khi phản ứng kết thúc lọc lấy kết tủa nung đến khối lượng không đổi. Tính khối lượng chất rắn thu được sau khi nung
Lm hộ mik vs ạ
!!!
Đọc tiếp
Dẫn luồng khí H2 dư đi qua ống nghiệm chứa 16 gam CuO nung nóng .Sau một thời gian thu được chất rắn A. Hòa tan hoàn toàn A bằng một lượng vừa đủ dung dịch H2SO4 đặc nóng thu được dung dịch B và 3,36 lít( điều kiện tiêu chuẩn) khí không màu mùi xốc. a. tính phần trăm khối lượng cho đã bị khử b. cho dung dịch B phản ứng với dung dịch Ba(OH)2 dư. Sau khi phản ứng kết thúc lọc lấy kết tủa nung đến khối lượng không đổi. Tính khối lượng chất rắn thu được sau khi nung Lm hộ mik vs ạ !!!
a)
\(n_{CuO}=\dfrac{16}{80}=0,2\left(mol\right)\)
Gọi số mol CuO bị khử là a
\(n_{SO_2}=\dfrac{3,36}{22,4}=0,15\left(mol\right)\)
PTHH: CuO + H2 --to--> Cu + H2O
a----------------->a
Cu + 2H2SO4 --> CuSO4 + SO2 + 2H2O
a---------------------------->a
=> a = 0,15 (mol)
=> Phần trăm CuO bị khử = \(\dfrac{0,15}{0,2}.100\%=75\%\)
b)
Bảo toàn Cu: \(n_{CuSO_4}=n_{CuO}=0,2\left(mol\right)\)
=> \(\left\{{}\begin{matrix}n_{BaSO_4}=0,2\left(mol\right)\\n_{CuO}=0,2\left(mol\right)\end{matrix}\right.\)
=> mrắn = 0,2.233 + 0,2.80 = 62,6(g)
Đúng 1
Bình luận (0)
dẫn khí H2 dư qua m gam bột Fe2O3 khi phản ứng xảy ra hoàn toàn lấy chất rắn cân lại cân lại ,thấy khối lượng giảm 7,2 g
a) Tính thể tích H2 cần dùng ở điều kiện tiêu chuẩn
b) Tính m và khối lượng sắt thu được
xem giúp mik vs ;-;