Cho 5,4 gam kim loại R hòa tan hoàn toàn trong H2SO4 đặc nóng, phản ứng kết thúc thu được 6,72 lít SO2 sản phẩm khử duy nhất ở đktc. Tìm kim loại R và tính khối lượng muối tạo thành

Những câu hỏi liên quan
Bài 7. Cho 5,4 gam kim loại R tan hoàn toàn trong H2SO4 đặc nóng, phản ứng kết thúc thu được 6,72 lít SO2 sản phẩm khí duy nhất ở đktc. Tìm kim loại R và tính khối lượng muối tạo thành sau phản ứng?
Giải theo cách lớp 8 nhé
Đặt hoá trị của kim loại R là n (n ∈ N*)
\(n_{SO_2}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\)
PTHH: \(2R+2nH_2SO_{4\left(đặc,nóng\right)}\rightarrow R_2\left(SO_4\right)_n+nSO_2\uparrow+2nH_2O\)
\(\dfrac{0,6}{n}\)<---------------------------------------------0,3
\(\rightarrow M_R=\dfrac{5,4}{\dfrac{0,6}{n}}=9n\left(g\text{/}mol\right)\)
Vì n hoá trị của R nên ta xét bảng
| n | 1 | 2 | 3 |
| MR | 9 | 18 | 27 |
| Loại | Loại | Al |
---> Vậy R là Al
Đúng 3
Bình luận (1)
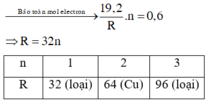
Hòa tan 19,2 gam kim loại R trong
H
2
SO
4
đặc, dư thu được 6,72 lít khí
SO
2
(sản phẩm khử duy nhất ở đktc). Kim loại R là A. Cu. B. Mg. C. Ba. D. Fe.
Đọc tiếp
Hòa tan 19,2 gam kim loại R trong H 2 SO 4 đặc, dư thu được 6,72 lít khí SO 2 (sản phẩm khử duy nhất ở đktc). Kim loại R là
A. Cu.
B. Mg.
C. Ba.
D. Fe.
a) Cho 12 gam hỗn hợp hai kim loại Cu, Fe (tỉ lệ mol tương ứng là 1:1) tan hoàn toàn trong H2SO4 đặc, nóng, dư thu được V lít SO2 (sản phẩm khử duy nhất, đktc). Tính giá trị của V.b) Cho 4,5 gam một kim loại R tan hoàn toàn trong H2SO4 đặc nóng dư thu được 2,24 lít hỗn hợp hai khí SO2 và H2S (đktc) có tỉ khối so với H2 là 24,5 và dung dịch X. Tìm kim loại R và khối lượng muối tạo thành trong dung dịch sau phản ứng
Đọc tiếp
a) Cho 12 gam hỗn hợp hai kim loại Cu, Fe (tỉ lệ mol tương ứng là 1:1) tan hoàn toàn trong H2SO4 đặc, nóng, dư thu được V lít SO2 (sản phẩm khử duy nhất, đktc). Tính giá trị của V.
b) Cho 4,5 gam một kim loại R tan hoàn toàn trong H2SO4 đặc nóng dư thu được 2,24 lít hỗn hợp hai khí SO2 và H2S (đktc) có tỉ khối so với H2 là 24,5 và dung dịch X. Tìm kim loại R và khối lượng muối tạo thành trong dung dịch sau phản ứng
a) Gọi nCu = a (mol) => nFe = a (mol)
=> 64a + 56a = 12
=> a = 0,1 (mol)
PTHH:
Cu + 2H2SO4 (đặc, nóng) ---> CuSO4 + SO2 + 2H2O
0,1------------------------------------------->0,1
2Fe + 6H2SO4 (đặc, nóng) ---> Fe2(SO4)3 + 3SO2 + 6H2O
0,1--------------------------------------------------->0,3
=> VSO2 = (0,3 + 0,1).22,4 = 8,96 (l)
b) \(n_{hh}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\)
\(M_{hh}=24,5.2=49\left(\dfrac{g}{mol}\right)\)
Áp dụng sơ đồ đường chéo, ta có:
\(\dfrac{n_{SO_2}}{n_{H_2S}}=\dfrac{V_{SO_2}}{V_{H_2S}}=\dfrac{64-49}{49-34}=\dfrac{1}{1}\)
\(\rightarrow n_{SO_2}=n_{H_2S}=\dfrac{0,1}{2}=0,05\left(mol\right)\)
PTHH:
2R + 2nH2SO4 (đặc, nóng) ---> R2(SO4)n + nSO2 + 2nH2O
\(\dfrac{0,1}{n}\)<------------------------------------------------0,05
8R + 5nH2SO4 (đặc, nóng) ---> 4R2(SO4)n + nH2S + 4nH2O
\(\dfrac{0,4}{n}\)<-------------------------------------------------0,05
\(\rightarrow n_R=\dfrac{0,1}{n}+\dfrac{0,4}{n}=\dfrac{0,5}{n}\left(mol\right)\\ \rightarrow M_R=\dfrac{4,5}{\dfrac{0,5}{n}}=9n\left(\dfrac{g}{mol}\right)\)
Xét n = 3 thoả mãn => MR = 27 (g/mol)
Vậy R là Al
Đúng 1
Bình luận (0)
Cho 17,2 gam hỗn hợp kim loại gồm Fe cà Cu tác dụng vừa đủ với dd H2SO4 đặc nóng dư thu được 6,72 lít khí SO2 (đktc) là sản phẩm khử duy nhất. Tính khối lượng mỗi muối và khối lượng dung dịch H2SO4 80% phản ứng
`2Fe + 6H_2 SO_[4(đ,n)] -> Fe_2(SO_4)_3 + 3SO_2 \uparrow + 6H_2 O`
`0,05` `0,15` `0,025` `(mol)`
`Cu + 2H_2 SO_[4(đ,n)] -> CuSO_4 + SO_2 \uparrow + 2H_2 O`
`0,225` `0,45` `0,225` `(mol)`
`n_[SO_2]=[6,72]/[22,4]=0,3(mol)`
Gọi `n_[Fe]=x` ; `n_[Cu]=y`
`=>` $\begin{cases} \dfrac{3}{2}x+y=0,3\\56x+64y=17,2 \end{cases}$
`<=>` $\begin{cases}x=0,05\\y=0,225 \end{cases}$
`@m_[Fe_2(SO_4)_3]=0,025.400=10(g)`
`@m_[CuSO_4]=0,225.160=36(g)`
`@m_[dd H_2 SO_4]=[(0,15+0,45).98]/80 .100=73,5(g)`
Đúng 4
Bình luận (0)
Sửa đề: 80% ---> 98% (80% chưa đặc nên không giải phóng SO2 được)
Gọi \(\left\{{}\begin{matrix}n_{Fe}=a\left(mol\right)\\n_{Cu}=b\left(mol\right)\end{matrix}\right.\)
\(\rightarrow56a+64b=17,2\left(1\right)\)
PTHH:
\(2Fe+6H_2SO_{4\left(đặc,nóng\right)}\rightarrow Fe_2\left(SO_4\right)_3+3SO_2\uparrow+6H_2O\)
a------>3a------------------->0,5a--------------->1,5a
\(Cu+2H_2SO_{4\left(đặc,nóng\right)}\rightarrow CuSO_4+SO_2\uparrow+2H_2O\)
b----->2b------------------->b------------->b
\(\rightarrow1,5a+b=\dfrac{6,72}{22,4}=0,3\left(2\right)\)
Từ \(\left(1\right)\left(2\right)\rightarrow\left\{{}\begin{matrix}a=0,05\left(mol\right)\\b=0,225\left(mol\right)\end{matrix}\right.\)
\(\rightarrow\left\{{}\begin{matrix}m_{Fe_2\left(SO_4\right)_3}=0,5.0,05.400=10\left(g\right)\\m_{CuSO_4}=0,225.160=36\left(g\right)\\m_{ddH_2SO_4}=\dfrac{\left(0,05.3+0,225.2\right).98}{98\%}=60\left(g\right)\end{matrix}\right.\)
Đúng 2
Bình luận (0)
Hòa tan hết 9,6 gam kim loại M trong dung dịch H2SO4 đặc, nóng thu được SO2 là sản phẩm khử duy nhất. Cho toàn bộ lượng SO2 này hấp thụ vào 0,4 lít dung dịch KOH 0,6M, sau phản ứng cô cạn dung dịch thu được 21,42 gam hỗn hợp muối. Kim loại M là A. Ca B. Mg C. Fe D. Cu
Đọc tiếp
Hòa tan hết 9,6 gam kim loại M trong dung dịch H2SO4 đặc, nóng thu được SO2 là sản phẩm khử duy nhất. Cho toàn bộ lượng SO2 này hấp thụ vào 0,4 lít dung dịch KOH 0,6M, sau phản ứng cô cạn dung dịch thu được 21,42 gam hỗn hợp muối. Kim loại M là
A. Ca
B. Mg
C. Fe
D. Cu
Hòa tan hết 9,6 gam kim loại M trong dung dịch H2SO4 đặc, nóng thu được SO2 là sản phẩm khử duy nhất. Cho toàn bộ lượng SO2 này hấp thụ vào 0,4 lít dung dịch KOH 0,6M sau phản ứng cô cạn dung dịch thu được 21,42 gam hỗn hợp muối. Kim loại M là A. Ca. B. Mg. C. Fe. D. Cu.
Đọc tiếp
Hòa tan hết 9,6 gam kim loại M trong dung dịch H2SO4 đặc, nóng thu được SO2 là sản phẩm khử duy nhất. Cho toàn bộ lượng SO2 này hấp thụ vào 0,4 lít dung dịch KOH 0,6M sau phản ứng cô cạn dung dịch thu được 21,42 gam hỗn hợp muối. Kim loại M là
A. Ca.
B. Mg.
C. Fe.
D. Cu.
Đáp án D.
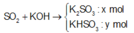
Ta có hệ phương trình
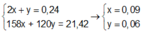
![]()
Gọi hóa trị của kim loại M là n
Áp dụng định luật bảo toàn electron ta có
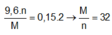
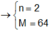
Đúng 0
Bình luận (0)
Hòa tan hết 9,6 gam kim loại M trong dung dịch H2SO4 đặc, nóng thu được SO2 là sản phẩm khử duy nhất. Cho toàn bộ lượng SO2 này hấp thụ vào 0,4 lít dung dịch KOH 0,6M sau phản ứng cô cạn dung dịch thu được 21,42 gam hỗn hợp muối. Kim loại M là A. Ca. B. Mg. C. Fe. D. Cu.
Đọc tiếp
Hòa tan hết 9,6 gam kim loại M trong dung dịch H2SO4 đặc, nóng thu được SO2 là sản phẩm khử duy nhất. Cho toàn bộ lượng SO2 này hấp thụ vào 0,4 lít dung dịch KOH 0,6M sau phản ứng cô cạn dung dịch thu được 21,42 gam hỗn hợp muối. Kim loại M là
A. Ca.
B. Mg.
C. Fe.
D. Cu.
Câu 3: Cho 4,5g một kim loại R tan hoàn toàn trong H2SO4 đặc nóng thu được 2,24 lít hỗn hợp SO2, H2S có tỉ khối so với H2 là 24,5 và dung dịch X. Tìm kim loại R và tính khối lượng muối tạo thành trong dung dịch sau phản ứng?
- Áp dụng phương pháp đường chéo ta có :\(n_{H_2S}=n_{SO2}\)
\(\Rightarrow n_{H_2S}=n_{SO2}=\dfrac{1}{2}n_{hh}=0,05mol\)
\(Bte:xn_R=\dfrac{4,5x}{R}=2n_{SO2}+8n_{H2O}=0,5\)
- Lập bảng giá trị thấy : \(\left(x;R\right)=\left(3;27\right)\) TM
=> Kim loại đó là Al .
\(BTNT\left(Al\right):n_{Al2\left(SO4\right)3}=\dfrac{1}{2}n_{Al}=\dfrac{1}{12}mol\)
\(\Rightarrow m_M=28,5g\)
Đúng 1
Bình luận (0)
Cho 11g hỗn hợp Al, Fe phản ứng hoàn toàn với H2SO4 đặc nóng dư, thu được 10,08 lít SO2 sản phẩm khử duy nhất ở đktc và đúng dịch A. a. Tính % theo khối lượng của mỗi kim loại trong hỗn hợp. b. Tính khối lượng dd H2SO4 đã dùng biết dd H2SO4 có nồng độ 98% và đã dùng dư 20% so lượng cần thiết đểu phản ứng.