1. Hãy biểu diễn dung dịch H2SO4 đặc 98% ( d= 1,84g/ml) theo nồng độ mol.
2. Hãy lập biểu thức liên hệ giữa nồng độ phần trăm, khối lượng riêng và nồng độ mol
1.Có m gam dung dịch X chứa chất tan A(khối lượng mol MA),nồng độ C%.Thiết lập biểu thức liên hệ giữa các đại lượng trên.
2.Có m gam dung dịch y chứa n mol chất tan A, khối lượng riêng của dung dịch là D \(\dfrac{gam}{ml}\).Thiết lập biểu thức liên hệ giữa các đại lượng trên.
1/ \(n_A=\dfrac{m_{dd}.C\%}{100.M_A}\)
2/ \(V_{dd}=\dfrac{m}{D}\)
=> \(C_M=\dfrac{n}{V}=\dfrac{n.D}{m}\)
Lập công thức liên hệ giữa nồng độ phần trăm, khối lượng riêng và nồng độ mol
Lú quá rồi nhỉ. Dưới là đáp án em có nhưng em cần cách làm ạ. Anh chị làm xong có thể check đáp án ở dưới. Mong anh chị không hiểu lầm em tự đăng tự trả lời. Em xin lỗi.
Lập biểu thức liên hệ giữa nồng độ % (C%), nồng độ mol/l (CM) và khối lượng riêng D.
Lấy V lít hay 1000V ml dung dịch
=> Khối lượng dung dịch là: mdd = 100V. D
=> Khối lượng chất tan là:\( {m_{c\tan }} = {{{m_{dd}}} \over {100\% }}.C\% = {{1000V.D} \over {100\% }}.C\% = 10V.D.C\% \)
=> Số mol của chất tan là: \({n_{c\tan }} = {{{m_{c\tan }}} \over M} = {{10V.D.C\% } \over M}\)
Mà ta có:
\(\eqalign{ & {C_M} = {{{n_{c\tan }}} \over V} = {{{{10V.D.C\% } \over M}} \over V} \cr & \Rightarrow {C_M} = {{10.D.C\% } \over M}\,\,\,\,\,\,(dpcm) \cr} \)
\(C\%=\dfrac{C_M.M}{10D}\\ C_M=\dfrac{C\%.10D}{M}\)
Giải thích các đại lượng:
C%: nồng độ phần trăm (%)
CM: nồng độ mol (mol/l hay M)
D: khối lượng riêng (g/ml)
M: khối lượng mol (g/mol)
Hãy tính toán và trình bày cách pha chế 0,5lit dung dịch H 2 S O 4 có nồng độ 1mol/l từ H 2 S O 4 có nồng độ 98%, khối lượng riêng là 1,84g/ml.
* Số mol của H 2 S O 4 cần để pha chế 500ml dung dịch H 2 S O 4 1M:
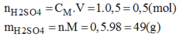
* Khối lượng H 2 S O 4 98% có chứa 49g H 2 S O 4 :
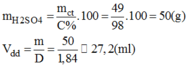
* Cách pha chế: Đổ khoảng 400ml nước cất vào cốc có chia độ có dung tích khoảng 1lit. Rót từ từ 27,2ml H 2 S O 4 98% vào cốc khuấy đều. Sau đó thêm dần dần nước cất vào cốc cho đủ 500ml. ta pha chế được 500ml dung dịch H 2 S O 4 1M.
1. Nồng độ dung dịch là j? Thế nào là nồng độ phần trăm (khối lượng), nồng độ mol (mol/l)
2. Lập biểu thức liên hệ giữa độ tan và nồng độ phần trăm củ chất tan trog dung dịch bão hoà chất đó.
1)
- nồng độ dung dịch :
+ nồng độ phần trăm
+ nồng độ mol
- nồng độ phần trăm là cho biết số gam chất tan có trong 100 gam dd
Khối lượng chất tan là mct
Khối lượng dd là mdd
Nồng độ phần trăm là C%
=> C% = \(\frac{m_{ct}.100}{m_{dd}}\)
- Nồng độ mol của dd là cho biết số mol chất tan cú trong một lit dd
CM =\(\frac{n}{C_v}\)
2.
công thức liên hệ là :
C% = \(\frac{S}{S+100}.100\%\)
Câu 1 :
- Nồng độ dung dịch gồm :
+ Nồng độ phần trăm của dd : cho biết số gam chất tan có trong 100 gam dd
+ Nồng độ mol của dd : cho biết số mol chất tan cú trong một lit dd
Câu 2 :
C% = S/(S+100) *100%
Cho 32g NaOH vào nước được 400ml dd có khối lượng riêng D=1,2g/ml . Tính nồng độ mol và nồng độ phần trăm của dung dịch
9 / Hãy viết công thức tính nồng độ phần trăm , khối lượng chất tan, khối lượng dung dịch và nồng độ mol/l . ( 1đ
Nồng độ phần trăm :
C% = \(\dfrac{m_{ct}}{m_{dd}}.100\%\)
Khối lượng chất tan = mdd - m dung môi
Khối lượng dung dịch = mctan + mdung môi
Nồng độ mol CM = n/v
\(C\% = \dfrac{m_{chất\ tan}}{m_{dung\ dịch}}.100\%\\ m_{chất\ tan} = m_{dd}.C\%\\ m_{dung\ dịch} = \dfrac{m_{chất\ tan}}{C\%}\\ C_M = \dfrac{n_{chất\ tan}}{V_{dung\ dịch}}\)
Hòa tan 36,5 gam HCl vào nước, thu được 500ml dung dịch có khối lượng riêng D = 1,1 g/ml. Tính nồng độ mol và nồng độ phần trăm của dung dịch thu được.
Hòa tan 21,8 gam hh 2oxit Na2O và K2O có tỉ lệ mol là 2 : 1 vào một lượng nước rồi thêm cho đủ 500 ml dung dịch. tính nồng độ mol và nồng độ phần trăm mỗi chất trong dung dịch thu được, biết dung dịch có khối lượng riêng D=1,04g/cm3