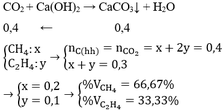dẫn 11,2 hỗn hợp khí CO2 và CO vào 100ml dung dịch Ca(OH)2 thu được một muối không tan có khối lượng là 40g. Tính nồng độ mol của Ca(OH)2 và phần trăm về thể tích của CO2 trong hỗn hợp ban đầu

Những câu hỏi liên quan
Dẫn 4,48 lít hỗn hợp khí CO,CO2 (đktc) vào 100ml dd Cả(OH)2,thu được muối duy nhất không tán, có khối lượng 10g. Tính nồng độ mol của dung dịch Ca(OH)2
nCO2+CO=\(\dfrac{4,48}{22,4}\)= 0,2(mol)
CO2 + Ca(OH)2 \(\rightarrow\) CaCO3\(\downarrow\) + H2O (*)
Muối duy nhất không tan là CaCO3\(\downarrow\)
nCaCO3=\(\dfrac{10}{100}\)= 0,1(mol)
\(\Rightarrow\)Theo (*) nCaCO3=nCa(OH)2= 0,1(mol)
\(\Rightarrow\) CM Ca(OH)2=\(\dfrac{0,1}{0,1}\)= 1(M)
Đúng 0
Bình luận (0)
Dẫn 11.2 lít hỗn hợp khí CO và CO2 (đktc) vào dung dịch Ca(OH)2 thu được muối không tan có khối lượng là 10g.tính khối lượng thành phần % theo khối lượng của khí CO2 có trong hỗn hợp
Xem chi tiết
\(CO_2 + Ca(OH)_2 \to CaCO_3 + H_2O\)
Theo PTHH :
\(n_{CO_2} = n_{CaCO_3} = \dfrac{10}{100} = 0,1\ mol\)
\(n_{hỗn\ hợp\ khí} = \dfrac{11,2}{22,4} = 0,5(mol)\)
⇒ \(n_{CO} = 0,5 - 0,1 = 0,4(mol)\)
Suy ra : mhỗn hợp = 0,1.44 + 0,4.28 = 15,6(gam)
Vậy :
\(\%m_{CO_2} = \dfrac{0,1.44}{15,6}.100\% = 28,21\%\\\%m_{CO} = 100\% -28,21\% = 71,79\%\)
Đúng 2
Bình luận (1)
Dẫn luồng khí CO dư đi qua 20,05 gam hỗn hợp hai oxit ZnO và
F
e
2
O
3
ở nhiệt độ cao, thu được hỗn hợp hai kim loại và khí
C
O
2
. Dẫn khí
C
O
2
sinh ra vào dung dịch
C
a
(
O
H
)
2
dư, thu được 35 gam kết tủa.Viết phản ứng xảy ra.Tính khối...
Đọc tiếp
Dẫn luồng khí CO dư đi qua 20,05 gam hỗn hợp hai oxit ZnO và F e 2 O 3 ở nhiệt độ cao, thu được hỗn hợp hai kim loại và khí C O 2 . Dẫn khí C O 2 sinh ra vào dung dịch C a ( O H ) 2 dư, thu được 35 gam kết tủa.
Viết phản ứng xảy ra.
Tính khối lượng mỗi kim loại tạo thành.
Tính thành phần phần trăm theo khối lượng mỗi oxit trong hỗn hợp ban đầu.
Đốt cháy hoàn toàn 3,66 lít hỗn hợp khí gồm CO và CH4 cần dùng hết 3,66 lít khí CO2 a) Tính thành phần % về thể tích của mỗi khí trong hỗn hợp ban đầu? b) Sục toàn bộ dd CO2 thu được vào 100ml dd Ca(OH)2 1,5M.Tính khối lượng kết tủa tạo thành M.n giải giúp mình vs mình đang cần gấp
Đốt cháy hoàn toàn 0,3 mol hỗn hợp metan và etilen. Lấy toàn bộ lượng khí CO2 sinh ra cho vào dung dịch Ca(OH)2 dư thu được 40 gam kết tủa. Tính phần trăm về thể tích mỗi khí trong hỗn hợp ban đầu (các khí trên đo ở cùng điều kiện).
Dẫn 11,2l hỗn hợp khí CO, CO2(đktc) vào dung dịch Ca(OH)2 thu được muối không tan có khối lượng 10 gam. Tính thành phần phần trăm theo thể tích của CO2 trong hỗn hợp
https://i.imgur.com/WHHIgmF.jpg
Cho 22,4 lít hỗn hợp X gồm hai khí CO, CO2 đi qua than nóng đỏ (không có mặt không khí) thu được khí Y có thể tích hơn thể tích X là 7,84 lít (thể tích khí đo được ở đktc). Dẫn Y đi qua dung dịch Ca(OH)2 vừa đủ thì thu được dung dịch chỉ chứa 20,25 gam Ca(HCO3)2. Thành phần phần trăm về thể tích của khí CO trong hỗn hợp X là: A. 25% B. 37,5% C. 40% D. 50%
Đọc tiếp
Cho 22,4 lít hỗn hợp X gồm hai khí CO, CO2 đi qua than nóng đỏ (không có mặt không khí) thu được khí Y có thể tích hơn thể tích X là 7,84 lít (thể tích khí đo được ở đktc). Dẫn Y đi qua dung dịch Ca(OH)2 vừa đủ thì thu được dung dịch chỉ chứa 20,25 gam Ca(HCO3)2. Thành phần phần trăm về thể tích của khí CO trong hỗn hợp X là:
A. 25%
B. 37,5%
C. 40%
D. 50%
Đáp án C
Đặt nCO= x mol; n C O 2 = y mol trong hỗn hợp X
→ x+ y= 22,4/22,4= 1mol (1)
CO2+ C → t 0 2CO
z z 2z mol
Khí Y chứa 2z+x mol khí CO và y-z mol khí CO2
nY - nX = 7,84/22,4 = 0,35 mol
→ nY = 0,35+ 1 = 1,35 mol
→ 2z +x + y-z = 1,35→ x+ y + z = 1,35 mol (2)
2CO2+ Ca(OH)2 → Ca(HCO3)2
Ta có: n C O 2 = 2. n C a ( H C O 3 ) 2 = 2.20,25/162 = 0,25 mol
→ y - z = 0,25 (3)
Từ (1,2,3) ta có x = 0,4; y = 0,6; z = 0,35 mol
→ % V C O = % n C O = 0 , 4 1 . 100 % = 40 %
Đúng 0
Bình luận (0)
Hòa tan hết 4,68 g hỗn họp 2 muối ACO3 và BCO3 bằng dung dịch H2SO4 loangx , sau phản ứng thu được 1 dung dịch X và 1,12 lít CO2 ở đktc .a.Tính tổng khôi lượng các muối tạo thành trong dung dịch X.b.Tìm các kim loại A,B và tính thành phần phần trăm theo khối lượng của muối trong hỗn hợp đầu, biết nACO:nBCO32:3, MA:MB3:5.c. Cho toàn bộ lượng khí CO2 thu được ở trên hấp thụ vào 200 ml dung dịch Ba(OH)2. Tính nồng độ mol của dung dịch Ba(OH)2 để thu được 1,97 g kết tủa
Đọc tiếp
Hòa tan hết 4,68 g hỗn họp 2 muối ACO3 và BCO3 bằng dung dịch H2SO4 loangx , sau phản ứng thu được 1 dung dịch X và 1,12 lít CO2 ở đktc .
a.Tính tổng khôi lượng các muối tạo thành trong dung dịch X.
b.Tìm các kim loại A,B và tính thành phần phần trăm theo khối lượng của muối trong hỗn hợp đầu, biết nACO:nBCO3=2:3, MA:MB=3:5.
c. Cho toàn bộ lượng khí CO2 thu được ở trên hấp thụ vào 200 ml dung dịch Ba(OH)2. Tính nồng độ mol của dung dịch Ba(OH)2 để thu được 1,97 g kết tủa
a)
Do A và B đều là kim loại hóa trị II nên ta sử dụng phương pháp trung bình coi A và B là một chất gọi là X
=> CT chung của 2 muối là XCO3
Ta có nCO2 = \(\dfrac{1,12}{22,4}\) = 0,05 ( mol )
XCO3 + H2SO4 → XSO4 + H2O + CO2
0,05 <---- 0,05 <---0,05 <-- 0,05 < -0,05
bảo toàn khối lượng ta có
mXSO4 = mXCO3 + mH2SO4 - mH2O - mCO2
= 4,68 + ( 98 . 0,05 ) - ( 18 . 0,05 ) - ( 44 . 0,05 )
= 6,48 ( gam )
Đúng 0
Bình luận (0)
b) MXCO3 = mXCO3 : nXCO3 = 4,68 : 0,05 = 93,6
=> X = 93,6 - 12 - 16 . 3 = 33,6
có nACO3 : nBCO3 = 2 : 3
và nACO3 + nBCO3 = 0,05
=> nACO3 = 0,02 và nBCO3 = 0,03
=> nA = 0,02 và nB = 0,03
=> ( 0,02 . A + 5 : 3 . 0,03 . B) / 0,05 = 33,6
=> A = 24 ( là magie - Mg ) do B = A . 5 :3
=> B = 40 ( là canxi - Ca )
=> mMgCO3 = 1,68 ( gam )
=> %mMgCO3 = \(\dfrac{1,68}{4,68}\) . 100 \(\approx\) 36 %
=> %mCaCO3 = 100 - 36 = 64%
Đúng 1
Bình luận (0)
c) nCO2 = 0,05 ( mol )
Do tạo kết tủa nên có 2 trường hợp
=> tạo 2 muối : trung hòa và axit
2CO2 + Ba(OH)2 -------> Ba(HCO3)2
0,04 --> 0,02
CO2 + Ba(OH)2 --------> BaCO3 + H2O
0,01 <--- 0,01 <------- 0,01
=> nBa(OH)2 = 0,03
=> CM = n : V = 0,03 : 0,2 = 0,15 M
Đúng 0
Bình luận (0)
Cho 22,4 lít hỗn hợp A gồm hai khí CO, CO2 đi qua than nóng đỏ (không có mặt không khí) thu được khí B có thể tích hơn thể tích A là 5,6 lít (thể tích khí đo được ở đktc). Dẫn B đi qua dung dịch Ca(OH)2 vừa đủ thì thu được dung dịch chỉ chứa 20,25 g Ca(HCO3)2. Thành phần phần trăm (về thể tích) của mỗi khí trong hỗn hợp lần lượt là A. 25% và 75% B. 37,5% và 62,5% C. 40% và 60% D. 50% và 50%
Đọc tiếp
Cho 22,4 lít hỗn hợp A gồm hai khí CO, CO2 đi qua than nóng đỏ (không có mặt không khí) thu được khí B có thể tích hơn thể tích A là 5,6 lít (thể tích khí đo được ở đktc). Dẫn B đi qua dung dịch Ca(OH)2 vừa đủ thì thu được dung dịch chỉ chứa 20,25 g Ca(HCO3)2. Thành phần phần trăm (về thể tích) của mỗi khí trong hỗn hợp lần lượt là
A. 25% và 75%
B. 37,5% và 62,5%
C. 40% và 60%
D. 50% và 50%
Tóm tắt:
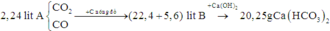
Quan sát – định hướng: Khi cho A qua than nóng đỏ thì chỉ có CO2 tham gia phản ứng tạo CO. Vậy thể tích tăng là do chính phản ứng này tạo ra lượng khí CO nhiều hơn lượng khí CO2 tham gia phản ứng. Đề không cho là phản ứng hoàn toàn và thêm dữ kiện phản ứng với Ca(OH)2.
Chắc chắn trong B còn một lượng khí CO2 chưa phản ứng. Khi cho B qua Ca(OH)2 thì chỉ có CO2 phản ứng được với Ca(OH)2. Qua 2 lần phản ứng đều chỉ có CO2 tham gia phản ứng và qua 2 lần thì CO2 hết.
Từ đó hoàn toàn có thể tính được số mol của CO2.
Ta có phương trình phản ứng:
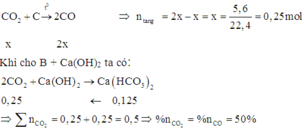
Đáp án D
Đúng 0
Bình luận (0)