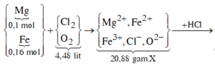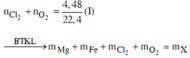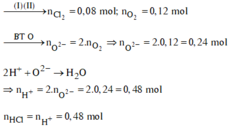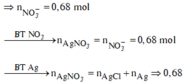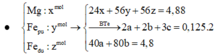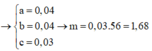16. Trộn đều hỗn hợp gồm CuO và một oxit của Fe với lượng C dư. Phản ứng kết thúc thu được 2,8 lít khí và 12 gam hỗn hợp 2 kim loại. Xác định công thức Oxit Fe biết số mol của CuO và oxit Fe=2:1

Những câu hỏi liên quan
trộn đều hỗn hợp gồm cuo và một oxit sắt với lượng cacbon dư khi phản ứng kết thúc thu được 2,8(l)co2 và 12g hỗn hợp hai kim loại . Xác định công thức hóa học của oxit sắt biết tỉ số mol cuo : số mol fe =2:1
Bài 2: Cho hỗn hợp 2 kim loại Na và Fe vào một lượng H2O (lấy dư), sau khi kết thúc phản ứng thu được 160 gam dung dịch A và một lượng khí phản ứng vừa đủ với 40 (g) bột Đồng (II) oxit (CuO) ở nhiệt độ cao. Tính Nồng độ phần trăm của dung dịch A
1) 2Na+2H2O → 2NaOH+H2
2) H2+CuOto→ Cu+H2O
Có nCuO=\(\dfrac{40}{80}\)=0,5 mol
Dựa vào PTHH 2) nH2=nCuO=0,5mol
Dựa vào PTHH 1) nNaOH=2nH2=0,5.2=1moll
Vậy mNaOH=1.40=40
→C%NaOH=\(\dfrac{40}{160}\).100%=25%
Đúng 2
Bình luận (0)
Bài 2:
Cho hỗn hợp 2 KL Na và Fe vào H2O dư thì chỉ có Na pư
2Na + 2H2O → 2NaOH + H2
1 <----- 0,5
H2 + CuO ---> Cu + H2O
0,5 <-- 0,5
mNaOH = 1 × 40 = 40 g
=> C% NaOH = mct/ mdd ×100
= 40/160×100 = 25%
Đúng 1
Bình luận (0)
Cho hỗn hợp 2 kim loại Na và Fe vào một lượng H2O (lấy dư), sau khi kết thúc phản ứng thu được 160 gam dung dịch A và một lượng khí phản ứng vừa đủ với 40 (g) bột Đồng (II) oxit (CuO) ở nhiệt độ cao.Tính Nồng độ phần trăm của dung dịch A
- Cho hỗn hợp 2 KL Na và Fe vào H2O dư thì chỉ có Na dư
2Na + 2H2O ---> 2NaOH + H2
1 <----- 0,5
H2 + CuO ---> Cu + H2O
0,5 <-- 0,5
- m NaOH = 1 × 40 = 40 g
=> C% NaOH = mct/ mdd ×100
= 40/160×100 = 25%
Đúng 3
Bình luận (0)
Khí sinh ra : H2
\(CuO + H_2 \xrightarrow{t^o} Cu + H_2O\)
Theo PTHH : \(n_{H_2} = n_{CuO} = \dfrac{40}{80} = 0,5(mol)\\\)
\(2Na + 2H_2O \to 2NaOH + H_2\)
Ta có :
\(n_{NaOH} = 2n_{H_2} = 0,5.2 = 1(mol)\\ \Rightarrow C\%_{NaOH} = \dfrac{1.40}{160}.100\%=25\%\)
Đúng 2
Bình luận (0)
a) Cho 29,6 gam hỗn hợp gồm Cu và Fe tác dụng với oxi không khí, sau phản ứng thu được 39,2 gam hỗn hợp A gồm ( CuO, FeO, Fe2O3 và Fe3O4). Hòa tan hoàn toàn A trong dung dịch H2SO4 loãng, dư. --Tính số mol H2SO4 đã tham gia phản ứng -- Tính khối lượng muối sunfat thu được.b) Khử hoàn toàn 2,552 gam một oxit kim loại cần 985,6 ml H2(đktc), lấy toàn bộ lượng kim loại thoát ra cho vào dung dịch HCl dư thu được 739,2 ml H2(đktc).---Xác định công thức của oxit kim loại đã dùng?
Đọc tiếp
a) Cho 29,6 gam hỗn hợp gồm Cu và Fe tác dụng với oxi không khí, sau phản ứng thu được 39,2 gam hỗn hợp A gồm ( CuO, FeO, Fe2O3 và Fe3O4). Hòa tan hoàn toàn A trong dung dịch H2SO4 loãng, dư.
--Tính số mol H2SO4 đã tham gia phản ứng
-- Tính khối lượng muối sunfat thu được.
b) Khử hoàn toàn 2,552 gam một oxit kim loại cần 985,6 ml H2(đktc), lấy toàn bộ lượng kim loại thoát ra cho vào dung dịch HCl dư thu được 739,2 ml H2(đktc).
---Xác định công thức của oxit kim loại đã dùng?
1.a. Sơ đồ các quá trình phản ứng
Kim loại + Oxi \(\rightarrow\) (hỗn hợp oxit ) + axit \(\rightarrow\) muối + H2O
Từ quá trình trên => số mol H2SO4 phản ứng = số mol oxi trong oxit
Theo bài ta có: moxi = 39,2 – 29,6 = 9,6(g)
=> \(n_O=\frac{9,6}{16}=0,6mol\)
=> số mol H2SO4 phản ứng = 0,6 (mol)
b. Khối lượng muối = khối lượng kim loại + khối lượng gốc sunfat
=> mm = 29,6 + 96. 0,6 = 87,2 (g)
2. Gọi công thức của oxit cần tìm là MxOy
Phương trình phản ứng.
MxOy + yH2 \(\rightarrow\) xM + yH2O (1)
\(n_{H_2}=\frac{985,6}{22,4.1000}=0,044\left(mol\right)\)
Theo định luật bảo toàn khối lượng
=> khối lượng kim loại = 2,552 + 0,044.2 – 0,044.18 = 1,848(g)
Khi M phản ứng với HCl
2M + 2nHCl \(\rightarrow\) 2MCln + nH2 (2)
\(n_{H_2}=\frac{739,2}{22,4.1000}=0,033\left(mol\right)\)
(2) => \(\frac{1,848}{M}.n=2.0,033\)
=> M = 28n
Với n là hóa trị của kim loại M
Chỉ có n = 2 với M = 56 (Fe) là thỏa mãn
Theo (1) \(\frac{x}{y}=\frac{n_M}{n_{H_2}}=\frac{0,033}{0,044}=\frac{3}{4}\)
=> oxit cần tìm là Fe3O4
Đúng 0
Bình luận (0)
1.a. Sơ đồ các quá trình phản ứng
Kim loại + Oxi ![]() (hỗn hợp oxit ) + axit
(hỗn hợp oxit ) + axit ![]() muối + H2O
muối + H2O
Từ quá trình trên => số mol H2SO4 phản ứng = số mol oxi trong oxit
Theo bài ta có: moxi = 39,2 – 29,6 = 9,6(g)
=> ![]()
=> số mol H2SO4 phản ứng = 0,6 (mol)
b. Khối lượng muối = khối lượng kim loại + khối lượng gốc sunfat
=> mm = 29,6 + 96. 0,6 = 87,2 (g)
2. Gọi công thức của oxit cần tìm là MxOy
Phương trình phản ứng.
MxOy + yH2 ![]() xM + yH2O (1)
xM + yH2O (1)
![]()
Theo định luật bảo toàn khối lượng
=> khối lượng kim loại = 2,552 + 0,044.2 – 0,044.18 = 1,848(g)
Khi M phản ứng với HCl
2M + 2nHCl ![]() 2MCln + nH2 (2)
2MCln + nH2 (2)
![]()
(2) => ![]()
=> M = 28n
Với n là hóa trị của kim loại M
Chỉ có n = 2 với M = 56 (Fe) là thỏa mãn
Theo (1) ![]()
=> oxit cần tìm là Fe3O4
Đúng 0
Bình luận (0)
ta có VH2 = 985,6ml=0,9856l
VH2 sau phản ứng= 739,2ml=0,7392l
Trong phản ứng ta thấy cứ mỗi mol H2 tác dụng vs 1 mol O tạo thành H2o nên số mol O=H2
no=nh2=V:22,4= 0,9856:22,4=0,044 mol
=> m0=n.M=0,044.16=0,704g
mR=2,552-0,704=1,848g
gọi a là hóa tri kim loại R
2R+2aHCl => 2RCla+aH2
2 2a 2 a
0,066:a 0,033
nH2=V:22,4=0,7392:22,4=0,033
từ pt => n R=0,066:a
mặt khác có mR=1,848g
<=> 1,848=0,066:a.R
<=>28a=R
vì R là kim loại nên a nhân giá trị 1,2,3
ta nhân a=2 =>R=56
vậy R là Fe
gọi cthh của R là FexOy
ta có
nFe=x=m:M=1,848:56x=0,033 mol(1)
nO=y=m:M=0,704:16y=0,044(2)
x:y=(1):(2)=0,033:0,044=3:4
vây cthh là Fe3O4
bạn xem kĩ nha
Đúng 0
Bình luận (0)
Cho 9,6g hỗn hợp A gồm Mg và Fe tác dungkk vừa đủ với 2,8 lít khí õi. Sau khi phản ứng xảy ra hoàn toàn thu được hỗn hợp gồm 2 oxit là MgO và Fe3O4.
a. Tính khối lượng của từng kim loại trong hỗn hợp ban đầu
b. Tính khối lượng của hỗ hợp oxit thu được
\(a) n_{Mg} = a(mol) ; n_{Fe} = b(mol)\\ \Rightarrow 24a + 56b = 9,6(1)\\ 2Mg + O_2 \xrightarrow{t^o} 2MgO\\ 3Fe + 2O_2 \xrightarrow{t^o} Fe_3O_4\\ n_{O_2} = 0,5a + \dfrac{2}{3}b = \dfrac{2,8}{22,4} = 0,125(2)\\ (1)(2)\Rightarrow a = 0,05 ; b = 0,15\\ m_{Mg} = 0,05.24 = 1,2(gam) ; m_{Fe} = 0,15.56 = 8,4(gam)\\ b) m_{oxit} = m_A + m_{O_2} = 9,6 + 0,125.32 = 13,6(gam)\)
Đúng 2
Bình luận (0)
cho 15,6 gam hỗn hợp X gồm Cuo và một oxit sắt tác dụng với khí hidro(dư) đun nóng,kết thúc thu được hai kim loại.cho hai kim loại vào dung dịch HCl dư,kết thúc thu được 3,36 lít khí H2 và có 3,6 gam chất rắn.Tìm công thức oxit sắt đã dùng.
3,6 gam chất rắn không tan là Cu
\(n_{CuO} = n_{Cu} = \dfrac{3,6}{64}= 0,05625(mol)\\ Fe + 2HCl \to FeCl_2 + H_2\\ n_{Fe} = n_{H_2} =\dfrac{3,36}{22,4}= 0,15(mol)\\ m_X = m_{CuO} + m_{oxit\ sắt} \Rightarrow m_{oxit\ sắt} =15,6 -0,05625.80 = 11,1(gam)\\ m_{Oxit\ sắt} = m_{Fe} + m_{O(trong\ oxit\ sắt)}\\ Rightarrow n_O = \dfrac{11,1-0,15.56}{16} = 0,16875(mol)\\ \dfrac{n_{Fe}}{n_O} = \dfrac{0,15}{0,16875} = \dfrac{8}{9}\)
(Sai đề)
Đúng 0
Bình luận (0)
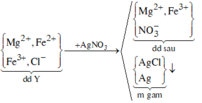
Đốt cháy hỗn hợp gồm 0,10 mol Mg và 0,16 mol Fe trong 4,48 lít (đktc) hỗn hợp khí gồm Cl2 và O2, thu được 20,88 gam hỗn hợp rắn X gồm các muối và oxit của kim loại (không thấy khí thoát ra). Hòa tan X trong dung dịch HCl loãng, thu được dung dịch Y chỉ chứa các muối. Cho dung dịch AgNO3 dư vào Y, kết thúc phản ứng thu được Y, kết thúc phản ứng thu được m gam kết tủa. Giá trị của m là: A. 98,32. B. 96,16. C. 91,84. D. 94,00.
Đọc tiếp
Đốt cháy hỗn hợp gồm 0,10 mol Mg và 0,16 mol Fe trong 4,48 lít (đktc) hỗn hợp khí gồm Cl2 và O2, thu được 20,88 gam hỗn hợp rắn X gồm các muối và oxit của kim loại (không thấy khí thoát ra). Hòa tan X trong dung dịch HCl loãng, thu được dung dịch Y chỉ chứa các muối. Cho dung dịch AgNO3 dư vào Y, kết thúc phản ứng thu được Y, kết thúc phản ứng thu được m gam kết tủa. Giá trị của m là:
A. 98,32.
B. 96,16.
C. 91,84.
D. 94,00.
Bài 1:dẫn H2 đến dư đi qua 19,06g hỗn hợp Fe2O3, Al2O3, CuO cho đến khi phản ứng xảy ra hoàn toàn. Sau phản ứng thu được 15,06g chất rắn. Mặt kahcs 0,54 mol hỗn hợp X tác dụng vừa đủ với 800ml dung dịch HCl 2,55M. Tính % số mol các chất trogn hỗn hợpBài 2: Cho dòng khí CO dư đi qua hỗn hợp gồm CuO và một oxit cảu kim loại R đến phản ứng hoàn toàn thu được 29,6g hỗn hợp rắn A và khí B Cho B vào dung dịch Ca(OH)2 dư được 65g kết tủa. Mặt khác cho A vào dung dịch HCl dư thoát ra 6,72 l khí ở đktc...
Đọc tiếp
Bài 1:dẫn H2 đến dư đi qua 19,06g hỗn hợp Fe2O3, Al2O3, CuO cho đến khi phản ứng xảy ra hoàn toàn. Sau phản ứng thu được 15,06g chất rắn. Mặt kahcs 0,54 mol hỗn hợp X tác dụng vừa đủ với 800ml dung dịch HCl 2,55M. Tính % số mol các chất trogn hỗn hợp
Bài 2: Cho dòng khí CO dư đi qua hỗn hợp gồm CuO và một oxit cảu kim loại R đến phản ứng hoàn toàn thu được 29,6g hỗn hợp rắn A và khí B Cho B vào dung dịch Ca(OH)2 dư được 65g kết tủa. Mặt khác cho A vào dung dịch HCl dư thoát ra 6,72 l khí ở đktc. Xác định công thức của oxit. Biết Cu ko tan trogn dd HCl và tỉ lệ mol của Cu và R là 2:3
Bài 3:Cho 39,1g hh gồm K và Ba vòa nước sau khi kết thúc phản ứng thu được chất rắn Y và 3,36 lít khí đktc Cho nước dư vào Y được dung dịch Z và 4,48 lít khí thoát ra. Hấp thự hoàn toàn V lít SO2 đktc vào Z được 43,4 g kết tủa. Tính khối lượng mỗi chất trogn X và tính V.
P/S: Mong mọi người giúp đỡ nhanh nhanh ạ!!!!
Cho 4,88 gam hỗn hợp Mg và Fe vào dung dịch gồm AgNO3 và Cu(NO3)2, thu được chất rắn X gồm ba kim loại và dung dịch Y gồm hai muối. Đun nóng X với dung dịch H2SO4 đặc, dư thu được 2,8 lít khí SO2 (đktc). Cho dung dịch NaOH dư vào Y, lọc lấy kết tủa rồi nung trong không khí, thu được 4,8 gam oxit. Giả thiết các phản ứng xảy ra hoàn toàn. Khối lượng của Fe trong X là: A. 1,68 gam. B. 2,80 gam. C. 1,12 gam. D. 2,24 gam.
Đọc tiếp
Cho 4,88 gam hỗn hợp Mg và Fe vào dung dịch gồm AgNO3 và Cu(NO3)2, thu được chất rắn X gồm ba kim loại và dung dịch Y gồm hai muối. Đun nóng X với dung dịch H2SO4 đặc, dư thu được 2,8 lít khí SO2 (đktc). Cho dung dịch NaOH dư vào Y, lọc lấy kết tủa rồi nung trong không khí, thu được 4,8 gam oxit. Giả thiết các phản ứng xảy ra hoàn toàn. Khối lượng của Fe trong X là:
A. 1,68 gam.
B. 2,80 gam.
C. 1,12 gam.
D. 2,24 gam.