Cho m gam một kim loại A hóa trị I vào nước.Sau phản ứng thu được dung dịch bazo có khối lượng 8 g trong đó khối lượng kim loại chiếm 57,5%
a)Xác định kim loại A
b)Tính m
đun nóng m gam kim loại M có hóa trị không đổi trong không khí đến khi phản ứng xảy ra hoàn toàn thì thu được oxit có khối lượng 1,25m gam .Để hòa tan hết lượng oxit trên cần 200 g dung dịch H2SO4 19,6% thu được dung dịch X .Xác định kim loại M .Tính nồng độ phần trăm C% của chất tan có trong dung dịch X
Gọi n là hóa trị của M
Phản ứng xảy ra:
4M+nO2→2M2On
Giả sử số mol M là 1 mol.
→nM2On=1/2nM=0,5 mol
→mM=m=1M(M)=M(M)gam
mM2On=0,5.(2MM+16MO)=0,5(2MM+16n)=MM+8n=1,25m
→MM+8n=1,25MM→MM=32n→n=2→MM=64→M:Cu(Đồng)
Hòa tan oxit
CuO+H2SO4→CuSO4+H2O
Ta có:
mH2SO4=200.19,6%=39,2 gam
→nH2SO4=39,298=0,4 mol = nCuO=nCuSO4
→mCuO=0,4.(64+16)=32 gam;mCuSO4=0,4.(64+96)=64 gam
Áp dụng định luật bảo toàn khối lượng:
mddX=mCuO+mddH2SO4=200+32=232 gam
→C%CuSO4=64232=27,5862%
chúc bạn học tốt
Gọi n là hóa trị của M Phản ứng xảy ra: 4M+nO2→2M2On
Giả sử số mol M là 1 mol.
→nM2On=1/2nM=0,5 mol →mM=m=1M(M)=M(M)gam
mM2On=0,5.(2MM+16MO)=0,5(2MM+16n)=MM+8n=1,25m →MM+8n=1,25MM→MM=32n→n=2→MM=64→M:Cu(Đồng)
Hòa tan 1,08 gam kim loại M có hóa trị III vào dung dịch H2SO4 vừa đủ thu được 1,344 lít H2 (đktc) và chất M2(SO4)3.
a/ Viết PTHH.
b/ Xác định kim loại M.
c/ Tính khối lượng H2SO4 đã phản ứng.
nH2 = 1,344 : 22,4 = 0,06(mol)
pthh 2M+ 3H2SO4 ---> M2(SO4)3+ 3H2
0,04<-- 0,06---------------------------0,06(mol)
M M = 1,08 : 0,04 = 27 (g/mol )
=> M : Al
mH2SO4 = 0,06.98 =5,88 (g)
nH2 = 1,344/22,4 = 0,06 (mol)
PTHH:
2M + 3H2SO4 -> Al2(SO4)3 + 3H2
0,04 <--- 0,06 <--- 0,02 <--- 0,06
M(M) = 1,08/0,04 = 27 (g/mol(
=> M là Al
mH2SO4 = 0,06 . 98 = 5,88 (g)
Cho 17 g oxit kim loại a nhóm hóa trị 3 vào dung dịch H2 SO4 vừa đủ thu được 57 g muối xác định kim loại a ra tính khối lượng dung dịch H2 SO4 10% đã dùng - cho 0,72 g một kim loại m hóa trị 2 tác dụng hết với dung dịch H2 SO4 dư thì thu được 672 ml khí H2 điều kiện chuẩn xác định tên kim loại đó - hòa tan hoàn toàn toàn phẩy 85 gam một kim loại kiềm thổ r bằng 200 ml dung dịch HCl Ơ hay nếu trung hòa lượng axit đó cần 100 ml dung dịch NaOH 3 3 xác định tên kim loại trên. - cho 0,88 g hỗn hợp hai kim loại x y nhóm 2A Ở hai chu kì liên tiếp tác dụng với dung dịch H2 SO4 loãng thu được 672 ml khí điều kiện tiêu chuẩn và m gam muối khan. Xác định hai kim loại x y , Tính m gam muối khan thu được - Cho 11,2 g hỗn hợp 2 kim loại kiềm a b ở hai chu kì liên tiếp vào dung dịch 200ml H2O thu được 4,48 lít khí điều kiện tiêu chuẩn và dung dịch E . Xác định AB . Tính C phần trăm các chất trong dung dịch E. Để trung hòa dung dịch E trên cần bao nhiêu ml dung dịch H2 SO4 1M
Nhúng một thanh kim loại M hóa trị II vào dung dịch CuSO4 dư. Sau phản ứng, khối lượng thanh kim loại giảm 0,24 gam. Cũng thanh kim loại đó nếu nhúng vào dung dịch AgNO3 dư thì khi phản ứng xong khối lượng thanh kim loại tăng 0,52 gam. Giả sử số mol kim loại M tác dụng ở hai phản ứng là như nhau. Xác định kim loại M đã dùng.
khối lượng thanh kim loại giảm -> nguyển tử khối của KL phải lớn hơn Cu và đứng trước Cu trong dãy điện hóa
khối lượng thanh kim loại tăng -> nguyển tử khối của KL phải nhỏ hơn Ag
=> KL cần tìm là Zn
Cho m gam bột kim loại R hóa trị 2 vào dung dịch CuSO4 dư. Sau phản ứng hoàn toàn, khối lượng chất rắn thu được giảm 0,24 gam so với khối lượng chất rắn ban đầu. Cũng cho m gam bột kim loại trên vào dung dịch AgNO3 dư, đến khi phản ứng hoàn toàn, khối lượng chất rắn thu được tăng 0,52 gam so với khối lượng chất rắn ban đầu. Kim loại R là
A. Sn
B. Cd
C. Zn
D. Pb
Cho 12,8 gam kim loại A hóa trị II phản ứng hoàn toàn với khí Cl2 thu muối B. Hòa tan B vào nước thu được 400ml dung dịch C. Nhúng thanh sắt nặng 11,2 gam vào dung dịch C, sau một thời gian thấy kim loại A bám vào thanh sắt và khối lượng thanh sắt là 12,0 gam, nồng độ FeCl2 trong dung dịch là 0,25M. Xác định kim loại A và nồng độ mol của kim loại B trong dung dịch C.
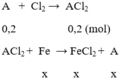
số mol FeCl2 là n = 0,25 . 0,4 = 0,1 (mol)
gọi x là số mol Fe phản ứng
khối lượng kim loại tăng là Δm = mA - mFe = Ax – 56x = 0,8
x = 0,1 → A.0,1 – 56.0,1 = 0,8 → A = 64. A là Cu
số mol Cu là nCu = 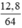 = 0,2 (mol)
= 0,2 (mol)
số mol CuCl2 → n(CuCl2) = nCu = 0,2 (mol)
nồng độ mol/l CuCl2 là C(M(CuCl2)) = 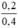 = 0,5M
= 0,5M
PTHH: \(2A+3Cl_2\underrightarrow{t^o}2ACl_3\)
a) Bảo toàn khối lượng: \(m_{Cl_2}=m_{ACl_3}-m_A=21,3\left(g\right)\)
\(\Rightarrow n_{Cl_2}=\dfrac{21,3}{71}=0,3\left(mol\right)\) \(\Rightarrow n_A=0,2mol\)
\(\Rightarrow M_A=\dfrac{5,4}{0,2}=27\) \(\Rightarrow\) A là Nhôm
b) PTHH: \(Al+3AgNO_3\rightarrow Al\left(NO_3\right)_3+3Ag\)
Ta có: \(n_{AgNO_3}=0,3\cdot1,5=0,45\left(mol\right)\)
\(\Rightarrow n_{Al}=0,15mol\) \(\Rightarrow m_{Al}=0,15\cdot27=4,05\left(g\right)\)
Cho 3,64 gam hỗn hợp E gồm một oxit, một hiđroxit và một muối cacbonat trung hòa của một kim loại M có hóa trị II tác dụng vừa đủ với 117,6 gam dung dịch H2SO4 10%. Sau phản ứng, thu được 0,448 lít khí (đktc) và dung dịch muối duy nhất có nồng độ 10,867% (khối lượng riêng là 1,093 gam/ml); nồng độ mol là 0,545M.
a) Viết các phương trình phản ứng xảy ra và xác định kim loại M.
b) Tính % khối lượng của các chất có trong hỗn hợp E.
a) Đặt số mol của MO, M(OH)2, MCO3 tương ứng là x, y, z.
Nếu tạo muối trung hòa ta có các phản ứng:
MO + H2SO4 →MSO4 + H2O (1)
M(OH)2 + H2SO4 →MSO4 + 2H2O (2)
MCO3 + H2SO4 →MSO4 + H2O + CO2 (3)
Nếu tạo muối axít ta có các phản ứng:
MO + 2H2SO4 →M(HSO4)2 + H2O (4)
M(OH)2 + 2H2SO4 →M(HSO4)2 + 2H2O (5)
MCO3 + 2H2SO4 →M(HSO4)2 + H2O + CO2 (6)
Ta có :
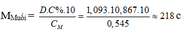
– TH1: Nếu muối là MSO4 M + 96 = 218 M = 122 (loại)
– TH2: Nếu là muối M(HSO4)2 M + 97.2 = 218 M = 24 (Mg)
Vậy xảy ra phản ứng (4, 5, 6) tạo muối Mg(HSO4)2
b) Theo (4, 5, 6) Số mol CO2 = 0,448/22,4 = 0,02 molz = 0,02 (I)
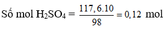
2x + 2y + 2z = 0,12 (II)
Đề bài: 40x + 58y + 84z = 3,64 (III)
Giải hệ (I, II, III): x = 0,02; y = 0,02; z = 0,02
%MgO = 40.0,02.100/3,64 = 21,98%
%Mg(OH)2 = 58.0,02.100/3,64 = 31,87%
%MgCO3 = 84.0,02.100/3,64 = 46,15%
hòa tan hoàn toàn 8,6 gam hỗn hợp kim loại có hóa trị I và oxit của nó vào nước được dung dịch A. Cô cạn dung dịch A và thu được 11,2 gam hidroxit khan
a) Xác định kim loại hóa trị I
b) Tính khối lượng mỗi chất trong hỗn hợp ban đầu