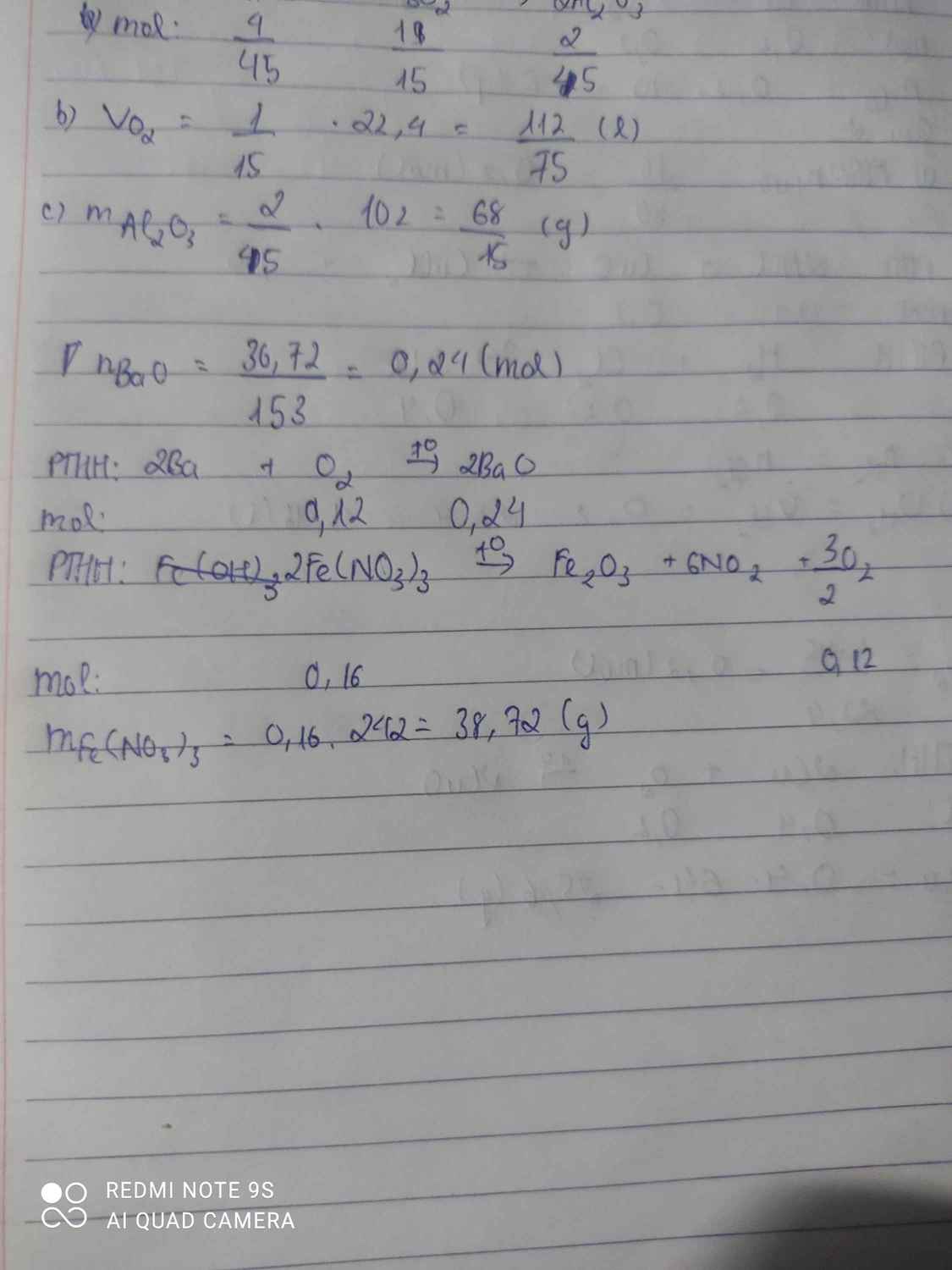cần dùng bao nhiêu gam KClO3 để điều chế ra lượng O2 tác dụng vừa hết với 6,2 p?

Những câu hỏi liên quan
Bài 4. Nung nóng KMnO4 để điều chế 6,72 lít O2 (ở đktc).a. Tính khối lượng thuốc tím cần dùng?b. Cần dùng bao nhiêu gam KClO3 để điều chế cũng với một thể tích khí O2 trên?c. Nếu cho lượng khí O2 trên tác dụng hết với Cu. Hỏi sau phản ứng thu được bao nhiêu gam đồng (II) oxit.Bài 5. Cho 16 gam đồng (II) oxit phản ứng hết V lít khí hidro H2 (đktc) ở nhiệt độ thích hợp, sau phản ứng thu được Cu và H2O. Biết phản ứng xảy ra vừa đủ. a/ Tính giá trị V./ b/ Tính khối lượn...
Đọc tiếp
Bài 4. Nung nóng KMnO4 để điều chế 6,72 lít O2 (ở đktc).
a. Tính khối lượng thuốc tím cần dùng?
b. Cần dùng bao nhiêu gam KClO3 để điều chế cũng với một thể tích khí O2 trên?
c. Nếu cho lượng khí O2 trên tác dụng hết với Cu. Hỏi sau phản ứng thu được bao nhiêu gam đồng (II) oxit.
Bài 5. Cho 16 gam đồng (II) oxit phản ứng hết V lít khí hidro H2 (đktc) ở nhiệt độ thích hợp, sau phản ứng thu được Cu và H2O. Biết phản ứng xảy ra vừa đủ. a/ Tính giá trị V./ b/ Tính khối lượng Cu thu được sau phản ứng.
Bài 6. Cho11,6 gam oxit sắt từ Fe3O4 phản ứng hết V lít khí hidro H2 (đktc) ở nhiệt độ thích hợp, sau phản ứng thu được Fe và H2O. Biết phản ứng xảy ra vừa đủ. a/ Tính giá trị V. b/ Tính khối lượng Fe thu được sau phản ứng.
Bài 7. Người ta dùng H2 (dư) tác dụng hết với x gam Fe2O3 nung nóng thu được y gam Fe. Cho lượng sắt này tác dụng với dung dịch H2SO4 loãng dư thì thu được 6,72 lít khí H2 (đktc). Tính giá trị x và y.
Bài 8. Cho 3,6 gam magie phản ứng hoàn toàn với dung dịch axit sunfuric loãng (H2SO4)
a.Viết phương trình phản ứng xảy ra và tính thể tích hidro thu được ở đktc.
b. Cho lượng khí H2 thu được tác dụng hết với CuO. Hỏi sau phản ứng thu được bao nhiêu gam Cu?
Bài 9. Cho 3,6 gam magie trên vào dung dịch chứa 14,6 gam axit clohidric (HCl)a. Hỏi sau phản ứng chất nào còn dư, dư bao nhiêu gam?b. Tính thể tích H2 (đktc)?
Bài 4. 2\(KMnO_4\) ---> \(K_2MnO_4\) + \(MnO_2\) + \(O_2\) (Lập và cân bằng phương trình)
0,6 mol 0,3 mol 0,3 mol 0,3 mol
a. + Số mol của \(O_2\)
\(n_{O_2}\) = \(\dfrac{V}{22,4}\) = \(\dfrac{6,72}{22,4}\) = 0,3 (mol)
+ Khối lượng của \(KMnO_4\) (thuốc tím) cần dùng:
\(m_{KMnO_4}\) = n . M = 0,6 . 158 = 94,8 (g)
b. 2\(KClO_3\) ---> 2\(KCl\) + 3\(O_2\) (Lập và cân bằng phương trình)
0,2 mol 0,2 mol 0,3 mol
Số g \(KClO_3\) dùng để điều chế:
\(m_{KClO_3}\) = n . M = 0,2 . 122,5 = 24,5 (g)
c. 2Cu + \(O_2\) ---> 2\(CuO\) (Lập và cân bằng phương trình)
0,6 mol 0,3 mol 0,6 mol
Số g của CuO sau phản ứng thu được:
\(m_{CuO}\) = n . M = 0,6 . 80 = 48 (g)
________________________________________
Bài 4 trước nha bạn, có gì sai thì nhắn mình :))
Đúng 1
Bình luận (0)
Bài 5. CuO + \(H_2\) ---> Cu + \(H_2O\) (Lập và cân bằng phương trình)
0,2 mol 0,2 mol 0,2 mol 0,2 mol
a. + Số mol của CuO:
\(n_{CuO}\) = \(\dfrac{m}{M}\) = \(\dfrac{16}{80}\) = 0,2 (mol)
+ Thể tích của \(H_2\)
\(V_{H_2}\) = n . 22,4 = 0,2 . 22,4 = 4,48 (lít)
b. Khối lượng Cu sau phản ứng:
\(m_{Cu}\) = n . M = 0,2 . 64 = 12,8 (g)
______________________________
Bài 5 nha, sai thì nhắn mình :))
Đúng 0
Bình luận (0)
Bài 6. \(Fe_3O_4\) + 4\(H_2\) ---> 3Fe + 4\(H_2O\) (Lập và cân bằng phương trình)
0,05 mol 0,2 mol 0,15 mol 0,2 mol
a. + Số mol của \(Fe_3O_4\)
\(n_{Fe_3O_4}\) = \(\dfrac{m}{M}\) = \(\dfrac{11,6}{232}\) = 0,05 (mol)
+ Thể tích của \(H_2\)
\(V_{H_2}\) = n . 22,4 = 0,2 . 22,4 = 4,48 (lít)
b. Khối lượng của Fe thu được sau phản ứng:
\(m_{Fe}\) = n . M = 0,15 . 56 = 8,4 (g)
_________________________________________
Bài 6 này :))
Đúng 1
Bình luận (3)
Xem thêm câu trả lời
Cần bao nhiêu g KClO3 để điều chế ra lượng O2 tác dụng hết với 6,2g photpho
PTHH: (1) 2 KClO3 -to => 2 KCl + 3 O2
(2) 5 O2 +4 P -to => 2 P2O5
Ta có: nP= 6,2/31= 0,2(mol)
=> nO2(1)= nO2(2)= 5/4 . 0,2= 0,25 (mol)
=> nKClO3 = 2/3. 0,25= 1/6 (mol)
=> mKClO3 = 1/6 . 122,5 ≈ 20,417 (g)
Đúng 0
Bình luận (0)
Câu 3. Cho 13g Zinc tác dụng hết với khí Oxygen tạo ra Zinc oxide. a) Viết phương trình hóa học b) Tính khối lượng sản phẩm và thể tích khí O2 cần dùng. c) Tính khối lượng muối KClO3 cần dùng để điều chế lượng O2 trên.
\(n_{Zn}=0,2mol\\ a.2Zn+O_2-^{^{ }t^{^0}}->2ZnO\\ b.m_{ZnO}=0,2.71=14,2g\\ n_{O_2}=0,2:2=0,1mol\\ V_{O_2}=0,1.22,4=2,24L\\ c.2KClO_3-^{^{ }t^{^{ }0}}->2KCl+3O_2\\ n_{KClO_3}=\dfrac{2}{3}.0,1=\dfrac{0,2}{3}mol\\ m_{KClO_3}=122,5\cdot\dfrac{0,2}{3}=8,166g\)
Đúng 3
Bình luận (1)
Cho phản ứng:
F
e
N
O
3
3
−
t
o
→
F
e
2
O
3
+
N
O
2
↑
+
O
2
↑
Cần lấy bao nhiêu gam
F
e
N...
Đọc tiếp
Cho phản ứng:
F e N O 3 3 − t o → F e 2 O 3 + N O 2 ↑ + O 2 ↑
Cần lấy bao nhiêu gam F e N O 3 3 để điều chế lượng oxi tác dụng vừa đủ với bari tạo thành 36,72 gam oxit?
Trong không khí photpho tác dụng với O2 tạo ra P2O5 a. Từ 6,2 g photpho có thể tạo thành tối đa bao nhiêu gam P2O5 b. Để thu được 35,5 gam P2O5 cần dùng bao nhiêu gam P và bao nhiêu lít O2 (ở 25C, 1 bar)
\(a.n_P=\dfrac{6,2}{31}=0,2mol\\ 4P+5O_2\xrightarrow[]{t^0}2P_2O_5\)
\(n_{P_2O_5}=0,2.2:4=0,1mol\\ m_{P_2O_5}=0,1.142=14,2g\)
\(b.n_{P_2O_5}=\dfrac{35,5}{142}=0,25mol\\ n_P=0,25.2=0,5mol\\ m_P=0,5.31=15,5g\\ n_{O_2}=\dfrac{0,25.5}{2}=0,625mol\\ V_{O_2}=0,625.24,79=15,49375l\)
Đúng 2
Bình luận (0)
1: muốn điều chế đc 256 gam khí oxi thì cần phải dùng bao nhiêu gam KMnO4 chứa 5% tạp chất trơ ?2: tính khối lượng NaCO3 cần dùng để điều chế ra được lượng oxi tác dụng vừa đủ với 1,0 kgvthanđá ( chứa 10% tạp chất trơ)3: Tính khổi lượng KNO3 cần dùng để điều chế được 24,24 gam O2 . biết hiệu suất cần phản ứng đạt 90%( MN GIÚP ĐỠ MK NHANH NHA. MK CẦN GẤP )
Đọc tiếp
1: muốn điều chế đc 256 gam khí oxi thì cần phải dùng bao nhiêu gam KMnO4 chứa 5% tạp chất trơ ?
2: tính khối lượng NaCO3 cần dùng để điều chế ra được lượng oxi tác dụng vừa đủ với 1,0 kgvthanđá ( chứa 10% tạp chất trơ)
3: Tính khổi lượng KNO3 cần dùng để điều chế được 24,24 gam O2 . biết hiệu suất cần phản ứng đạt 90%
( MN GIÚP ĐỠ MK NHANH NHA. MK CẦN GẤP )
nung hoàn toàn a gam KClO3 để điều chế O2 cho 3 gam Al tác dụng hết với dung dịch HCl ta được AlCl3 và H2 a lập phương trình hóa học b tính tỉ lệ a / b Nếu khối lượng hai chất bằng nhau. CẦN GẤP
Đề đang lỗi nhiều chổ, bạn cập nhật đầy đủ câu hỏi nha
Đúng 0
Bình luận (0)
Tính khối lượng KMnO4 cần dùng để thu được thể tích khí ở đktc vừa đủ tác dụng với 12 gam Photpho. Nếu ko dùng KMnO4. Nếu ko dùng KMnO4 thì cần bao nhiêu gam KClO3 để thu được thể tích khí đủ dùng cho phản ứng trên?
\(n_P=\dfrac{12}{31}mol\)
\(4P+5O_2\underrightarrow{t^o}2P_2O_5\)
\(\dfrac{12}{21}\)\(\rightarrow\)\(\dfrac{5}{7}\)
Khối lượng \(KMnO_4\) cần dùng để thu lượng khí trên:
\(2KMnO_4\underrightarrow{t^o}K_2MnO_2+MnO_2+O_2\)
\(\dfrac{10}{7}\) \(\leftarrow\) \(\dfrac{5}{7}\)
\(\Rightarrow m_{KMnO_4}=\dfrac{10}{7}\cdot158=225,71g\)
Nếu không dùng \(KMnO_4\) mà dùng \(KClO_3\) để thu được khí đủ dùng trên:
\(2KClO_3\underrightarrow{t^o}2KCl+3O_2\)
\(\dfrac{10}{21}\) \(\leftarrow\) \(\dfrac{5}{7}\)
\(m_{KClO_3}=\dfrac{10}{21}\cdot122,5=58,33g\)
Đúng 2
Bình luận (3)
nP = 12/31 (mol)
PTHH: 4P + 5O2 -> (to) 2P2O5
Mol: 12/31 ---> 15/31
2KMnO4 -> (to) K2MnO4 + MnO2 + O2
nKMnO4 = 15/31 . 2 = 30/31 (mol)
mKMnO4 = 30/31 . 158 = 4740/31 (g)
PTHH: 2KClO3 -> (to, MnO2) 2KCl + 3O2
nKClO3 = 30/31 : 3 . 2 = 15/31 (mol)
mKClO3 = 15/31 . 122,5 = 3675/62 (g)
Đúng 0
Bình luận (0)
cho phản ứng FE(NO3)3--->fe203+no2+o2 lấy bao nhiêu gam FE(NO3)để điều chế lượng oxi tác dụng vừa đủ với bải tạo thành 36,72gam oxit