cho 31,84g hh NaX, NaY ( X và Y là hai halogen) vào dd AgNO3 dư thu đc 57,34g kết tủa. Tìm công thức NaX và NaY

Những câu hỏi liên quan
cho 31,84g hỗn hợp NaX và NaY (X,Y là 2 halogen ở 2 chu kỳ liên tiếp) vào dd AgNO3 dư thu được 57,34g kết tủa .Công thức của 2 muối là
Cho 31,84 gam hỗn hợp NaX và NaY (X, Y là 2 nguyên tố halogen ở 2 chu kì liên tiếp) vào dung dịch AgNO3 dư thì thu được 57,34g kết tủa.Biết cả NaX và NaY đều tạo kết tủa với AgNO3. Công thức của hai muối là A. NaBr và NaI B. NaF và NaCl C. NaCl và NaBr D. NaF, NaBr
Đọc tiếp
Cho 31,84 gam hỗn hợp NaX và NaY (X, Y là 2 nguyên tố halogen ở 2 chu kì liên tiếp) vào dung dịch AgNO3 dư thì thu được 57,34g kết tủa.Biết cả NaX và NaY đều tạo kết tủa với AgNO3. Công thức của hai muối là
A. NaBr và NaI
B. NaF và NaCl
C. NaCl và NaBr
D. NaF, NaBr
Đáp án A.
Hỗn hợp (NaX, NaY) = NaM
NaM + AgNO3 → AgM↓+NaNO3
Ta có
![]() => M = 81,6 => X,Y lần lượt là Br (80) và I (127)
=> M = 81,6 => X,Y lần lượt là Br (80) và I (127)
Đúng 0
Bình luận (0)
Cho 31,84 gam hỗn hợp NaX và NaY (X, Y là 2 nguyên tố halogen ở 2 chu kì liên tiếp) vào dung dịch AgNO3 dư thì thu được 57,34g kết tủa. Công thức của hai muối là A. NaBr và NaI B. NaF và NaCl. C. NaCl và NaBr D. NaF, NaCl hoặc NaBr, NaI
Đọc tiếp
Cho 31,84 gam hỗn hợp NaX và NaY (X, Y là 2 nguyên tố halogen ở 2 chu kì liên tiếp) vào dung dịch AgNO3 dư thì thu được 57,34g kết tủa. Công thức của hai muối là
A. NaBr và NaI
B. NaF và NaCl.
C. NaCl và NaBr
D. NaF, NaCl hoặc NaBr, NaI
TH1: NaF và NaCl
Kết tủa chỉ có AgCl
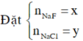
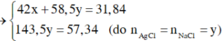
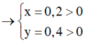
Vậy CT 2 muối có thể là NaF và NaCl
TH2: Hỗn hợp muối không chứa NaF
Đặt CT chung của 2 muối ban đầu là NaX
![]()
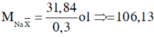
=> 2 muối là NaBr và NaI
Đáp án A
Đúng 0
Bình luận (0)
Cho 31,8g hỗn hợp NaX và NaY ( X, Y là các halogen ở 2 chu kì liên tiếp) vào dung dịch \(AgNO_3\) dư thu được 57,34g kết tủa trắng . Tìm Công thức của NaX; NaY và tính thành phần % của kim loại của mỗi muối
Các pro hóa giúp vs ạ :((
Trường hợp 1:
Cả hai muối đều tác dụng với AgNO3
Gọi công thức chung là NaR
Ta có:nAgR=nNaR
<=>\(\dfrac{57,34}{108+R}\)=\(\dfrac{31,84}{23+R}\)
<=>R=83,13
=>Ta có : Br(80)<R(83,13)<I(127)
Gọi số mol :
-NaBr: xmol
-NaI: y mol
\(\left\{{}\begin{matrix}103x+150y=31,84\\188x+235y=57,34\end{matrix}\right. }\)
<=>\(\left\{{}\begin{matrix}x=0,28\\y=0,02\end{matrix}\right.\)
=>mNaBr=0,28.103=28,84g
=>mNaI=0,02.150=3g
*
Trường hợp 2:
Là có muối NaF và NaCl
nAgCl=nNaCl=\(\dfrac{57,34}{143,5}\)=0,4 mol
mNaCl=0,4.58,5=23,4gmNaCl=0,4.58,5=23,4g
mNaF=31,84−23,4=8,44g
=>Từ 2 trường hợp trên em tính đc % kim loại nhé
Đúng 4
Bình luận (4)
Cho 0,03 mol hỗn hợp NaX và NaY ( X, Y là hai halogen thuộc chu kì kế tiếp – đều tạo kết tủa với AgNO3) tác dụng với lượng dư dung dịch AgNO3 thu được 4,75 gam kết tủa. Công thức hai muối trên là A. NaBr, NaI B. NaF, NaCl C. NaCl, NaBr D. NaF, NaCl hoặc NaBr, NaI
Đọc tiếp
Cho 0,03 mol hỗn hợp NaX và NaY ( X, Y là hai halogen thuộc chu kì kế tiếp – đều tạo kết tủa với AgNO3) tác dụng với lượng dư dung dịch AgNO3 thu được 4,75 gam kết tủa. Công thức hai muối trên là
A. NaBr, NaI
B. NaF, NaCl
C. NaCl, NaBr
D. NaF, NaCl hoặc NaBr, NaI
Đáp án C
Gọi công thức chung của NaX và NaY là NaM.
NaM + AgNO3 → AgM↓+NaNO3
0,03 →0,03 (mol)
![]()
=> M = 50,3 => X,Y lần lượt là Cl và Br
Đúng 0
Bình luận (0)
Cho 3,184g hỗn hợp NaX và NaY (X, Y là 2 nguyên tố halogen ở 2 chu kì liên tiếp; X, Y khác F) vào dung dịch A g N O 3 dư thì thu được 5,734g kết tủa. Công thức của 2 muối là
A. NaBr và NaI.
B. NaCl và NaI.
C. NaCl và NaBr.
D. Không xác định được.
cho 31,84 g hỗn hợp NaX, NaY (X, Y là 2 halogen ở 2 chu kì liên tiếp) vào AgNO3 dư, thu được 57,34g kết tủa. Xác định tên 2 halogen
(Bài này giải như bình thường thôi. Nhưng lưu ý với bạn là nếu có 1 muối là NaF thì muối này ko tạo kết tủa với AgNO3 đâu)
* Trường hợp 1: Ko có muối NaF
Gọi công thức tổng quát chung hai muối là: NaX.
Phương trình hoá học viết được:
NaX + AgNO3 = AgX + NaNO3
(23+X) (108+X) (g)
31,84 57,34
=> X=83,13 => Hai halogen là: Bx và I.
* Trường hợp 2: ! trong hai muối là NaF (giả sử là NaX)
Lúc đó chỉ có NaY phản ứng (chỉ có 3 khả năng: Cl, Br hoặc I thôi nên thử từng khả năng cũng được) => đáp án: Cl
Vậy 2 muối là NaF và NaCl hoặc NaBr và NaI.
Đúng 0
Bình luận (0)
Cho 15,92g hỗn hợp A gồm NaX, NaY(X,Y là hia halogen ở hai chu kì liên tiếp và Mx<My vào nước được dung dịch B. Cho dd B tác dụng với dd AgNO3 dư, thu được 28,67g kết tủa. Tìm công thức NaX,NaY biết mNaX>mNaY
\(NaM+AgNO_3\rightarrow AgM+NaNO_3\)
\(n_{NaM}=n_{AgM}\)
\(\Leftrightarrow\frac{15,92}{23+M_M}=\frac{28,67}{108+M_M}\)
\(\Rightarrow M_M=83,333\)
\(\Rightarrow\) X là Brom(Br) ;Y là Iot(I)
Vậy NaX là NaBr và NaY là NaI
Cho 5,965gam hỗn hợp A gồm: NaX, NaY (X,Y là hai halogen liên tiếp, nguyên tử khối của X < Y) vào dung dịch A g N O 3 dư. Kết thúc phản ứng thu được 1,435gam kết tủa. Xác định hai nguyên tố X, Y.
















