đôt cháy hòan tòan 7,4g éste X cân dùng 7,84l oxi(đktc). CTPT của X là?
Đốt cháy hòan tòan một thể tích khí thiên nhiên gồm metan,etan,propan bằng oxi không khí (trong không khí, oxi chiếm 20% thế tích), thu được 7,84 lít khí CO2 (ở đktc) và 9,9 gam nước. Thế tích không khí (ở đktc) nhỏ nhất cần dùng để đốt cháy hoàn tòan lượng khí thiên nhiên trên 1à (Cho H=1; C=12; O=16)
A. 70,0 lít.
B. 7,84 lít.
C. 84,0 lít.
D. 56,0 lít.
Đáp án A
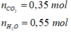
Áp dụng bảo toàn nguyên tố oxi ta có:

Đốt cháy hòan tòan 448ml một hiđrocacbon A , cần dùng vừa đủ 5,6 lít không khí. Sản phẩm cháy cho vào dd Ba(OH)2 dư thu được 7,88 g kết tủa.(Biết các thể tích khí đều đo ở đktc ,oxi chiếm 20% thể tích không khí ).
a. Xác định công thức phân tử của hidrocacbon A.
b. Cho mg hỗn hợp X gồm chất A và C4H6 (biết d hhX / CH4 là 2,675 )đi qua dung dịch Brom dư sau phản ứng có 32 g brom phản ứng. Mặt khác cũng lượng hỗn hợp X trên khi cho qua dung dịch AgNO3/NH3 dư thu được 19,26 g kết tủa. Tính % thể tích và CTCT của từng chất trong X 
a) \(n_A=\dfrac{0,448}{22,4}=0,02\left(mol\right)\)
\(n_{O_2}=\dfrac{\dfrac{5,6}{22,4}.20}{100}=0,05\left(mol\right)\)
\(n_{BaCO_3}=\dfrac{7,88}{197}=0,04\left(mol\right)\)
=> nC = nCO2 = 0,04 (mol)
Số nguyên tử C = \(\dfrac{0,04}{0,02}=2\) (nguyên tử)
Bảo toàn O: \(n_{H_2O}=0,05.2-0,04.2=0,02\left(mol\right)\)
=> nH = 0,04 (mol)
Số nguyên tử H = \(\dfrac{0,04}{0,02}=2\) (nguyên tử)
=> CTPT: C2H2
b)
Gọi \(\left\{{}\begin{matrix}n_{C_2H_2}=a\left(mol\right)\\n_{C_4H_6}=b\left(mol\right)\end{matrix}\right.\)
\(\overline{M}=\dfrac{26a+54b}{a+b}=2,675.16=42,8\left(g/mol\right)\)
=> \(a=\dfrac{2}{3}b\) (1)
\(\left\{{}\begin{matrix}\%V_{C_2H_2}=\dfrac{a}{a+b}.100\%=\dfrac{\dfrac{2}{3}b}{\dfrac{2}{3}b+b}.100\%=40\%\\\%V_{C_4H_6}=100\%-40\%=60\%\end{matrix}\right.\)
TN1: \(n_{Br_2}=\dfrac{32}{160}=0,2\left(mol\right)\)
PTHH: C2H2 + 2Br2 --> C2H2Br4
a---->2a
C4H6 + 2Br2 --> C4H6Br4
b---->2b
=> 2a + 2b = 0,2 (2)
(1)(2) => a = 0,04 (mol); b = 0,06 (mol)
PTHH: C2H2 + 2AgNO3 + 2NH3 --> C2Ag2 + 2NH4NO3
0,04-------------------------->0,04
C4H6 + AgNO3 + NH3 --> C4H5Ag + NH4NO3
0,06----------------------->0,06
=> mkt = 0,04.240 + 0,06.161 = 19,26 (g)
--> Thỏa mãn đề bài
=> C4H6 có pư với AgNO3/NH3
=> C4H6 là ankin có nối ba đầu mạch
CTCT:
C2H2: \(CH\equiv CH\)
C4H6: \(CH\equiv C-CH_2-CH_3\)
2. Đốt cháy hoàn toàn 7,4g este X đơn chức thu đc 6,72 lít khí CO2(đktc) và 5,4g H2O. a) Xác định CTPT của X b) Đun 7,4g X trong dd NaOH vừa đủ đến khi pư hoàn toàn thu đc 3,2g ancol Y và 1 lượng muối Z. Viết công thức cấu tạo của X và tính khối lượng Z?
a) Gọi công thức phân tử của este X là CxHyOz.
a ax a.
y\2 (mol)Ta có :
(mol) ;
(mol)
=> mO = 7,4 – 0,3.12 -0,3.2 = 3,2g ; nO = 0,2 (mol)
=> x : y : z = 3 : 6 : 2
Vì X là este đơn chức nên công thức phân tử của X là C3H6O2
b)
nX = 0,1 mol, nY = 0,1 mol.
MY = 32g/mol => CTPT của Y : CH3OH
CTPT của X : CH3COOCH3.
đốt cháy hòan tòan 8,4 lít khí mentan( CH4) trong không khí.
a/ viết phương trình phản ứng sảy ra
\(CH_4+2O_2\rightarrow\left(t^o\right)CO_2+2H_2O\)
Đốt cháy hoàn toàn m gam este đơn chức X cần 5,6 lít khi oxi (đktc), thu được 12,4 gam hỗn hợp CO2 và nước có tỉ khối so với H2 là 15,5. CTPT của X là
A. C2H4O2
B. C3H6O2
C. C4H8O2
D. C5H10O2
Chọn đáp án C
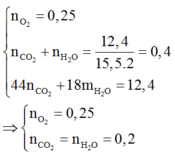
Như vậy, đây là este no, đơn chức
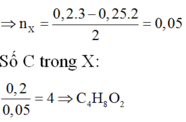
Đốt cháy hoàn toàn m gam este đơn chức X cần 5,6 lít khi oxi (đktc), thu được 12,4 gam hỗn hợp CO2 và nước có tỉ khối so với H2 là 15,5. CTPT của X là
A. C2H4O2
B. C3H6O2
C. C4H8O2
D. C5H10O2
Đôt cháy hết 17 gam một hợp chất X thu được 9 gam nước và 11,2 lít khí SO2 (đktc)
a) Tính thể tích khí O2 cần dùng để đốt cháy hết X.
b) X có những nguyên tố nào?
c) Tính tỉ lệ số nguyên tử của mỗi nguyên tố trong hợp chất X
d) Xác định công thức của X. Biết khối lượng mol của X bằng 34 g/mol.
a.
\(n_{SO_2}=\dfrac{11.2}{22.4}=0.5\left(mol\right)\)
Bảo toàn khối lượng :
\(m_{O_2}=9+0.5\cdot64-17=24\left(g\right)\)
b.
X có những nguyên tố : H và S
c.
\(n_{H_2O}=\dfrac{9}{18}=0.5\left(mol\right)\Rightarrow n_H=0.5\cdot2=1\left(mol\right)\)
Số nguyên tử H : Số nguyên tử S = 1 : 0.5 = 2 : 1
d.
Ta có công thức nguyên của X : \(\left(H_2S\right)_n\)
\(M_X=34n=34\left(\dfrac{g}{mol}\right)\)
\(\Rightarrow n=1\)
\(CT:H_2S\)
4. Đôt cháy 4,48 lít đktc hydrocacbon A, hấp thụ hết sp cháy vào dd Ba(OH)2 dư tạo ra 118,2 gam kết tủa, khối lượng dd giảm 77,4 gam . a. Tìm CTPT A
b Viết CTCT A
a) n A= 4,48/22,4=0,2 mol
n BaCO3= 118,2/197
= 0,6 mol
CO2+ Ba(OH)2=× BaCO3 + H2O
n CO2= n BaCO3= 0,6 mol
m dd giảm = mCO2 + m H2O- m BaCO3
= 44×0,6+18×nH2O- 118,2 = -77,4 gam
=× n H2O= 0,8 mol
Số C = nCO2/ nA
= 0,6/0,2=3
Số H= 2×nH2O/ nA
=2×0,8/0,2= 8
=× CTPT A là C3H8
b) CTCT:
CH3-CH2-CH3
Đoota cháy hết 1,62g hỗn hợp 2 este đơn chức no hở là đồng đẳng kế tiếp cần dùng vừa đủ 1,904 lít Oxi(đktc). CTPT 2 este?
\(n_{O_2}=\dfrac{1.904}{22.4}=0.085\left(mol\right)\)
Bảo toàn O :
\(n_{CO_2}=n_{H_2O}=\dfrac{1.62+\dfrac{1.904}{22.4}\cdot32}{44+18}=0.07\left(mol\right)\)
\(n_{este}=\dfrac{0.07\cdot2+0.07-0.085\cdot2}{2}=0.02\left(mol\right)\)
\(M=\dfrac{1.62}{0.02}=81\)
\(CT:C_3H_6O_2,C_4H_8O_2\)