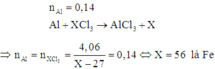Cho 3.78g bột Al phản ứng vừa đủ dung dịch XCl3 tạo ra dung dịch Y, khối lượng chất tan trong dung dịch Y giảm 4.06g so với dung dịch XCl3. Xác định công thức XCl3. tính nồng độ phần trăm các chất tan có trong Y

Những câu hỏi liên quan
Cho 3.78g bột Al phản ứng vừa đủ dung dịch XCl3 tạo ra dung dịch Y, khối lượng chất tan trong dung dịch Y giảm 4.06g so với dung dịch XCl3. Xác định công thức XCl3.
Mn giải bài này giúp mik theo cách tăng giảm khối lượng với, cảm ơn nhiều ạ
\(n_{Al}=\dfrac{3,78}{27}=0,14\left(mol\right)\\ Al+XCl_3\rightarrow AlCl_3+X\\ m_{giảm}=4,06\left(g\right)=m_X-m_{Al}\\n_X=n_{XCl_3}=n_{AlCl_3}=n_{Al}=0,14\left(mol\right)\\ m_X=m_{Al}+4,06=3,78+4,06=7,84\left(g\right)\\ M_X=\dfrac{7,84}{0,14}=56\left(\dfrac{g}{mol}\right)\\ Vậy.XCl_3.là:FeCl_3 \)
Đúng 1
Bình luận (0)
Cho 3.78g bột Al phản ứng vừa đủ dung dịch XCl3 tạo ra dung dịch Y, khối lượng chất tan trong dung dịch Y giảm 4.06g so với dung dịch XCl3. Xác định công thức XCl3.
Mọi người giải giúp mình với TT.
P/s có thể giải bài này theo cách tăng giảm khối lượng không nhỉ ?
C1: Al + XCl3 --> AlCl3 + X
nAl = 3,78 : 27 = 0,14 mol. => nAlCl3 tạo ra = 0,14 mol.
=> mAlCl3 = 0,14. 133,5 = 18,69g.
=> mXCl3 = 18,69 + 4,06 = 22,75g.
=> MXCl3 = 22,75 : 0,14 = 162,5 = X + 35,5 .3 => X = 56 (Fe)
C2: Dúng tăng giảm khối lượng
M chênh lệh giữa Al và X là 4,06 : 0,14 = 29 => x = 29 + 27 = 56 (fe)
Đúng 1
Bình luận (0)
Cho 3,78 gam bột nhôm phản ứng vừa đủ với dung dịch muối XCl3 tạo thành dung dịch Y, khối lượng chất tan trong dung dịch Y giảm 4,06 gam so với dung dịch XCl3. Xác định công thức của muối XCl3: A. InCl3. B. GaCl3 C. FeCl3. D. CrCl3.
Đọc tiếp
Cho 3,78 gam bột nhôm phản ứng vừa đủ với dung dịch muối XCl3 tạo thành dung dịch Y, khối lượng chất tan trong dung dịch Y giảm 4,06 gam so với dung dịch XCl3. Xác định công thức của muối XCl3:
A. InCl3.
B. GaCl3
C. FeCl3.
D. CrCl3.
GIÚP TỚ AAAAA:((
Cho 31.6g Al phản ứng vừa đủ với dung dịch H2SO4 19,6%.Hãy tính
A) Khối lượng dung dịch H2SO4 đã dùng
B) Thể tích khí tạo ra ở ĐKTC C) nồng độ phần trăm chất tan có trong phản ứng
\(n_{Al}=\dfrac{31,6}{27}=\dfrac{158}{135}\left(mol\right)\)
PT : \(2Al+6H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2\)
\(\dfrac{158}{135}\)---->\(\dfrac{316}{45}\)--------->\(\dfrac{158}{135}\)---->\(\dfrac{158}{45}\)
a) \(m_{ddH2SO4}=\dfrac{\dfrac{316}{45}.98}{19,6\%}=3511,1\left(g\right)\)
b) \(V_{H2\left(đktc\right)}=\dfrac{158}{45}.22,4=78,65\left(l\right)\)
\(C\%_{Al2\left(SO4\right)3}=\dfrac{\dfrac{158}{135}.342}{31,6+3511,1-\dfrac{158}{45}.2}.100\%=11,32\%\)
Đúng 2
Bình luận (1)
cho 12,9 gam hỗn hợp A gồm Al và Al2O3 tác dụng vừa đủ với dung dịch HCL 3,65% sau phản ứng thu được dung dịch Y và 3,36 lít khí (đktc) a) viết PTPU xảy ra và tính phần trăm khối lượng mỗi chất trong hỗn hợp đầu b) tính m và nồng độ phần trăm các chất trong dung dịch Y
Xem chi tiết
a) 2Al + 6HCl -> 2AlCl3 + 3H2
Al2O3 + 6HCl -> 2AlCl3 + 3H2O
nH2 = 0,15mol => nAl=0,1mol => mAl=2,7g; mAl2O3 = 10,2g => nAl2O3 = 0,1mol
=>%mAl=20,93% =>%mAl2O3 = 79,07%
b) nHCl = 0,1.3+0,1.6=0,9 mol=>mHCl(dd)=100g
mddY=12,9+100-0,15.2=112,6g
mAlCl3=22,5g=>C%=19,98%
Hoà tan hoàn toàn 10,2 gam Al2O3 trong dung dịch HNO3 15% vừa đủ, phản ứng tạo muối Al(NO3)3 (tan) và nước.
a/ Tính khối lượng dung dịch HNO3 phản ứng.
b/ Tính nồng độ % chất tan trong dung dịch thu được.
\(n_{Al}=\dfrac{10,2}{102}=0,1\left(mol\right)\)
PTHH: Al2O3 + 6HNO3 ---> 2Al(NO3)3 + 3H2O
0,1 0,6 0,2 0,3
\(\rightarrow m_{HNO_3}=0,6.63=37,8\left(g\right)\\ m_{ddHNO_3}=\dfrac{37,8}{15\%}=252\left(g\right)\\ m_{dd\left(sau.pư\right)}=252+10,2=262,2\left(g\right)\\ m_{Al\left(NO_3\right)_3}=0,2.213=42,6\left(g\right)\\ C\%_{Al\left(NO_3\right)_3}=\dfrac{42,6}{262,2}=16,25\%\)
Đúng 2
Bình luận (0)
Dùng lượng vừa đủ dung dịch HCl 10% để hòa tan m gam CuO, thu được dung dịch X. Trộn 200 ml dung dịch X với 150 ml dung dịch CuSO4 1,23 M (d= 1,18 g/ml), thu được dung dịch Y. Xác định giá trị của tổng nồng độ phần trăm các chất tan trong dung dịch Y
Xem chi tiết
bạn cho mình gửi sắp đến thi học kì 2 rồi. đây là những món quà mà bn sẽ nhận đc:1: áo quần2: tiền3: đc nhiều người yêu quý4: may mắn cả5: luôn vui vẻ trong cuộc sống6: đc crush thích thầm7: học giỏi8: trở nên xinh đẹpphật sẽ ban cho bn những điều này nếu cậu gửi tin nhắn này cho 25 người, sau 3 ngày bn sẽ có những đc điều đó. nếu bn ko gửi tin nhắn này cho 25 người thì bn sẽ luôn gặp xui xẻo, học kì 2 bn sẽ là học sinh yếu và bạn bè xa lánh( lời nguyền sẽ bắt đầu từ khi đọc) ( mình cũng bị ép);-; Đúng(0)
Đúng 0
Bình luận (0)
bn cho mình gửi sắp đến thi học kì 2 rồi. đây là những món quà mà bn sẽ nhận đc:
1: áo quần
2: tiền
3: đc nhiều người yêu quý
4: may mắn cả
5: luôn vui vẻ trong cuộc sống
6: đc crush thích thầm
7: học giỏi
8: trở nên xinh đẹp
phật sẽ ban cho bn những điều này nếu cậu gửi tin nhắn này cho 25 người, sau 3 ngày bn sẽ có những đc điều đó. nếu bn ko gửi tin nhắn này cho 25 người thì bn sẽ luôn gặp xui xẻo, học kì 2 bn sẽ là học sinh yếu và bạn bè xa lánh( lời nguyền sẽ bắt đầu từ khi đọc) ( mình
cũng bị ép);-;
Đúng 0
Bình luận (0)
Cho 5,4 gam kim loại X hóa trị III hòa tan hết vào dung dịch HCl thu được 6,72 lít khí H2 (đktc)
a)Lập PTHH của phản ứng.
b)Xác định kim loại X.
c) Tính khối lượng muối XCl3 tạo thành
\(a,PTHH:2X+6HCl\to 2XCl_3+3H_2\\ b,n_{H_2}=\dfrac{6,72}{22,4}=0,3(mol)\\ \Rightarrow n_{X}=\dfrac{2}{3}n_{H_2}=0,2(mol)\\ \Rightarrow M_{X}=\dfrac{5,4}{0,2}=27(g/mol)\)
Vậy X là nhôm (Al)
\(c,n_{AlCl_3}=n_{Al}=0,2(mol)\\ \Rightarrow m_{AlCl_3}=0,2.133,5=26,7(g)\)
Đúng 0
Bình luận (0)
1. Hòa tan hoàn toàn 7,8g hỗn hợp Z gồm Al và Mg trong dung dịch H2SO4 loãng 24,5% vừa đủ,thì khối lượng dung dịch sau phản ứng tăng so với dung dịch axit ban đầu là 7ga) Viết PTHH của phản ứng,tính khối lượng mỗi chất trong Zb) Tính nồng độ phần trăm ( C% ) của các chất tan trong duch dịch sau phản ứng2. Cho 8,96 lít khí CO ( ở đktc ) từ từ đi qua ống sứ nung nóng chứa 17,4g một oxit của kim loại M,đến khi phản ứng hoàn toàn chỉ thu được kim loại M và hỗn hợp khí Y có tỉ khối so với khí H2 bằng...
Đọc tiếp
1. Hòa tan hoàn toàn 7,8g hỗn hợp Z gồm Al và Mg trong dung dịch H2SO4 loãng 24,5% vừa đủ,thì khối lượng dung dịch sau phản ứng tăng so với dung dịch axit ban đầu là 7g
a) Viết PTHH của phản ứng,tính khối lượng mỗi chất trong Z
b) Tính nồng độ phần trăm ( C% ) của các chất tan trong duch dịch sau phản ứng
2. Cho 8,96 lít khí CO ( ở đktc ) từ từ đi qua ống sứ nung nóng chứa 17,4g một oxit của kim loại M,đến khi phản ứng hoàn toàn chỉ thu được kim loại M và hỗn hợp khí Y có tỉ khối so với khí H2 bằng 20.Viết PTHH của phản ứng,xác định CT của oxit