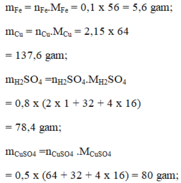Bài 1: Tính khối lượng của 1 mol Cl2, CH4 , CO2 , K2O , Fe2O3, CuSO4, NaOH, Fe(NO3)2 , Fe(OH)2 , K NO3, Tính khối lượng của 0,1 mol CaCO3 ; 0,5 mol H2O ; 0,15 mol CuO.

Những câu hỏi liên quan
Bài 4. Tính thể tích (đo ở đktc) của: a) 0,5 mol SO2 b) 3,2 g CH4 c) 0,9.1023 phân tử khí N2
Bài 5. Tính khối lượng của: a) 0,1 mol Al b) 0,3 mol Cu(NO3)2 ; c) 1,2.1023 phân tử Na2CO3 d) 8,96 lít CO2 (đktc) ; e) Mỗi nguyên tố có trong 0,5 mol K2CO3
cứu mình cần gấp
4.
a) \(V_{SO_2}=0.5\cdot22.4=11.2\left(l\right)\)
b) \(V_{CH_4}=\dfrac{3.2}{16}\cdot22.4=4.48\left(l\right)\)
c) \(V_{N_2}=\dfrac{0.9\cdot10^{23}}{6\cdot10^{23}}\cdot22.4=3.36\left(l\right)\)
5.
a) \(m_{Al}=0.1\cdot27=2.7\left(g\right)\)
b) \(m_{Cu\left(NO_3\right)_2}=0.3\cdot188=56.4\left(g\right)\)
c) \(m_{Na_2CO_3}=\dfrac{1.2\cdot10^{23}}{6\cdot10^{23}}\cdot106=21.2\left(g\right)\)
d) \(m_{CO_2}=\dfrac{8.96}{22.4}\cdot44=17.6\left(g\right)\)
e) \(m_K=0.5\cdot2\cdot39=39\left(g\right)\\ m_C=0.5\cdot12=6\left(g\right)\\ m_O=0.5\cdot3\cdot16=24\left(g\right)\)
Đúng 2
Bình luận (1)
a. Tính số mol của : 14g Fe, 20g Ca, 25g CaCO3, 4g NaOH, 1,5.1023phân tử H2O
b. Tính khối lượng của: 0,25mol ZnSO4, 0,2 mol AlCl3, 0,3 mol Cu; 0,35mol Fe2(SO4)3.
c. Tính thể tích của các chất khí ở đktc: 0,2mol CO2; 0,15mol Cl2; 0,3mol SO2; 0,5mol CH4.
a)
\(n_{Fe}=\dfrac{14}{56}=0,25\left(mol\right)\)
\(n_{Ca}=\dfrac{20}{40}=0,5\left(mol\right)\)
\(n_{CaCO_3}=\dfrac{25}{100}=0,25\left(mol\right)\)
\(n_{NaOH}=\dfrac{4}{40}=0,1\left(mol\right)\)
\(n_{H_2O}=\dfrac{1,5.10^{23}}{6.10^{23}}=0,25\left(mol\right)\)
b)
\(m_{ZnSO_4}=0,25.161=40,25\left(g\right)\)
\(m_{AlCl_3}=0,2.133,5=26,7\left(g\right)\)
\(m_{Cu}=0,3.64=19,2\left(g\right)\)
\(m_{Fe_2\left(SO_4\right)_3}=0,35.400=140\left(g\right)\)
c)
\(V_{CO_2}=0,2.22,4=4,48\left(l\right)\)
\(V_{Cl_2}=0,15.22,4=3,36\left(l\right)\)
\(V_{SO_2}=0,3.22,4=6,72\left(l\right)\)
\(V_{CH_4}=0,5.22,4=11,2\left(l\right)\)
Đúng 2
Bình luận (0)
a: \(n_{Fe}=\dfrac{14}{56}=0.25\left(mol\right)\)
\(n_{Ca}=\dfrac{20}{40}=0.5\left(mol\right)\)
Đúng 2
Bình luận (0)
Hãy tính khối lượng của những lượng chất sau: 0,1 mol Fe; 2,15 mol Cu; 0,8 mol H 2 S O 4 ; 0,5 mol C u S O 4 .
1) Hỗn hợp gồm 0,15 mol CO2 và 0,05 mol CO. Tính tỉ khối của hỗn hợp so với không khí
2) Tính khối lượng của các chất
a) 3,675g CaCl2 . 2H2O
b) 19,98g CuCO3 . CU(OH)2 (quặng mabchit)
c) 11,1g Mg (NO3)2
d) 14,4g FeS2
không phải là tính khối lượng chất mà là Tính số mol nha mọi người
Đúng 0
Bình luận (0)
Hãy cho biết khối lượng của những lượng chất sau:
a) 0,5 mol nguyên tử N; 0,01 mol nguyên tử Cl; 3 mol nguyên tử O;
b) 0,5 mol phân tử N2; 0,10 mol phân tử Cl2 ; 3 mol phân tử O2
c) 0,1 mol Fe ; 2,15 mol Cu, 0,8 mol H2SO4 ; 0,5 mol CuSO4
a) mN = 0,5 .14 = 7g.
mCl = 0,1 .35.5 = 3.55g
mO = 3.16 = 48g.
b) mN2 = 0,5 .28 = 14g.
mCl2 = 0,1 .71 = 7,1g
mO2 = 3.32 =96g
c) mFe = 0,1 .56 =5,6g mCu = 2,15.64 = 137,6g
mH2SO4 = 0,8.98 = 78,4g.
mCuSO4 = 0,5 .160 = 80g
Đúng 0
Bình luận (0)
Tính :a) khối lượng của 0,025 mol FeCl3; 0,5 mol H2O; 0,35 mol Cu(NO3)2b) Thể tích ở đktc của: 0,3 mol khí H2 ; 16 gam khí SO2 ; 26,4 gam CO2
Đọc tiếp
Tính :
a) khối lượng của 0,025 mol FeCl3; 0,5 mol H2O; 0,35 mol Cu(NO3)2
b) Thể tích ở đktc của: 0,3 mol khí H2 ; 16 gam khí SO2 ; 26,4 gam CO2
a)
\(m_{FeCl_3}=0,025\cdot162,5=4,0625\left(g\right)\)
\(m_{H_2O}=0,5\cdot18=9\left(g\right)\)
\(m_{Cu\left(NO_3\right)_2}=0,35\cdot188=65,8\left(g\right)\)
b)
\(V_{H_2}=0,3\cdot22,4=6,72\left(l\right)\)
\(n_{SO_2}=\dfrac{16}{64}=0,25\left(mol\right)\) \(\Rightarrow V_{SO_2}=0,25\cdot22,4=5,6\left(l\right)\)
\(n_{CO_2}=\dfrac{26,4}{44}=0,6\left(mol\right)\) \(\Rightarrow V_{CO_2}=0,6\cdot22,4=13,44\left(l\right)\)
Đúng 0
Bình luận (0)
Cho 13,0 gam bột Zn vào dung dịch có chứa 0,1 mol Fe(NO3)3 ; 0,1 mol Cu(NO3)2 và 0,1 mol AgNO3. Khuấy đều cho phản ứng xảy ra hoàn toàn. Tính khối lượng kết tủa thu được sau phản ứng ?
A. 17,2 gam
B. 14,0 gam
C. 19,07 gam
D. 16,4 gam
Chọn đáp án A
Với bài toán kim loại tác dụng với muối các bạn cứ quan niệm là kim loại mạnh nhất sẽ đi nuốt anion của thằng yếu nhất trước.
Ta có
![]()
lượng NO3 này sẽ phân bổ dần cho:
Đầu tiên
![]()
![]()
Và Cu + Ag bị cho ra ngoài hết
![]()
Đúng 0
Bình luận (0)
a. Tính số mol của : 14g Fe, 25g CaCO3, 4gNaOH, 1,5.1023phân tử
b. Tính khối lượng của: 0,25 mol ZnSO4,0,2 mol AICI3, 0,3 mol Cu; 0,35 mol Fe2(SO4)3
c. Tính thể tích của các chất khí ở đktc: 0,2 mol CO2; 0,15 mol CI2; 0,3 mol SO2
a) \(n_{Fe}=\dfrac{14}{56}=0,25\left(mol\right)\)
\(n_{CaCO_3}=\dfrac{25}{100}=0,25\left(mol\right)\)
\(n_{NaOH}=\dfrac{4}{40}=0,1\left(mol\right)\)
\(n_{...}=\dfrac{1,5.10^{23}}{6.10^{23}}=0,25\left(mol\right)\)
b)
\(m_{ZnSO_4}=0,25.161=40,25\left(g\right)\)
\(m_{AlCl_3}=0,2.133,5=26,7\left(g\right)\)
\(m_{Cu}=0,3.64=19,2\left(g\right)\)
\(m_{Fe_2\left(SO_4\right)_3}=0,35.400=140\left(g\right)\)
d) \(V_{CO_2}=0,2.22,4=4,48\left(l\right)\)
\(V_{Cl_2}=0,15.22,4=3,36\left(l\right)\)
\(V_{SO_2}=0,3.22,4=6,72\left(l\right)\)
Đúng 4
Bình luận (0)
1. Cho 222g Canxi hiđroxit Ca(OH2) tác dụng hoàn toàn với 325g sắt (III) clorua FeCl2. Sau phản ứng thứ được 214g sắt(III) hiđroxit Fe(OH)3 và x (g) canxi clorua CaCl2
a) Lập PTHH; b) Xác định x
2. Tính khối lượng mol của các chất khí có tỉ khối số với khí hiđro lần lương là: 16,8,14,35,5,22
3. Cho chất khí A có tỉ khối hơi đối với khí metan CH4 bằng 2,74. Tìm khối lượng mol của chất khí B, biết rằng tỉ khối hơi của chất khí B số với chất khí A bằng 1,4545
4. Tìm ng.tố X biết 18×10^22 nguyên...
Đọc tiếp
1. Cho 222g Canxi hiđroxit Ca(OH2) tác dụng hoàn toàn với 325g sắt (III) clorua FeCl2. Sau phản ứng thứ được 214g sắt(III) hiđroxit Fe(OH)3 và x (g) canxi clorua CaCl2
a) Lập PTHH; b) Xác định x
2. Tính khối lượng mol của các chất khí có tỉ khối số với khí hiđro lần lương là: 16,8,14,35,5,22
3. Cho chất khí A có tỉ khối hơi đối với khí metan CH4 bằng 2,74. Tìm khối lượng mol của chất khí B, biết rằng tỉ khối hơi của chất khí B số với chất khí A bằng 1,4545
4. Tìm ng.tố X biết 18×10^22 nguyên tử X có khối lượng 19,5g
5. Số mol của
a) 25g CaCO3; b) 4g NaOH; c) 1,5×10^23 phân tử H2O
Khối lượng của
a) 0,25 mol ZnSO4; b) 0,2 mol AlCl3; c) Hỗn hợp gồm: 0,5 mol Ca(OH)2 - 0, 35 mol Fe2(SO4) 3
Thế tích của các chất khí ở ĐTC của
a) 0,2 mol CO2; b) 0,15 mol Cl2; c) Hỗm hợp khí: 0,3 mol SO2 - 0,5 mol CH4
1. Cho 222g Canxi hiđroxit Ca(OH2) tác dụng hoàn toàn với 325g sắt (III) clorua FeCl2. Sau phản ứng thứ được 214g sắt(III) hiđroxit Fe(OH)3 và x (g) canxi clorua CaCl2
a) Lập PTHH; b) Xác định x
(Bạn viết sai đề : Sắt (III) clorua là: \(FeCl_3\) )
-Giải:
a.PTHH: \(3Ca\left(OH\right)_2+2FeCl_3\rightarrow2Fe\left(OH\right)_3+3CaCl_2\)
b. Áp dụng định luật bảo toàn khối lượng ta có:
\(m_{Ca\left(OH_{ }\right)_2}+m_{FeCl_3}=m_{Fe\left(OH\right)_3}+m_{CaCl_2}\)
\(\Rightarrow m_{CaCl_2}=m_{Ca\left(OH\right)_2}+m_{FeCl_3}-m_{Fe\left(OH\right)_3}\)
\(m_{CaCl_2}=222+325-214=333\left(g\right)\)
Vậy khối lượng \(CaCl_2\) là 333g hay x = 333g
Đúng 0
Bình luận (0)
Bài 5:
GIẢI:
* TÍNH SỐ MOL:
a. \(n_{CaCO_3}=\dfrac{m}{M}=\dfrac{25}{100}=0,25\left(mol\right)\)
b. \(n_{NaOH}=\dfrac{4}{40}=0,1\left(mol\right)\)
c. \(n_{H_2O}=\dfrac{1,5\times10^{23}}{6\times10^{23}}=0,25\left(mol\right)\)
* KHỐI LƯỢNG:
\(a.m_{ZnSO_4}=n.M=0,25.161=40,25\left(g\right)\)
b. \(m_{AlCl_3}=0,2.133,5=26,7\left(g\right)\)
c. \(m_{hh}=0,5.74+0,35.400=37+140=177\left(g\right)\)
* THỂ TÍCH:
a. \(V_{CO_2}=n.22,4=0,2.22,4=4,48\left(l\right)\)
b. \(V_{Cl_2}=0,15.22,4=3,36\left(l\right)\)
c. \(V_{hh}=\left(0,3+0,5\right).22,4=17,92\left(l\right)\)
Đúng 0
Bình luận (0)