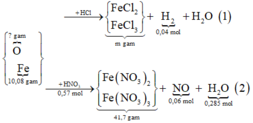
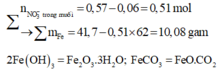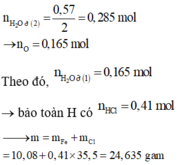Hỗn hợp A chứa Fe và M có khối lượng không đổi. Tỉ lệ số mol của M và Fe trong A là 2:3. Chia hỗn hợp thành 3 phần bằng nhau
-Phần 1: Đốt cháy hết trong oxi được 66,8g hỗn hợp gồm Fe3O4 và oxit của M
-Phần 2: Hòa tan hết trong dung dịch HCl thu được 26,88 lit H2 ở đktc
-Phần 3: Tác dụng vừa đủ với 33,6 lít H2 ở đktc
Xác định khối lượng M và khối lượng từng kim loại có trong hỗn hợp M