Cho 10 gam hỗn hợp gồm Fe và FeO phản ứng hoàn toàn với dung dịch H2SO4 loãng người ta thu được 1,12 lit khí ở đktc.
1. Tính khối lượng của mỗi chất có trong hỗn hợp?
2. Tính khối lượng dung dịch H2SO4 9,8% cần dùng để phản ứng hết với hỗn hợp trên?
Cho 10 gam hỗn hợp gồm Fe và FeO phản ứng hoàn toàn với dung dịch H2SO4 loãng người ta thu được 1,12 lit khí ở đktc.
1. Tính khối lượng của mỗi chất trong hỗn hợp?
2. Tính khối lượng dung dịch H2SO4 9,8% cần dùng để phản ứng hết với hỗn hợp trên?
3. Tính nồng độ phần trăm của dung dịch muối sau phản ứng
\(n_{H2}=\dfrac{1,12}{22,4}=0,05\left(mol\right)\)
Pt : \(Fe+H_2SO_4\rightarrow FeSO_4+H_2|\)
1 1 1 1
0,05 0,05 0,05 0,05
\(FeO+H_2SO_4\rightarrow FeSO_4+H_2O|\)
1 1 1 1
0,1 0,1 0,1
1) \(n_{Fe}=\dfrac{0,05.1}{1}=0,05\left(mol\right)\)
\(m_{Fe}=0,05.56=2,8\left(g\right)\)
\(m_{FeO}=10-2,8=7,2\left(g\right)\)
2) Có : \(m_{FeO}=7,2\left(g\right)\)
\(n_{FeO}=\dfrac{7,2}{72}=0,1\left(mol\right)\)
\(n_{H2SO4\left(tổng\right)}=0,05+0,1=0,15\left(mol\right)\)
\(m_{H2SO4}=0,15.98=14,7\left(g\right)\)
\(m_{ddH2SO4}=\dfrac{14,7.100}{9,8}=150\left(g\right)\)
3) \(n_{FeSO4\left(tổng\right)}=0,05+0,1=0,15\left(mol\right)\)
⇒ \(m_{FeSO4}=0,15.152=22,8\left(g\right)\)
\(m_{ddspu}=10+150-\left(0,05.2\right)=159,9\left(g\right)\)
\(C_{FeSO4}=\dfrac{22,8.100}{159,9}=14,26\)0/0
Chúc bạn học tốt
Câu 3: Cho 12,8 gam hỗn hợp X gồm FeO và Fe vào dung dịch H2SO4 loãng, dư. Sau khi các phản ứng xảy ra hoàn toàn thu được 2,24 lit khí ở đktc.
a. Viết phương trình phản ứng xảy ra.
b. Tính thành phần phần trăm theo khối lượng mỗi chất trong hỗn hợp X.
c. Cho 6,4 gam hỗn hợp X ở trên tác dụng với dung dịch H2SO4 đặc nóng, dư thu được khí SO2. Sục toàn bộ lượng khí SO2 thu được vào dung dịch nước vôi trong lấy dư thấy xuất hiện kết tủa. Cho biết khối lượng dung dịch nước vôi trong tăng hay giảm bao nhiêu gam?
Chào em, em đăng bài nhầm môn, em đăng sang môn Hóa nha!
Cho 32 gam hỗn hợp X gồm Fe và FeO phản ứng với dung dịch H2SO4 loãng, dư, thu được 5,6 lít khí H2 (đktc). Tính % khối lượng mỗi chất trong X
\(n_{H_2}=\dfrac{5,6}{22,4}=0,25\left(mol\right)\)
PTHH: Fe + H2SO4 ---> FeSO4 + H2
0,25<--------------------------0,25
\(\Rightarrow m_{Fe}=0,25.56=14\left(g\right)\\ \Rightarrow\left\{{}\begin{matrix}\%m_{Fe}=\dfrac{14}{32}.100\%=43,75\%\\\%m_{FeO}=100\%-43,75\%=56,25\%\end{matrix}\right.\)
Câu 2: Hòa tan hoàn toàn 20 gam hỗn hợp và FeO bằng lượng vừa đủ dung dịch H2SO4 gồm Fe 10%, thu được 2,24 lít khí H2 (ở đktc) và dung dịch Y. a) Viết các phương trình phản ứng xảy ra. b) Tính khối lượng dung dịch Y và C% của chất tan trong dung dịch Y. (45,6g và 14,53%)
Hòa tan hoàn toàn 20 gam hỗn hợp X gồm Fe và FeO vào m gam dung dịch H2SO4 9,8% (loãng), (dư 10% so với lượng đã lấy) thì thu được 2,24 lít khí (đktc)
a) Tính % theo khối lượng của FeO và giá trị m
b) Cho toàn bộ lượng X trên tác dụng với H2SO4 đặc, nóng, dư thu được V lít khí SO2 (sản phẩm khử duy nhất ở đktc). Tính V
c) Lượng khí SO2 này có thể làm mất màu tối đa bao nhiêu ml dung dịch Br2 1M
Cho 18,8 gam hỗn hợp rắn A gồm Fe và FeO vào H2SO4 đặc nóng dư thu được Vml khí đkc. Cũng lượng rắn A trên nhưng cho vào dung dịch H2SO4 loãng dư thì thu được 1,12 lít khí đkc.
a/ Tính V
b/ Tính % khối lượng của Fe và FeO trong hỗn hợp ban đầu
nFe= a mol
n FeO= b mol
Ta có 56a+72b=18,8 (1)
2Fe+ 6H2SO4(đ)-> Fe2(SO4)3 +3SO2+6H2O
a. 1,5a
2FeO +4H2SO4(đ)-> Fe2(SO4)3 +SO2+4H2O
b. 0,5b
Mặt khác ta có
Fe+H2SO4(l)-> FeSO4+H2
a. a
FeO+H2SO4-> FeSO4+H2O
a=nH2=1,12/22,4=0,05
Từ (1)=>b=0,222mol
=> nSO2=1,5a+0,5b= 0,186mol
V(SO2)=4,1664LIT
B, %mFe= 0,05.56.100%/18,8=14,9%
mFeO= 18,8-,05.56=16g
=> %mFeO = 16.100%/18,8=85,1%
Cho hỗn hợp X gồm Fe, FeO và Fe(NO3)2 có tổng số mol là 0,4 mol hoà tan hoàn toàn trong dung dịch loãng chứa 0,52 mol H2SO4, kết thúc phản ứng thu được dung dịch Y và 5,376 lít khí NO (đktc). Dung dịch Y có thể phản ứng tối đa với 8,96 gam Fe hoặc 10,24 gam Cu. Biết các phản ứng xảy ra hoàn toàn và sản phẩm khử duy nhất của N+5 trong cả quá trình là NO. Phần trăm khối lượng của Fe đơn chất trong hỗn hợp X gần nhất với
A. 25%
B. 26%
C. 27%
D. 28%
Chọn đáp án B
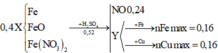
Y có thể gồm các ion thuộc 1 trong 3 trường hợp:
TH1: Fe2+ (có thể), Fe3+, H+, S O 4 2 -
TH2: Fe2+ (có thể), N O 3 - , S O 4 2 -
TH3: Fe3+, H+, N O 3 - , S O 4 2 -
Lượng Cu và Fe hoà tan tối đa là như nhau Þ Chỉ có thể là TH2 hoặc TH3 vì TH1 có H+ mà không
có N O 3 - Þ Tạo thêm H2, làm cho lượng Fe tối đa hoà tan được nhiều hơn Cu
nCu max = nFe max = 0,16 Þ Số mol Fe3+ trong Y tối đa = 0,16x2 = 0,32
Với TH3 thì nFe3+ = 0,4 Þ Chỉ có TH2 thỏa mãn Y
Trong đó Y chứa: Fe3+ (0,32 mol), Fe2+ (0,08 mol), N O 3 - , S O 4 2 - (0,52 mol)
BTĐT Þ nNO = 0,32x3 + 0,08x2 - 0,52x2 = 0,08
Bán phản ứng Þ nFeO = (0,52x2 - 0,24x4)/2 = 0,04
BTNT.N Þ nFe(NO3)2 = (0,24 + 0,08)/2 = 0,16 Þ nFe = 0,4 - 0,16 - 0,04 = 0,2
Vậy %Fe(NO3)2 = ![]()
Cho 28,4 gam hỗn hợp bột mịn X (gồm Al, Cr, Fe, Cu và Ag) vào dung dịch H 2 S O 4 loãng, nóng. Sau khi các phản ứng xảy ra hoàn toàn có 17,2 gam chất rắn tách ra, đồng thời thu được 4,48 lít khí (đktc). Độ tăng khối lượng của dung dịch sau phản ứng so với khối lượng dung dịch H2SO4 ban đầu là
A. 15,2 gam
B. 10,8 gam
C. 10 gam
D. 11,2 gam
a) Cho 29,6 gam hỗn hợp gồm Cu và Fe tác dụng với oxi không khí, sau phản ứng thu được 39,2 gam hỗn hợp A gồm ( CuO, FeO, Fe2O3 và Fe3O4). Hòa tan hoàn toàn A trong dung dịch H2SO4 loãng, dư. 1. Tính số mol H2SO4 đã tham gia phản ứng 2. Tính khối lượng muối sunfat thu được.
b) Khử hoàn toàn 2,552 gam một oxit kim loại cần 985,6 ml H2(đktc), lấy toàn bộ lượng kim loại thoát ra cho vào dung dịch HCl dư thu được 739,2 ml H2(đktc). Xác định công thức của oxit kim loại đã dùng?
a, Ta có: $n_{O}=0,6(mol)$
Suy ra $n_{H^+/pu}=1,2(mol)\Rightarrow n_{H_2SO_4}=0,6(mol)$
Bảo toàn khối lượng ta có: $m_{muoi}=29,6+0,6.96=87,2(g)$
Theo gt ta có: $n_{H_2}=0,044(mol);n_{H_2/(2)}=0,033(mol)$
Gọi CTTQ của oxit là $M_xO_y$
Ta có: \(M_{M_xO_y}=58y\)
Mặt khác $m_{M}=2,552-0,044.16=1,848(g)\Rightarrow M_{M}=28n$
Vậy M là Fe
Do đó CT của oxit cần tìm là Fe3O4