Dùng 6.72l CO khử hoàn toàn 8g oxit kim loại M thu được kim loại và hỗn hợp khí B có tỉ khối so với H2 là 18. Mặt khác toàn bộ lượng kim loại sinh ra hòa tan hoàn toàn và dd HCl được 2.24l H2 (đktc). Tìm M và công thức oxit.
Giúp mk vs ạ
Dùng 6.72l CO khử hoàn toàn 8g oxit kim loại M thu được kim loại và hỗn hợp khí B có tỉ khối so với H2 là 18. Mặt khác toàn bộ lượng kim loại sinh ra hòa tan hoàn toàn và dd HCl được 2.24l H2 (đktc). Tìm M và công thức oxit.
Giúp mk vs ạ nêu cả cách giải vs
n CO = 6,72/22,4 = 0,3(mol)
n H2 = 2,24/22,4 = 0,1(mol)
B gồm : CO(x mol) ; CO2(y mol)
M B = 18.2 = 36
x + y = 0,3
28x + 44y = 36(x + y)
=> x = y = 0,15
$CO + O_{oxit} \to CO_2$
n O(oxit) = n CO2 = 0,15(mol)
=> m M = 8 - 0,15.16 = 5,6(gam)
n là hóa trị của M
$2M + 2HCl \to 2MCl_n + nH_2$
n M = 2/n . nH2 = 0,2/n (mol)
=> 0,2/n . M = 5,6
=> M = 28n
Với n = 2 thì M = 56(Fe)
n Fe = 5,6/56 = 0,1(mol)
n Fe / n O = 0,1/0,15 = 2/3 . Vậy oxit là Fe2O3
Khử hoàn toàn 2,784 gam một oxit kim loại bằng 1,344 lít CO (đktc), sau phản ứng thu được hỗn hợp khí có tỉ khối so với H2 là 20,4. Lấy toàn bộ lượng kim loại thoát ra cho vào dung dịch HCl dư thu được 806,4 ml H2(đktc). Xác định công thức của oxit kim loại đã dùng?
PTHH: AxOy + yCO --to--> xA + yCO2
Có: nCO(dư) + nCO2 = nCO(bd) = \(\dfrac{1,344}{22,4}=0,06\left(mol\right)\)
Mà \(\dfrac{28.n_{CO\left(dư\right)}+44.n_{CO_2}}{n_{CO}+n_{CO_2}}=20,4.2=40,8\)
=> nCO2 = 0,048 (mol)
\(n_{A_xO_y}=\dfrac{2,784}{x.M_A+16y}\left(mol\right)\)
AxOy + yCO --to--> xA + yCO2
=> \(\left\{{}\begin{matrix}n_{CO_2}=\dfrac{2,784y}{x.M_A+16y}=0,048\left(mol\right)\left(1\right)\\n_A=\dfrac{2,784x}{x.M_A+16y}\left(mol\right)\end{matrix}\right.\)
(1) => \(M_A=\dfrac{42y}{x}=>\dfrac{y}{x}=\dfrac{M_A}{42}\) (2)
PTHH: 2A + 2nHCl --> 2ACln + nH2
=> \(n_{H_2}=\dfrac{1,392xn}{x.M_A+16y}=0,036\left(mol\right)\)
=> \(1,392n=0,036.M_A+\dfrac{0,576y}{x}\) (3)
(2)(3) => MA = 28n
Xét n = 1 => L
Xét n = 2 => MA = 56 (Fe) => \(\dfrac{x}{y}=\dfrac{3}{4}\) => CTHH: Fe3O4
Xin cảm ơn mọi người đã đọc câu hỏi này nhưng em đã nghĩ ra đáp án cho bài tập này rồi ạ
Khử hoàn toàn 24 g một oxit kim loại M bằng H2 dư thu được 8,1 g nước. Hòa tan toàn bộ lượng kim loại sinh ra bằng dd H2SO4 loãng dư thu được 6,72 lít H2 ở đktc. Xác định oxit kim loại M?
Ta có: \(n_{H_2O}=\dfrac{8,1}{18}=0,45\left(mol\right)\)
⇒ n O (trong oxit) = 0,45 (mol)
Có: m oxit = mM + mO ⇒ mM = 24 - 0,45.16 = 16,8 (g)
Giả sử kim loại M có hóa trị n khi tác dụng với H2SO4.
PT: \(2M+nH_2SO_4\rightarrow M_2\left(SO_4\right)_n+nH_2\)
Ta có: \(n_{H_2}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\)
Theo PT: \(n_M=\dfrac{2}{n}n_{H_2}=\dfrac{0,6}{n}\left(mol\right)\)
\(\Rightarrow M_M=\dfrac{16,8}{\dfrac{0,6}{n}}=28n\)
Với n = 1 ⇒ MM = 28 (loại)
Với n = 2 ⇒ MM = 56 (nhận)
Với n = 3 ⇒ MM = 84 (loại)
⇒ M là Fe. ⇒ Oxit cần tìm là FexOy.
PT: \(Fe_xO_y+yH_2\underrightarrow{t^o}xFe+yH_2O\)
Theo PT: \(n_{Fe_xO_y}=\dfrac{1}{y}n_{H_2O}=\dfrac{0,45}{y}\left(mol\right)\)
\(\Rightarrow M_{Fe_xO_y}=\dfrac{24}{\dfrac{0,45}{y}}=\dfrac{160}{3}y\)
\(\Rightarrow56x+16y=\dfrac{160}{3}y\)
\(\Rightarrow\dfrac{x}{y}=\dfrac{2}{3}\)
Vậy: Oxit đó là Fe2O3.
Bạn tham khảo nhé!
Khử 3,48g một oxit của kim loại M cần dùng 1,344l khí H2(đktc). Toàn bộ lượng kim loại thu được cho tác dụng với dd HCl dư sinh ra 1,008l khí H2(đktc). Tìm kim loại M và oxit của nó.
nH2 (khử)= 1,344/22,4= 0,06 mol
nH2 (axit)= 1,008/22,4= 0,045 mol
nH2(khử)= nO(bị khử)
=> mO (bị khử)= 0,06.16= 0,96g
=> mM= 3,48-0,96= 2,52g
2M+ 2nHCl -> 2MCln+ nH2
nH2 (axit)= 0,045 mol => nM= 0,09/n mol
=> MM= 28n
n=2 => M=56. Vậy M là Fe
Mặt khác:
nFe= nH2(axit)= 0,045 mol
nO (bị khử)= 0,06 mol
nFe : nO= 3:4
Vậy oxit sắt là Fe3O4
dùng khí CO khử hoàn toàn 4g 1 oxit kim loại ở nhiệt độ cao, phản ứng thu được kim loại và hỗn hợp khí X có tỉ khối so với H2 là 19. Cho X hấp thụ hoàn toàn vào nước vôi trong dư, thu được 5g kết tủa. Tìm CTHH của oxit kim loại đã dùng
CTHH: A2Oy
\(n_{CaCO_3}=\dfrac{5}{100}=0,05\left(mol\right)\)
PTHH: A2Oy + yCO --to--> 2A + yCO2
\(\dfrac{0,05}{y}\)<---------------------0,05
Ca(OH)2 + CO2 --> CaCO3 + H2O
0,05<---0,05
=> \(M_{A_2O_y}=2.M_A+16y=\dfrac{4}{\dfrac{0,05}{y}}\)
=> \(M_A=32y\left(g/mol\right)\)
Xét y = 1 => MA = 32 (Loại)
Xét y = 2 => MA = 64 (Cu)
Vậy CTHH của oxit là CuO
Cho 7,5 gam hỗn hợp X gồm kim loại M (hóa trị không đổi) và Mg (tỉ lệ mol tương ứng 2 : 3) tác dụng với 3,36 lít Cl2, thu được hỗn hợp rắn Y. Hòa tan hết toàn bộ Y trong lượng dư dung dịch HCl, thu được 1,12 lít H2. Biết các phản ứng đều xảy ra hoàn toàn, các thể tích khí đều đo ở đktc. Kim loại M là
Cho 7,5 gam hỗn hợp X gồm kim loại M (hóa trị không đổi) và Mg (tỉ lệ mol tương ứng 2 : 3) tác dụng với 3,36 lít Cl2, thu được hỗn hợp rắn Y. Hòa tan hết toàn bộ Y trong lượng dư dung dịch HCl, thu được 1,12 lít H2. Biết các phản ứng đều xảy ra hoàn toàn, các thể tích khí đều đo ở đktc. Kim loại M là
Cho 7,5 gam hỗn hợp X gồm kim loại M (hóa trị không đổi) và Mg (tỉ lệ mol tương ứng 2 : 3) tác dụng với 3,36 lít Cl2, thu được hỗn hợp rắn Y. Hòa tan hết toàn bộ Y trong lượng dư dung dịch HCl, thu được 1,12 lít H2. Biết các phản ứng đều xảy ra hoàn toàn, các thể tích khí đều đo ở đktc. Kim loại M là
A. Al.
B. Na
C. Ca.
D. K.
Dùng V (lít) khí CO (đktc) khử hoàn toàn 4g một oxit kim loại ở nhiệt độ cao, phản ứng kết thúc thu được kim loại và hỗn hợp khí X có tỉ khối so với H2 là 19. Cho X hấp thụ hoàn toàn cào nước vôi trong dư, thu được 5g kết tủa. a) Tìm CTHH của oxit kim loại đã dùng b) Tính V? Xác định % về khối lượng của hỗn hợp khí X.
a)
$CO_2 +C a(OH)_2 \to CaCO_3 + H_2O$
n CO2 = n CaCO3 = 5/100 = 0,05(mol)
$CO + O_{oxit} \to CO_2$
n O(oxit) = n CO2 = 0,05(mol)
CTHH của oxit : RxOy
=> n oxit = 0,05/y (mol)
=> (Rx + 16y).0,05/y = 4
<=> Rx = 64y
Với x = y = 1 thì R = 64(Cu)
Vậy oxit là CuO
b)
X gồm CO(a mol) và CO2(0,05 mol)
M X = 19.2 = 38
=> 28a + 0,05.44 = (a + 0,05).38
<=> a = 0,03
n CO = n CO2 + n CO dư = 0,08(mol)
=> V = 0,08.22,4 = 1,792 lít
%m CO = 0,03.28/(0,03.28 + 0,05.44) .100% = 27,63%
%m CO2 = 100% -27,63% = 72,37%
\(n_{CaCO_3}=\dfrac{5}{100}=0.05\left(mol\right)\)
\(n_{CO_2}=0.05\left(mol\right)\)
\(n_{CO}=a\left(mol\right)\)
\(\overline{M}=\dfrac{28a+0.05\cdot44}{a+0.05}=19\cdot2=38\left(\dfrac{g}{mol}\right)\)
\(\Rightarrow x=0.03\)
\(M_xO_y+yCO\underrightarrow{^{t^0}}xM+yCO_2\)
\(\dfrac{0.05}{y}.................0.05\)
\(M=\dfrac{4}{\dfrac{0.05}{y}}=80y\)
\(\Leftrightarrow xM+16y=80y\)
\(\Leftrightarrow xM=64y\)
\(x=y=1,M=64\)
\(CT:CuO\)
\(V_{CO}=\left(0.05+0.03\right)\cdot22.4=1.792\left(l\right)\)
\(\%m_{CO}=\dfrac{0.03\cdot28}{0.03\cdot28+0.05\cdot44}\cdot100\%=27.63\%\)
\(\%m_{CO_2}=72.37\%\)
Khử hoàn toàn 24g hỗn hợp gồm CuO và Fe2O3 bằng khí CO dư
Kết thức phản ứng thu được hỗn hợp 2 kim loại
Cho toàn bộ kim loại sinh ra vào dung dịch H2(SO4) loãng dư thu được 4.48 lít H2 (đktc)
a) Tính khối lượng mỗi oxit trong hỗn hợp ban đầu?
b) Tính thế tích khí CO cần dùng ở đktc?
Khử hoàn toàn 4,06 gam một oxit kim loại bằng khí CO ở nhiệt độ cao thành kim loại. Dẫn toàn bộ khí sinh ra vào bình đựng dung dịch Ca(OH)2 (dư) tạo thành 7,00 gam kết tủa. Nếu lấy lượng kim loại sinh ra hòa tan hết vào dung dịch HCl (dư) thì thu được 1,176 lít khí H2 (đktc). Công thức của oxit kim loại là
A. FeO.
B. CrO.
C. Fe2O3.
D. Fe3O4
Gọi công thức oxit ban đầu là MxOy.
Có phản ứng khử hoàn toàn oxit MxOy thành kim loại:
![]()
Dẫn khí CO2 sinh ra hấp thụ vào dung dịch Ca(OH)2 dư:
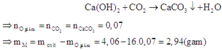
Cần lưu ý: Hóa trị của kim loại M trong oxit ban đầu và hóa trị của M trong sản phẩm của phản ứng giữa M với axit HCl có thể khác nhau.
Do đó ta gọi n là hóa trị của M thể hiện khi phản ứng với axit HCl.
![]()
Áp dụng định luật bào toàn mol electron, ta có:
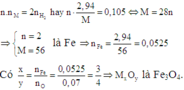
Đáp án D.