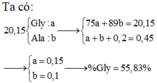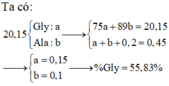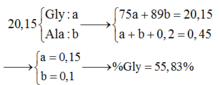cho 27 g R(OH)n tác dụng vừa đủ với 400ml dung dịch HCl 3,65% ( d= 1,5 g/ml) thu đc dd Y. Tìm R và tính % khối lượng chất tan trong Y

Những câu hỏi liên quan
Hoà tan hoàn toàn m g bột Cu trong 800 g dung dịch HNO3 được dung dịch Y và 2,24 lit khí NO (đktc). Y tác dụng vừa đủ với 300 ml dung dịch NaOH 2M được kết tủa R. Sau khi nung R đến khối lượng không đổi thu được 20 g chất rắn.
a. Tính khối lượng Cu ban đầu.
b. Tính khối lượng các chất trong Y và nồng độ % của dung dịch HNO3 đã dùng
nNO = 2,24/22,4 = 0,1 mol; nNaOH = 0,3.0,2 = 0,06 mol
a. Khi cho Y tác dụng với dung dịch NaOH thu được kết tủa R chỉ chứa Cu(OH)2.
Chất rắn thu được khi nung là CuO => nCuO = 20/80 = 0,25 mol
=> nCu(OH )2 = nCuO = 0,25 mol.
Theo định luật bảo toàn nguyên tố:
nCu (ban đầu) = nCu (trong CuO) = 0,25 mol => mCu = 0,25.64 = 16 g
b. Trong X, nCu2+ = nCu(OH)2 = 0,25 mol => mCu(NO3)2 = 188.0,25 = 47 g
Cu → Cu2+ + 2e
0,25 mol 0,5 mol
Mà: N+5 + 3e → N+2
0,3 mol 0,1 mol
Vậy chứng tỏ phản ứng của Cu và HNO3 phải tạo ra NH4NO3.
ne (Cu nhường) = Σne nhận = 0,5 mol => ne nhận N+5 →N-3 = 0,5 – 0,3 = 0,2 mol
N+5 + 8e → N-3
0,2 mol 0,025 mol
nNH4NO3 = 0,025 mol => mNH4NO3 = 80.0,025 = 2 g
Theo định luật bảo toàn nguyên tố:
n HNO3 pư = nN (trong Cu(NO3)2 ) + nN (trong NO) + nN (trong NH4NO3)
= 2nCu(NO3)2 + nNO + 2nNH4NO3 = 0,65 mol
Nếu sử dụng công thức tính nhanh ở trên ta có:
nHNO3 pư = 4.nNO + 10.nNH4NO3 = 4.0,1 + 10.0,25 = 0,65 mol
mHNO3 = 63.0,65 = 40,95 g => C% = 40,95/800.100% = 5,12%
Đúng 3
Bình luận (1)
C1: Cho 10.8 g hỗn hợp gồm Mg và Fe tác dụng với 102.2 g dung dịch HCl 20% thu được dung dịch A và 5.6 l khí- tính % khối lượng của mỗi kim loại trong hỗn hợp- tính % nồng độ các chất trong dung dịch A- cho dung dịch A tác dụng với lượng dư dung dịch AgNO3. tính khối lượng kết tủa.C2: cho 1.74 g hỗn hợp A gồm nhôm và magie tác dụn vừa đủ 100ml dung dịch HCl có D 1.05 g/ml, thu được 1.792l H2 và dung dịch X.- tính % khối lượng của nhôm- cho dung dịch X tác dụng vừa đủ 50 g dung dịch AgNO3 thu đư...
Đọc tiếp
C1: Cho 10.8 g hỗn hợp gồm Mg và Fe tác dụng với 102.2 g dung dịch HCl 20% thu được dung dịch A và 5.6 l khí
- tính % khối lượng của mỗi kim loại trong hỗn hợp
- tính % nồng độ các chất trong dung dịch A
- cho dung dịch A tác dụng với lượng dư dung dịch AgNO3. tính khối lượng kết tủa.
C2: cho 1.74 g hỗn hợp A gồm nhôm và magie tác dụn vừa đủ 100ml dung dịch HCl có D = 1.05 g/ml, thu được 1.792l H2 và dung dịch X.
- tính % khối lượng của nhôm
- cho dung dịch X tác dụng vừa đủ 50 g dung dịch AgNO3 thu được dung dịch Y. Tính C% dung dịch Y
C3: hòa tan hoàn toàn 10.3 gam hỗn hợp Mg và MgCO3 trong 100g dung dịch HCl 18.25% thu được dung dịch X và 4.48l hỗn hợp khí Y
- tính % khối lượng mỗi chất trong hỗn hợp ban đầu
- tính nồng độ % của các chất trong dung dịch X
- cho toàn bộ lượng khí H2 trong Y tác dụng với 1.68 l khí Cl2 (hiệu suất phản ứng 80%) rồi hấp thụ toàn bộ sản phẩm thu được vào dung dịch AgNO3 dư thì thu được bao nhiêu gam kết tủa?
cho m gam (mg+al2o3) tác dụng vừa đủ với 400ml đ HCL 2( khối lượng riêng là 1.2gam/ml) thu được dung dịch X và 2.24dm^3 khí sinh ra ở đktc. tính m và nồng độ % các chất tan trong dung dịch x
PTHH: \(Mg+2HCl\rightarrow MgCl_2+H_2\uparrow\)
\(Al_2O_3+6HCl\rightarrow2AlCl_3+3H_2O\)
Ta có: \(\left\{{}\begin{matrix}\Sigma n_{HCl}=0,4\cdot2=0,8\left(mol\right)\\n_{H_2}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}n_{Mg}=0,1mol\\n_{Al_2O_3}=0,1mol\end{matrix}\right.\) \(\Rightarrow\left\{{}\begin{matrix}m_{Al_2O_3}=0,1\cdot102=10,2\left(g\right)\\m_{Mg}=0,1\cdot24=2,4\left(g\right)\end{matrix}\right.\)
\(\Rightarrow m_{hh}=10,2+2,4=12,6\left(g\right)\)
Theo PTHH: \(\left\{{}\begin{matrix}n_{MgCl_2}=n_{Mg}=0,1mol\\n_{AlCl_3}=2n_{Al_2O_3}=0,2mol\end{matrix}\right.\) \(\Rightarrow\left\{{}\begin{matrix}m_{MgCl_2}=0,1\cdot95=9,5\left(g\right)\\m_{AlCl_3}=0,2\cdot133,5=26,7\left(g\right)\end{matrix}\right.\)
Mặt khác: \(\left\{{}\begin{matrix}m_{ddHCl}=400\cdot1,2=480\left(g\right)\\m_{H_2}=0,1\cdot2=0,2\left(g\right)\end{matrix}\right.\)
\(\Rightarrow m_{dd}=m_{hh}+m_{ddHCl}-m_{H_2}=492,4\left(g\right)\)
\(\Rightarrow\left\{{}\begin{matrix}C\%_{MgCl_2}=\dfrac{9,5}{492,4}\cdot100\%\approx1,93\%\\C\%_{AlCl_3}=\dfrac{26,7}{492,4}\cdot100\%\approx5,42\%\end{matrix}\right.\)
Đúng 1
Bình luận (0)
Cho 20,15 g hỗn hợp X gồm (NH2CH2 COOH và CH3CH(NH2)COOH) tác dụng với 200 ml dung dịch HCl 1M thu được dung dịch Y. Y tác dụng vừa đủ với 450 ml dung dịch NaOH 1M. Phần trăm khối lượng của mỗi chất trong X là A.58,53%và41,47%. B.55,83%và44,17%. C.53,58%và46,42%. D.52,59%và47,41%.
Đọc tiếp
Cho 20,15 g hỗn hợp X gồm (NH2CH2 COOH và CH3CH(NH2)COOH) tác dụng với 200 ml dung dịch HCl 1M thu được dung dịch Y. Y tác dụng vừa đủ với 450 ml dung dịch NaOH 1M. Phần trăm khối lượng của mỗi chất trong X là
A.58,53%và41,47%.
B.55,83%và44,17%.
C.53,58%và46,42%.
D.52,59%và47,41%.
Cho 20,15 g hỗn hợp X gồm (NH2CH2COOH và CH3CH(NH2)COOH) tác dụng với 200 ml dung dịch HCl 1M thu được dung dịch Y. Y tác dụng vừa đủ với 450 ml dung dịch NaOH 1M. Phần trăm khối lượng của mỗi chất trong X là A. 58,53% và 41,47%. B. 55,83% và 44,17%. C. 53,58% và 46,42%. D. 52,59% và 47,41%.
Đọc tiếp
Cho 20,15 g hỗn hợp X gồm (NH2CH2COOH và CH3CH(NH2)COOH) tác dụng với 200 ml dung dịch HCl 1M thu được dung dịch Y. Y tác dụng vừa đủ với 450 ml dung dịch NaOH 1M. Phần trăm khối lượng của mỗi chất trong X là
A. 58,53% và 41,47%.
B. 55,83% và 44,17%.
C. 53,58% và 46,42%.
D. 52,59% và 47,41%.
Cho 20,15 g hỗn hợp X gồm (NH2CH2 COOH và CH3CH(NH2)COOH) tác dụng với 200 ml dung dịch HCl 1M thu được dung dịch Y. Y tác dụng vừa đủ với 450 ml dung dịch NaOH 1M. Phần trăm khối lượng của mỗi chất trong X là A. 58,53% và 41,47%. B. 55,83% và 44,17%. C. 53,58% và 46,42%. D. 52,59% và 47,41%.
Đọc tiếp
Cho 20,15 g hỗn hợp X gồm (NH2CH2 COOH và CH3CH(NH2)COOH) tác dụng với 200 ml dung dịch HCl 1M thu được dung dịch Y. Y tác dụng vừa đủ với 450 ml dung dịch NaOH 1M. Phần trăm khối lượng của mỗi chất trong X là
A. 58,53% và 41,47%.
B. 55,83% và 44,17%.
C. 53,58% và 46,42%.
D. 52,59% và 47,41%.
Cho 20,15 g hỗn hợp X gồm (H2NCH2COOH và CH3CH(NH2)COOH) tác dụng với 450 ml dung dịch HCl 1M thu được dung dịch Y. Y tác dụng vừa đủ với 200 ml dung dịch NaOH 1M. Phần trăm khối lượng của mỗi chất trong X là: A. 55,83% và 44,17%. B. 53,58% và 46,42%. C. 58,53% và 41,47%. D. 52,59% và 47,41%.
Đọc tiếp
Cho 20,15 g hỗn hợp X gồm (H2NCH2COOH và CH3CH(NH2)COOH) tác dụng với 450 ml dung dịch HCl 1M thu được dung dịch Y. Y tác dụng vừa đủ với 200 ml dung dịch NaOH 1M. Phần trăm khối lượng của mỗi chất trong X là:
A. 55,83% và 44,17%.
B. 53,58% và 46,42%.
C. 58,53% và 41,47%.
D. 52,59% và 47,41%.
Tương tự công thức câu 18 ta thu được:
nhh = 0,25 (mol)
Gọi x và y lần lượt là số mol của H2NCH2COOH va CH3CH(NH2)COOH. Ta có hệ sau:
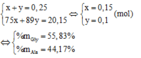
Đúng 0
Bình luận (0)
Cho m(g) Mg tác dụng vừa đủ 400g dung dịch HCl 3,65 a) Viết PTHH xảy ra và tính thể tích H2 thu được ở Đktc b) Tính khối lượng Mg tác dụng c) Tính khối lượng dung dịch MgO2 sau phản ứng và C% dd Mgcl2
mHCl= 3,65%.400= 14,6(g) => nHCl=14,6/36,5=0,4(mol)
a) PTHH: Mg +2 HCl -> MgCl2 + H2
0,2__________0,4_____0,2____0,2(mol)
V(H2,đktc)=0,2.22,4=4,48(l)
b)mMg=0,2.24=4,8(g)
c) mMgCl2= 0,2.95=19(g)
mddMgCl2= 400+4,8 - 0,2.2= 404,4(g)
=> C%ddMgCl2= (19/404,4).100=4,698%
Đúng 2
Bình luận (0)
cho 5,4g kim loại R có hóa trị n không đổi tác dụng vừa đủ vs V ml dung dịch H2SO4 loãng 24,5% ( KLR d= 1,08g/ml), sau phản ứng thu được dung dịch A và 6,72l khí H2 ở đktc. Xác định kim loại R, tính V và % khối lượng chất tan trong dung dịch A