Một hỗn hợp gồm Fe2(SO4)3 và MgSO4, trong đó số nguyên tử oxi chiếm 32/ 47 tổng số nguyên tử có trong hỗn hợp. Tính phần trăm theo khối lượng mỗi chất trong hỗn hợp.

Những câu hỏi liên quan
Một hỗn hợp X gồm FeSO4 và Al2(SO4)3,trong đó số ngyên tử oxi trong X chiếm 20/29 tổng số nguyên tử trong các nguyên tố trong hỗn hợp X. Tính thành phàn % khỗi lượng mỗi chất trong hỗn hợp X.
Gọi số mol FeSO4, Al2(SO4)3 là a, b (mol)
nFe = a (mol)
nAl = 2b (mol)
nS = a + 3b (mol)
nO = 4a + 12b (mol)
Có: \(\dfrac{n_O}{\Sigma n}=\dfrac{4a+12b}{a+2b+a+3b+4a+12b}=\dfrac{20}{29}\)
=> a = 2b
\(\left\{{}\begin{matrix}\%m_{FeSO_4}=\dfrac{152a}{152a+342b}.100\%=\dfrac{152.2b}{152.2b+342b}.100\%=47,059\%\\\%m_{Al_2\left(SO_4\right)_3}=100\%-47,059\%=52,941\%\end{matrix}\right.\)
Đúng 3
Bình luận (0)
Một hỗn hợp X gồm Al2(SO4)3 và K2SO4 trong đó số nguyên tử oxi chiếm 20/31 tổng số nguyên tử có trong hỗn hợp a,Tính % theo khối lượng mỗi muối trong trong hỗn hợp b,cho 82,8 g hỗn hợp X tác dụng 400ml đúng dịch Ba(OH)2 1M thu được m gam .Tính m
Một hỗ hợp gồm Al2(SO4)3 và K2SO4, trong đó số nguyên tử oxi chiếm 20/31 tổng số nguyên tử trong hỗn hợp. Tính phần trăm theo khối lượng của mỗi chất trong hỗn hợp.
Một hỗn hợp gồm CuSO4 và Fe2(SO4)3, trong đó % khối lượng S là 22,61%.
a/ Tính % khối lượng O trong hỗn hợp.
b/ Biết số nguyên tử Fe trong hỗn hợp là 18.1024.
- Tính số mol từng chất trong hỗn hợp.
- Tính khối lượng hỗn hợp.
a) Giả sử có 100 gam hỗn hợp
=> \(m_S=\dfrac{100.22,61}{100}=22,61\left(g\right)\)
=> \(n_S=\dfrac{22,61}{32}=\dfrac{2261}{3200}\left(mol\right)\)
Mà nO = 4nS
=> \(n_O=\dfrac{2261}{800}\left(mol\right)\)
\(\%m_O=\dfrac{\dfrac{2261}{800}.16}{100}.100\%=45,22\%\)
b)
\(n_{Fe}=\dfrac{18.10^{24}}{6.10^{23}}=30\left(mol\right)\)
=> \(n_{Fe_2\left(SO_4\right)_3}=15\left(mol\right)\)
Gọi số mol CuSO4 là x (mol)
=> mhh = 160x + 6000 (g)
nS = 15.3 + x = x + 45 (mol)
\(\%m_S=\dfrac{\left(x+45\right).32}{160x+6000}.100\%=22,61\%\)
=> x = 20 (mol)
mhh = 160.20 + 6000 = 9200 (g)
Đúng 4
Bình luận (0)
Hỗn hợp gồm MgSO4 và Fe2(SO4)3, trong đó % khối lượng nguyên tố oxi là 25%.
a/ Tính % khối lượng nguyên tố lưu huỳnh trong hỗn hợp.
b/ Tính % khối lượng nguyên tố oxi trong hỗn hợp.
c/ Từ 64 gam hỗn hợp, có thể điều chế được bao nhiêu gam hỗn hợp Mg và Fe? (2 cách).
a)
Giả sử có 100 gam hỗn hợp
\(m_O=\dfrac{25.100}{100}=25\left(g\right)\)
=> \(n_O=\dfrac{25}{16}=1,5625\left(mol\right)\)
Mà nO = 4.nS
=> \(n_S=\dfrac{1,5625}{4}=\dfrac{25}{64}\left(mol\right)\)
\(\%m_S=\dfrac{\dfrac{25}{64}.32}{100}.100\%=12,5\%\)
b) Đề bài cho rồi mà bn :)
c)
C1: %mkim loại = \(100\%-12,5\%-25\%=62,5\%\)
=> mkim loại = \(\dfrac{64.62,5}{100}=40\left(g\right)\)
C2:
\(m_S=\dfrac{64.12,5}{100}=8\left(g\right)\)
\(m_O=\dfrac{64.25}{100}=16\left(g\right)\)
=> mkim loại = 64 - 8 - 16 = 40 (g)
Đúng 1
Bình luận (0)
1 hh gồm Al2(SO4)3 và K2SO4, trong đó số nguyên tử O2 chiếm 20/31 tổng số nguyên tử có trong hỗn hợp. Tính % theo khối lượng mỗi muối trong hh
Gọi số nguyên tử của \(Al_2(SO_4)_3\) và \(K_2SO_4\) lần lượt là x và y.
Số nguyên tử của \(Al_2(SO_4)_3\) là \(2+3+4\cdot3=17x\)
Số nguyên tử của \(K_2SO_4\) là \(2+1+4=7y\)
Mà số nguyên tử \(O_2\) trong hỗn hợp là \(4\cdot3x+4y=12x+4y\)
Theo bài: \(n_{O_2}=\dfrac{20}{31}n_{hh}\)
\(\Rightarrow12x+4y=\dfrac{20}{31}\left(17x+7y\right)\)
\(\Rightarrow y=2x\)
Có \(\%m_{Al_2\left(SO_4\right)_3}=\dfrac{342x}{342x+174y}\cdot100\%=\dfrac{342x}{342x+174\cdot2x}\cdot100\%=49,56\%\)
\(\%m_{K_2SO_4}=100\%-49,56\%=50,44\%\)
Đúng 3
Bình luận (0)
\(\%m_{\dfrac{O}{Nhôm.sunfat}}=\dfrac{4.16.3}{342}.100\approx56,14\%\\ \%m_{\dfrac{O}{Kali.sunfat}}=\dfrac{4.16}{174}.100\approx36,78\%\\ Gọi:a=n_{Al_2\left(SO_4\right)_3};b=n_{K_2SO_4}\left(a,b>0\right)\\ \Rightarrow Vì:m_{\dfrac{O}{hh}}=\dfrac{20}{31}\\ \Leftrightarrow\dfrac{a.12+b.4}{17a+7b}.100\%=\dfrac{20}{31}\\ \Leftrightarrow32a=16b\\ \Leftrightarrow\dfrac{a}{b}=\dfrac{16}{32}=\dfrac{1}{2}\\ \Leftrightarrow b=2a\\ \%m_{\dfrac{K_2SO_4}{hh}}=\dfrac{174.2a}{174.2a+342.a}.100\%\approx50,435\%\\ \Rightarrow\%m_{\dfrac{Al_2\left(SO_4\right)_3}{hh}}\approx49,565\%\)
Đúng 3
Bình luận (0)
Một hỗn hợp gồm Al2(SO4)3 và K2SO4, trong đó Số nguyên tử oxi chiếm 20/31 tổng số nguyên tử có trong hỗn hợp. Hoà tan hỗn hợp trên vào nước rồi cho tác dụng với dung dịch BaCl2 dư, hỏi khối lượng kết tủa thu được gấp bao nhiêu lần khối lượng hỗn hợp ban đầu: A. 1,788 lần. B. 1,488 lần. C. 1,688 lần. D. 1,588 lần.
Đọc tiếp
Một hỗn hợp gồm Al2(SO4)3 và K2SO4, trong đó Số nguyên tử oxi chiếm 20/31 tổng số nguyên tử có trong hỗn hợp. Hoà tan hỗn hợp trên vào nước rồi cho tác dụng với dung dịch BaCl2 dư, hỏi khối lượng kết tủa thu được gấp bao nhiêu lần khối lượng hỗn hợp ban đầu:
A. 1,788 lần.
B. 1,488 lần.
C. 1,688 lần.
D. 1,588 lần.
Đáp án C
Gọi
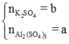
Áp dụng định luật bảo toàn nguyên tố cho O, Al, K và S ta có:
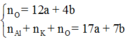
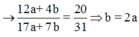
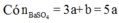
Nên
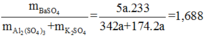
Đáp án C
Đúng 0
Bình luận (0)
Một hỗn hợp gồm Al2(SO4)3 và K2SO4, trong đó số nguyên tử oxi chiếm 20/31 tổng số nguyên tử có trong hỗn hợp. Hoà tan hỗn hợp trên vào nước rồi cho tác dụng với dung dịch BaCl2 dư, hỏi khối lượng kết tủa thu được gấp bao nhiêu lần khối lượng hỗn hợp ban đầu: A. 1,588 lần B. 1,788 lần C. 1,488 lần D. 1,688 lần
Đọc tiếp
Một hỗn hợp gồm Al2(SO4)3 và K2SO4, trong đó số nguyên tử oxi chiếm 20/31 tổng số nguyên tử có trong hỗn hợp. Hoà tan hỗn hợp trên vào nước rồi cho tác dụng với dung dịch BaCl2 dư, hỏi khối lượng kết tủa thu được gấp bao nhiêu lần khối lượng hỗn hợp ban đầu:
A. 1,588 lần
B. 1,788 lần
C. 1,488 lần
D. 1,688 lần
Đáp án : D
Giả sử có 1 mol hỗn hợp gồm x mol Al2(SO4)3 và (1 – x) mol K2SO4
=> tổng số mol các nguyên tố
= nAl + nK + nS + nO = 2x + 2.(1 – x) + (3x + 1 – x) + 4.( 3x + 1 – x) = 10x + 7
=>nO = nngto.%nO
=> 4.(3x + 1 – x) = (10x + 7).20/31
=> x = 1/3 mol
=> mhh đầu = 230g
Khi phản ứng với BaCl2 thì nBaSO4 = nSO4 = 3x + 1 – x = 5/3 mol
=> mBaSO4 = 388,3g
=> mBaSO4 : mhh = 1,688 lần
Đúng 0
Bình luận (0)
cho 32 gam Fe2(SO4)3
a. hãy tính số nguyên tử có trong lượng phân tử chất đó
b. tính thể tích khí Oxi ở đktc để có số nguyên tử oxi bằng số nguyên tử oxi có trong 32 gam hỗn hợp chất trên