Một hidro co khối lượng mol phan tu là 78g . Tìm tên kim loại trong hidroxit do

Những câu hỏi liên quan
cho phản ứng hóa học sau .cho kim loại natri tác dụng với nước tạo ra natri hidroxit và khí hidro
a, lập PTHH
b, tính khối lượng của natri tham gia phản ứng nếu khối lượng của nước , natri hidroxit và khí hidro trong phản ứng trên lần lượt là 36g ,80g,3g
a) PTHH: 2 Na + 2 H2O -> 2 NaOH + H2
b) Theo Định luật bảo toàn khối lượng, ta có:
mNa+mH2O=mNaOH +mH2
<=> mNa+ 36=80+3
<=>mNa= 47(g)
(Thật ram em xem lại nha, tính toán thì ra 47 gam, nhưng thực tế mà nói thì anh nghĩ ra 46 gam và 2 gam nước, coi lại chỗ KL nước he)
Đúng 1
Bình luận (0)
\(Na+H_2O\rightarrow NaOH+\dfrac{1}{2}H_2\)
\(b.\)
Bảo toàn khối lượng :
\(m_{Na}=80+3-36=47\left(g\right)\)
Đúng 0
Bình luận (0)
Cho biết khối lượng mol một oxit của kim loại là 160 g/mol, thành phần về khối lượng của kim loại trong oxit đó là 70%. Lập công thức hóa học của oxit. Gọi tên oxit đó
\(CT:M_xO_y\)
\(\%M=\dfrac{xM}{160}\cdot100\%=70\%\)
\(\Rightarrow xM=112\)
\(\text{Với : }\) \(x=2\Rightarrow M=56\)
\(M=56\cdot2+16y=160\left(g\text{/}mol\right)\)
\(\Rightarrow y=3\)
\(CT:Fe_2O_3:\text{Sắt (III) oxit}\)
Đúng 4
Bình luận (0)
Cho biết khối lượng mol của một oxit kim loại là 160gam, thành phần về khối lượng của kim loại trong oxit đó là 70%. Lập công thức hóa học của oxit. Gọi tên oxit kim loại đó.
Đặt công thức của oxit kim loại là MxOy
%mO = 100% - 70% = 30%
⇒ mO = 12y = 160.30% = 48
⇒ y = 3
mM = 160.70% = 112g = M.x (với M là phân tử khối của kim loại M)
Áp dụng quy tắc hóa trị ta có:
a.x = 2.3 = 6 (với a là hóa trị của M; a = 1; 2; 3)
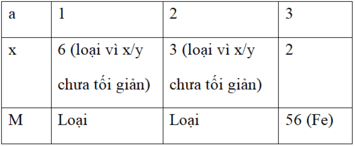
⇒ M là kim loại Sắt.
Vậy công thức hóa học của oxit kim loại là Fe2O3 (Sắt (III) oxit).
Đúng 2
Bình luận (0)
Cho biết khối lượng mol một oxit của kim loại là 160g/mol, thành phần về khối lượng của kim loại trong oxit đó là 70%. Lập công thức hoá học của oxit. Gọi tên oxit đó.
Cho biết khối lượng mol của một oxit của kim loại là 160 g/mol, thành phần về khối lượng của kim loại trong oxit đó là 70. Lập công thức hóa học của oxit. Gọi tên oxit đó.
Khối lượng của kim loại có trong oxit kim loại:
MKL = 112 g
Khối lượng nguyên tố oxi: mO = 160 – 112 = 48g
Đặt công thức hóa học của oxit kim loại là MxOy, ta có:
MKL. x = 112 => nếu x = 2 thì M = 56. Vậy M là Fe
16y = 48 => y = 3
Vậy CTHH: Fe2O3, đó là sắt (III) oxit
Đúng 0
Bình luận (0)
Hoan hô , Học sinh tự hỏi tự trả lời
Hoan hô oooooooooooooooooooooooooooo
Đúng 2
Bình luận (0)
Cho biết khối lượng mol của một oxit của kim loại là 160 g/mol, thành phần về khối lượng của kim loại trong oxit đó là 70. Lập công thức hóa học của oxit. Gọi tên oxit đó.
Khối lượng của kim loại có trong oxit kim loại:
MKL = 112 g
Khối lượng nguyên tố oxi: mO = 160 – 112 = 48g
Đặt công thức hóa học của oxit kim loại là MxOy, ta có:
MKL. x = 112 => nếu x = 2 thì M = 56. Vậy M là Fe
16y = 48 => y = 3
Vậy CTHH: Fe2O3, đó là sắt (III) oxit
Đúng 0
Bình luận (0)
Gọi Công thức hóa học của oxit đó là : MxOy
Ta có : khối lượng của M trong 1 mol là : 160 . 70 : 100 = 112(g)
=> khối lượng của Oxi trong 1 mol là : 160 - 112 = 48(g)
=> số nguyên tử Oxi có trong 1 phân tử Oxit là : 48 : 16 = 3 (nguyên tử)
=>y = 3 => M có hóa trị là III
Ta có : III . x = 3 . II
=> x = 2
=> MxOy = M2O3
=> Mkim loại M là 112 : 2 = 56 (g/mol)
=> M = Fe
Vậy tên Oxit đó là : Fe2O3
Đúng 1
Bình luận (0)
đề bài bị sai :
Cho biết khối lượng mol của một oxit của kim loại là 160 g/mol, thành phần về khối lượng của kim loại trong oxit đó là 70%. Lập công thức hóa học của oxit. Gọi tên oxit đó.
Đúng 1
Bình luận (1)
Xem thêm câu trả lời
A là hỗn hợp hai kim loại Ba và Mg, cho a gam A vào nước dư thì thu được 2,24 lít khí hidro (đktc). CŨng cho a gam A nhưng cho vào dung dịch axit clohidric dư thì thu được 4,48 lít khí hidro và một dung dịch B.
a) Tính a
b) Thêm vào B 0,1 mol axit sunfuric, sau đó thêm 0,3 mol natri hidroxit. Tính khối lượng phần kết tủa thu được
a. Lúc cho A vào nước:
\(Ba+2H_2O\rightarrow Ba\left(OH\right)_2+H_2\uparrow\left(1\right)\)
Theo phương trình (1)
\(n_{Ba}=n_{H_2\left(1\right)}=\dfrac{2,24}{22,4}=0,1mol\)
Lúc cho A vào HCl dư:
\(Ba+2HCl\rightarrow BaCl_2+H_2\uparrow\left(2\right)\)
\(Mg+2HCl\rightarrow MgCl_2+H_2\uparrow\left(3\right)\)
\(n_{H_2\left(2+3\right)}=\dfrac{4,48}{22,4}=0,2mol\)
\(\rightarrow n_{Ba}+n_{Mg}=0,2mol\)
\(\rightarrow n_{Mg}=0,1mol\)
\(\rightarrow a=m_A=0,1.24+0,1.137=16,1g\)
b. Dung dịch B:
\(MgCl_2:0,1mol\) và \(BaCl_2:0,1mol\)
\(BaCl_2+H_2SO_4\rightarrow BaSO_4\downarrow+2HCl\)
Xét \(n_{BaCl_2}=n_{H_2SO_4}\rightarrow P/ứ\) hoàn toàn
\(HCl+NaOH\rightarrow NaCl+H_2O\)
\(MgCl_2+2NaOH\rightarrow Mg\left(OH\right)_2\downarrow+2NaCl\)
Từ các phương trình \(n_{BaSO_4}=0,1mol;n_{Mg\left(OH\right)_2}=0,05mol\)
\(\rightarrow m\downarrow=0,1.233+0,05.58=26,2g\)
Đúng 0
Bình luận (0)
Cho kim loại K phản ứng vừa đủ với 7,2 gam nước, sau phản ứng thu được 18,4 gam kali hidroxit (KOH) và giải phóng 0,4 gam khí hidro H2. Tính khối lượng kim loại kali dã phản ứng.
Áp dụng định luật bảo toàn khối lượng, ta có:
\(m_K+m_{H_2O}=m_{KOH}+m_{H_2}\)
\(\Leftrightarrow m_K=m_{KOH}+m_{H_2}-m_{H_2O}=18,4+0,4-7,2=11,6\left(g\right)\)
Đúng 1
Bình luận (1)
áp dụng định luật bảo toàn khối lượng, ta có:
\(m_K+m_{H_2O}=m_{KOH}+m_{H_2}\)
\(m_K+7,2=18,4+0,4\)
\(m_K+7,2=18,8\)
\(m_K=18,8-7,2=11,6g\)
vậy khối lượng Kali đã phản ứng là \(11,6g\)
Đúng 1
Bình luận (0)
Bài 1: ngâm một lá đồng trong 500ml dd AgNO3 đến khi phản ứng hoàn toàn. Lấy lá đồng ra làm khô , cân thì lấy khối lượng lá đồng tăng thêm 15,2g . Hãy xác định nồng độ của mol của dd bạc nitrat.Bài 2: cho 78g một kim loại A tác dụng với khí clo dư tạo thành 149g muối. Hãy xác định kim loại A, biết rằng A có hóa trị 1Bài 3: viết các PTHH :a, điều chế Zn từ ZnSO4 b, điều chế MgSO4 từ mỗi chất sau: Mg, MgCl2, MgO, MgCO3 các hóa chất cần thiết coi như đủ
Đọc tiếp
Bài 1: ngâm một lá đồng trong 500ml dd AgNO3 đến khi phản ứng hoàn toàn. Lấy lá đồng ra làm khô , cân thì lấy khối lượng lá đồng tăng thêm 15,2g . Hãy xác định nồng độ của mol của dd bạc nitrat.
Bài 2: cho 78g một kim loại A tác dụng với khí clo dư tạo thành 149g muối. Hãy xác định kim loại A, biết rằng A có hóa trị 1
Bài 3: viết các PTHH :
a, điều chế Zn từ ZnSO4
b, điều chế MgSO4 từ mỗi chất sau: Mg, MgCl2, MgO, MgCO3
các hóa chất cần thiết coi như đủ
Bài 1 :
Pt : \(Cu+2AgNO_3\rightarrow Cu\left(NO_3\right)_2+2Ag|\)
1 2 1 2
x 0,2 2x
Gọi x là số mol của Cu
Vì khối lượng của đồng tăng so với ban đầu nên ta có phương trình :
\(m_{Ag}-m_{Cu}=15,2\left(g\right)\)
\(108.2x-64.x=15,2\)
\(216x-64x=15,2\)
\(152x=15,2\)
⇒ \(x=\dfrac{15,2}{152}=0,1\)
\(n_{AgNO3}=\dfrac{0,1.2}{1}=0,2\left(mol\right)\)
500ml = 0,5l
\(C_{M_{ddAgNO3}}=\dfrac{0,2}{0,5}=0,4\left(M\right)\)
Chúc bạn học tốt
Đúng 2
Bình luận (1)


























