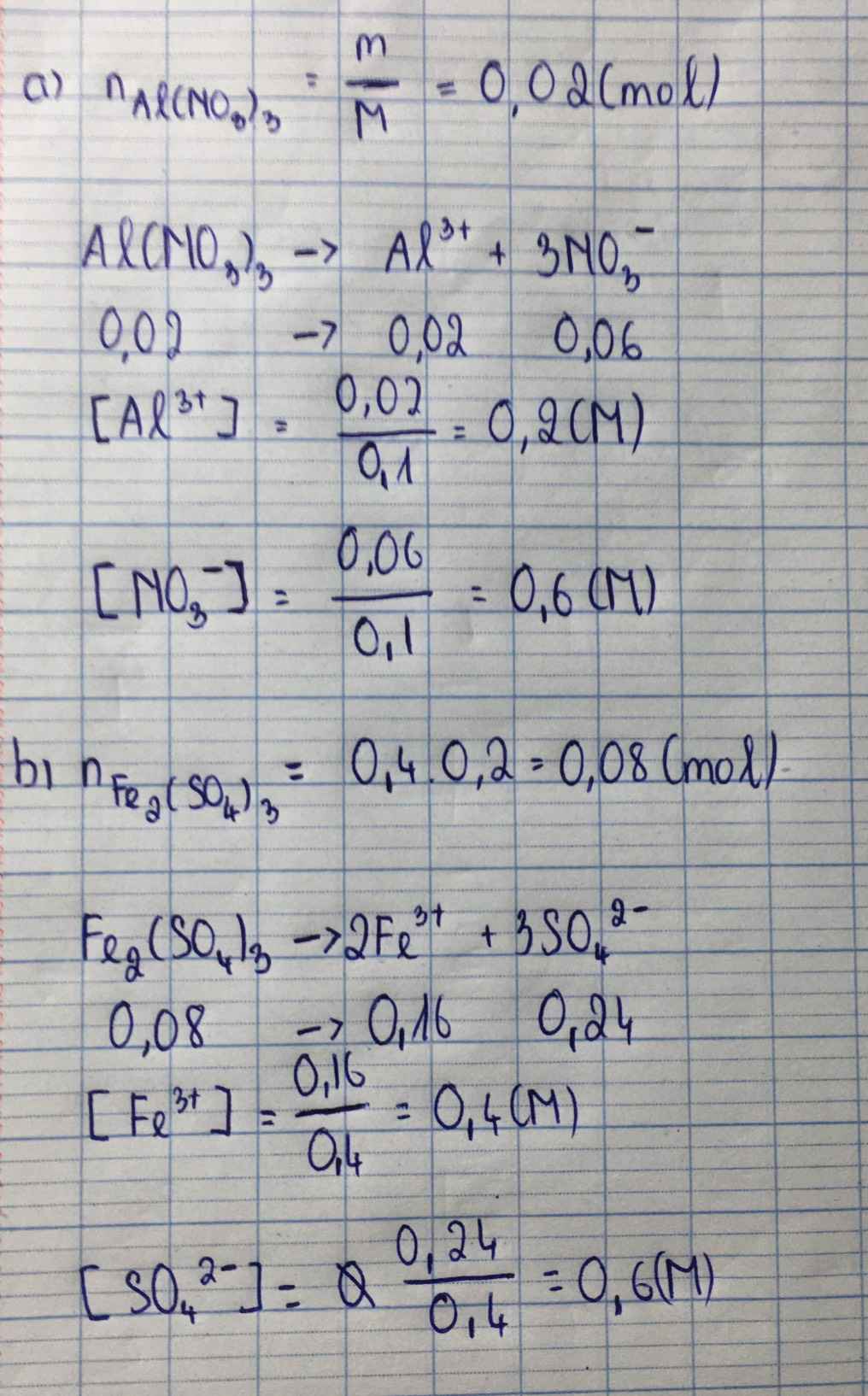Tính nồng độ mol/lít các ion trong các dung dịch sau a. Pha chế 100ml dung dịch vào 13,5 gam CuCl2 và 14,9 gam KCl

Những câu hỏi liên quan
Bài 4. Hòa tan 7,1 gam Na2SO4 ; 7,45 gam KCl ; 2,925 gam NaCl vào nước để được 1 lít dung dịch A.
Tính nồng độ mol/lít của mỗi ion trong dung dịch A.
Cần dùng bao nhiêu mol NaCl và bao nhiêu mol K2SO4 để pha thành 400 ml dung dịch muối có nồng độ ion như trong dung dịch A.
Có thể dùng 2 muối KCl và Na2SO4 để pha thành 400 ml dung dịch muối có nồng độ ion như dung dịch A được không?
a) Cần phải lấy bao nhiêu gam dung dịch CuCl2 10% và bao nhiêu gam dung dịch CuCl2 15,25% để pha thành 30 gam dung dịch CuCl2 13,5% (dung dịch B)
b) Hoà tan 1,61 gam kim loại Na vào 30 gam dung dịch B. Hãy tính nồng độ phần trăm của dung dịch NaCl trong dung dịch thu được sau phản ứng
Tính nồng độ mol/l các ion trong mỗi dd sau:
a) 100ml dd chứa 4,26 gam Al(NO3)3.
b) Tính nồng độ mol của ion Na+ trong dung dịch chứa NaNO3 0,1M,
Na2SO4 0,02M và NaCl 0,3M.
c) Dung dịch H2SO4 15% ( d= 1,1g/ml)
a) Ta có: \(n_{Al\left(NO_3\right)_3}=\dfrac{4,26}{213}=0,02\left(mol\right)\) \(\Rightarrow\left\{{}\begin{matrix}n_{Al^+}=0,02\left(mol\right)\\n_{NO_3^-}=0,06\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}\left[Al^+\right]=\dfrac{0,02}{0,1}=0,2\left(M\right)\\\left[NO_3^-\right]=\dfrac{0,06}{0,1}=0,6\left(M\right)\end{matrix}\right.\)
b) Ta có: \(\left[Na^+\right]=0,1+0,02\cdot2+0,3=0,304\left(M\right)\)
c) Bạn xem lại đề !!
Đúng 0
Bình luận (0)
Tính nồng độ mol/lit của các ion sau a, 100ml dung dịch chứa 4.26 gam al(no3)3 b, 400ml dung dịch Fe2(SO4)3 0,2M
Hoà tan 1,17 gam nacl vào 2,08 gam BaCl2 vào nước thu được 100ml dd X.Tính nồng độ mol các ion trong dung dịch X
\(n_{NaCl}=\dfrac{1,17}{58,5}=0,02\left(mol\right)\\ n_{BaCl_2}=\dfrac{2,08}{208}=0,01\left(mol\right)\\ \left[Na^+\right]=\dfrac{0,02}{0,1}=0,2\left(M\right)\\ \left[Ba^{2+}\right]=\dfrac{0,01}{0,1}=0,1\left(M\right)\\ \left[Cl^-\right]=\dfrac{0,02+0,01.2}{0,1}=0,4\left(M\right)\)
Đúng 2
Bình luận (0)
Hòa tan 7,1 gam Na2SO4, 7,45 gam kcl 2,925 g NaCl vào nước để được 1 lít dung dịch A
tính nồng độ mol trên lít của mỗi ion trong dung dịch A
cần dùng bao nhiêu mol NaCl và bao nhiêu mol K2SO4 để pha thành 400 ml dung dịch muối có nồng độ ion như trong dung dịch A
có thể dùng 2 muối kcl và Na2So4 để pha thành 400 ml dung dịch muối có nồng độ ion như dung dịch A được không
nNa+ = 0,05*2 + 0,05 = 0,15
->[Na+]=0,15/1=0,15(M)
nSO4 2- = 0,05 -> [SO4 2-] = 0,05
nCl- = 0,05 -> [Cl-] = 0,05
b)
Đặt x là mol Na+ ; y là mol Cl- ; z là mol SO4 2-
0,15=x*0,4 ->x=0,375
0,05 =y*0,4 -->y=1,25
0,05 = z*0,4 -> z=1,25
c)
Ko được
Vì để có nồng độ SO4 2- giốn ddX thì số mol Na2SO4 phải là 0,125
mà muốn có nồng độ Na+ giống dd X thì số mol Na2SO4 phải là 0,1875
=> mâu thuẫn
Cho dung dịch Ba(OH)2 đến dư vào 100ml dung dịch X có chứa các ion: NH4+, SO42-, NO3- thì có 23,3 gam một kết tủa được tạo thành và đun nóng thì chỉ có 6,72 lít (đktc) một chất khí thoát ra. Nồng độ mol của (NH4)2SO4 và NH4NO3 trong dung dịch X là bao nhiêu? A. 2M và 2M B. 1M và 1M C. 1M và 2M D. 2M và 2M
Đọc tiếp
Cho dung dịch Ba(OH)2 đến dư vào 100ml dung dịch X có chứa các ion: NH4+, SO42-, NO3- thì có 23,3 gam một kết tủa được tạo thành và đun nóng thì chỉ có 6,72 lít (đktc) một chất khí thoát ra. Nồng độ mol của (NH4)2SO4 và NH4NO3 trong dung dịch X là bao nhiêu?
A. 2M và 2M
B. 1M và 1M
C. 1M và 2M
D. 2M và 2M
Đáp án B
Ba2++ SO42- →BaSO4
0,1 ← 23,3/233
NH4++ OH- →NH3+ H2O
0,3← 0,3
Theo ĐLBT ĐT thì: nNO3(-)=0,1 mol
Vậy dung dịch X có 0,1 mol (NH4)2SO4 và 0,1 mol NH4NO3
Suy ra nồng độ mol (NH4)2SO4 1M và NH4NO3 1M
Đúng 0
Bình luận (0)
Điện phân dung dịch gồm 18,8 gam
Cu
NO
3
2
và 29,8 gam KCl (điện cực trơ, màng ngăn). Sau một thời gian khối lượng dung dịch giảm 17,15 gam so với ban đầu, thể tích dung dịch là 400 ml. Nồng độ mol/lít các chất trong dung dịch sau điện phân là: A.
KCl
0
,
5
M
;...
Đọc tiếp
Điện phân dung dịch gồm 18,8 gam Cu NO 3 2 và 29,8 gam KCl (điện cực trơ, màng ngăn). Sau một thời gian khối lượng dung dịch giảm 17,15 gam so với ban đầu, thể tích dung dịch là 400 ml. Nồng độ mol/lít các chất trong dung dịch sau điện phân là:
A. KCl = 0 , 5 M ; KNO 3 = 0 , 25 M ; KOH = 0 , 25 M
B. KCl = 0 , 25 M ; KNO 3 = 0 , 25 M ; KOH = 0 , 25 M
C. KCl = 0 , 375 M ; KNO 3 = 0 , 25 M ; KOH = 0 , 25 M
D. KCl = 0 , 25 M ; KNO 3 = 0 , 5 M ; KOH = 0 , 25 M
Cho 2.4 gam M vào 250ml dung dịch HCl 1M. Tính nồng độ mol/l của các ion trong dung dịch sau phản ứng.