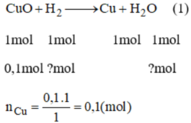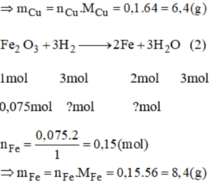Dùng H2 để khử 31,2 gam hỗn hợp CuO và Fe3O4 trong hỗn hợp, khối lượng Fe3O4 nhiều hơn khối lượng CuO là 15,2 gam. Tính khối lượng Fe và Cu thu được sau PƯ. (16.8,6.4)

Những câu hỏi liên quan
Dùng H2 để khử 31,2 gam hỗn hợp CuO và Fe3O4 trong hỗn hợp, khối lượng Fe3O4 nhiều hơn khối lượng CuO là 15,2 gam. Tính khối lượng Fe và Cu thu được sau PƯ. (16.8,6.4)
dùng tổng hiệu tính ra m CuO và m Fe3O4
m CuO = (31,2-15,2):2
m Fe3O4= 31,2-m CuO
viết PTHH của từng cái tác dụng vs H2 => tính ra mol của Fe và mol H2 => tính khối lượng Fe3O4 và khối lượng CuO => cộng lại
mình nghĩ vậy thôi... sai thì sorry nha
Đúng 0
Bình luận (0)
dùng \(H_2\) khử hoàn toàn 31,2 gam hỗn hợp CuO và \(Fe_3O_4\) trong hỗn hợp khối lượng \(Fe_3O_4\) lớn hơn khối lượng CuO là 15,2 gam.tính khối lượng Cu và Fe tạo ra
\(m_{Fe_3O_4} = \dfrac{31,2 + 15,2}{2} = 23,2(gam) \Rightarrow n_{Fe_3O_4} = \dfrac{23,2}{232} = 0,1(mol)\\ Fe_3O_4 + 4H_2 \xrightarrow{t^o} 3Fe + 4H_2O\\ n_{Fe} = 3n_{Fe_3O_4} = 0,3(mol) \Rightarrow m_{Fe} = 0,3.56 = 16,8(gam)\\ CuO + H_2 \xrightarrow{t^o} Cu + H_2O\\ n_{Cu} = n_{CuO} = \dfrac{31,2-23,2}{80} = 0,1(mol) \Rightarrow m_{Cu} = 0,1.64 = 6,4(gam)\)
Đúng 2
Bình luận (0)
Ta có:\(\left\{{}\begin{matrix}m_{CuO}+m_{Fe_3O_4}=31,2\\m_{Fe_3O_{\text{4}}}-m_{CuO}=15,2\end{matrix}\right.\)
\(\Leftrightarrow\left\{{}\begin{matrix}m_{Fe_3O_4}=23.2\\m_{CuO}=8\end{matrix}\right.\)
\(n_{Fe_3O_4}=\dfrac{23,2}{232}=0,1\left(mol\right)\)
\(n_{CuO}=\dfrac{8}{80}=0,1\left(mol\right)\)
\(Fe_3O_4+4H_2\underrightarrow{t^o}3Fe+4H_2O\)
\(0,1\rightarrow\) 0.3
\(CuO+H_2\underrightarrow{t^o}Cu+H_2O\)
\(0,1\rightarrow\) 0,1
\(m_{Fe}=0,3.56=16,8\left(g\right)\)
\(m_{Cu}=0,1.64=6,4\left(g\right)\)
Đúng 1
Bình luận (0)
Dùng H2 khử hết 31,2 g hỗn hợp gồm CuO và Fe2O3 . Trong hỗn hợp khối lượng CuO nhiều hơn CuO là 15,2 g . Tính khối lượng Cu và Fe thu được
Sửa đề 1 tí: Dùng H2 khử hết 31,2 g hỗn hợp gồm CuO và Fe2O3 . Trong hỗn hợp khối lượng Fe2O3 nhiều hơn CuO là 15,2 g . Tính khối lượng Cu và Fe thu được
PTHH:
\(CuO+H_2\rightarrow Cu+H_2O\uparrow\)
x.............x
\(Fe_2O_3+3H_2\rightarrow2Fe+3H_2O\)
y...............3y
Gọi x, y lần lượt là số mol của CuO, \(Fe_2O_3\)
Theo đề bài: Khử hết 31,2g g hỗn hợp gồm CuO và \(Fe_2O_3\), ta có:
\(80x+160y=31,2\left(1\right)\)
Trong hỗn hợp, \(Fe_2O_3\) 15,2g , ta có:
\(160y-80x=15,2\left(2\right)\)
Từ (1) (2) \(\Rightarrow\) Ta có hệ PT: \(\left\{{}\begin{matrix}80x+160y=31,2\\160y-80x=15,2\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}x=0,154\\y=0,118\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}m_{Cu}=0,154.64=9,856\left(g\right)\\m_{Fe}=0,118.56=6,608\left(g\right)\end{matrix}\right.\)
Đúng 0
Bình luận (0)
Cho 31,3 gam CuO và Fe3O4 trong đó Fe3O4 hơn CuO là 15,2 gam . dùng H2 khử hỗn hợp trên
a, tính khối lượng đồng và sắt thu đk b, tính thể tích H2 tham gia tất cả là bao nhiêu lít (đktc)a) Ta giải hệ: \(m_{CuO}+m_{Fe_2O_3}=37,6\) và \(m_{CuO}-m_{Fe_2O_3}=-15,2\)
\(m_{CuO}=8,05(g) \) ; \( m_{Fe_{2}O_{3}}=23,25(g)\)\(\Rightarrow\) \(n_{CuO}\)=0,1(mol) và \(n_{Fe_3O_4}\)=0,1(mol) CuO+H2 \(\rightarrow\) H2O+Cu(1)\(\Rightarrow\) \(n_{H_2\left(1\right)}\)=\(n_{CuO}\)=0,1(mol)và tiếp theo là phương trình \(Fe_3O_4\) tác dụng với \(H_2\): 4H2+Fe2O3\(\rightarrow\)3Fe+4H2O(2)\(\Rightarrow\) \(n_{H_2\left(2\right)}\)=\(4n_{CuO}\)=0,4(mol)\(\Rightarrow\)\(n_{H_2}\)=0,4+0,1=0,5(mol)\(\Rightarrow\)V=11,2(l)
Đúng 0
Bình luận (1)
Bài 6: Cho H2 khử 20 gam hỗn hợp Fe2O3 và CuO trong đó CuO chiếm 40% khối lượng.
a) Tính khối lượng Fe và khối lượng Cu thu được sau phản ứng?
b) Tính thể tích khí Hiđro (đktc) cần dùng?
a) \(m_{CuO}=\dfrac{20.40}{100}=8\left(g\right)\) => \(n_{CuO}=\dfrac{8}{80}=0,1\left(mol\right)\)
\(m_{Fe_2O_3}=20-8=12\left(g\right)\) => \(n_{Fe_2O_3}=\dfrac{12}{160}=0,075\left(mol\right)\)
PTHH: CuO + H2 --to--> Cu + H2O
0,1--->0,1------>0,1
Fe2O3 + 3H2 --to--> 2Fe + 3H2O
0,075--->0,225----->0,15
=> mCu = 0,1.64 = 6,4 (g)
=> mFe = 0,15.56 = 8,4 (g)
b) \(V_{H_2}=\left(0,1+0,225\right).22,4=7,28\left(l\right)\)
Đúng 4
Bình luận (0)
giúp em câu này với ạ,em đang cần gấp.em cảm ơn.
Khí hidro khử 56 gam hỗn hợp gồm CuO và fe2o3 trong hỗn hợp khối lượng fe2o3 nhiều hơn khối lượng CuO là 8 g
A/ tính khối lượng fe và cu thu được
B/tính thể tích khí hiđro sinh ra
Có 31,2(g) hỗn hợp CuO và Fe3O4 trong đó Fe3O4 hơn CuO 15,2(g).dùng H2 khử hỗn hợp đó .Tính
a)nKhoois lượng mỗi kim loại thu được
b) thể tích H2 đã tham gia pư(đktc)
a)
Gọi X là khối lượng của CuO
Gọi Y là khối lượng của Fe3O4
Theo bài ra ta có :
X + Y + 31,2 ( g ) (1)
Y - X = 15,2 ( g ) (2)
Từ (1) và (2) \(\Rightarrow\)X = 8 ; Y = 23,2
\(\Rightarrow\) nCuO =\(\dfrac{nCuO}{MCuO}\)= \(\dfrac{8}{80}=0,1\left(mol\right)\)
\(\Rightarrow\) nFe2O3 = \(\dfrac{23,2}{232}\)= 0,1 ( mol )
PTHH1 : CuO + H2 \(\rightarrow\) Cu + H2
0,1 : 0,1 : 0,1 : 0,1 ( mol)
PTHH2 : Fe3O4 + 4H2 \(\rightarrow\) 3Fe + 4H2
0,1 : 0,4 : 0,3 : 0,4 (mol)
\(\Rightarrow\) mCu = nCu . MCu = 0,1 . 64 = 6,4 (g)
\(\Rightarrow\) mFe = nFe . MFE = 0,3 . 56 = 16,8 (g)
b) \(\Rightarrow\)nH2 = nH2(PTHH1) + nH2(PTHH2)
\(\Rightarrow\)nH2 = 0,1+ 0,4 = 0,5 ( mol)
\(\Rightarrow\) VH2 = 0,5 . 22,4 = 11,2 ( l)
Đúng 0
Bình luận (0)
Có một hỗn hợp gồm 60% F e 2 O 3 và 40% CuO. Người ta dùng H 2 ( dư) để khử 20g hỗn hợp đó. Tính khối lượng Fe và khối lượng Cu thu được sau phản ứng.
Có 48(g) hỗn hợp gồm CuO và Fe3O4 với tỉ lệ khối lượng là:mFe2O3:mCuO= 3:1.Người ta dùng H2 để khử hỗn hợp đó.
a)Khối lượng Fe,Cu thu được.
b)Thể tích H2(đktc)đã tham gia pư
mCuO=\(48.\dfrac{1}{4}=12\left(gam\right)\)\(\Rightarrow m_{Fe_3O_4}=48-12=36\left(gam\right)\)
a)PTHH:CuO+H2\(\underrightarrow{t^0}\)H2O+Cu(1)
Fe3O4+4H2\(\underrightarrow{t^0}\)4H2O+3Fe(2)
Theo PTHH(1):80 gam CuO tạo ra 64 gam Cu và cần 22,4 lít H2
Vậy 12 gam CuO tạo ra 9,6 gam Cu và cần 3,36 lít H2
Theo PTHH(2):232 gam Fe3O4 tạo ra 168 gam Fe và cần 89,6 lít H2
Vậy:36 gam Fe3O4 tạo ra 26 gam Fe và cần 13,9 lít H2
\(\Rightarrow m_{Cu}=9,6\left(gam\right);m_{Fe_3O_4}=26\left(gam\right)\)
c)Từ câu b \(\Rightarrow V_{H_2}=13,9+89,6=103,5\left(lít\right)\)
Đúng 0
Bình luận (2)