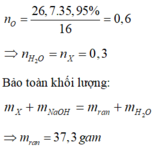cho 23,4 gam Al(OH)3 tác dụng với 200 ml dung dịch NaOH 2M , sau phản ứng thu được bao nhiêu gam NaAlO2 và bao nhiêu gam NaOH ?

Những câu hỏi liên quan
cho 23,4 gam Al(OH)3 tác dụng với 200 ml dung dịch NaOH 2M , sau phản ứng thu được bao nhiêu gam NaAlO2 và bao nhiêu gam NaOH ?
nAl(OH)3=\(\dfrac{23.4}{78}\)=0.3(mol)
nNaOH=0.2*2=0.4(mol)
Al(OH)3+NaOH---->NaAlO2+2H2O
mol:\(\dfrac{0.3}{1}\)<\(\dfrac{0.4}{1}\) => NaOH dư
Al(OH)3+NaOH---->NaAlO2+2H2O
mol:0.3--->0.3--------->0.3 (mol)
mNaAlO2=82*0.3=24.6(g)
nNaOH dư=0.4-0.3=0.1(mol)
mNaOH thu được=40*0.1=4(g)
Đúng 0
Bình luận (0)
cho 23,4 gam Al(OH)3 tác dụng với 250 ml dung dịch NaOH 2M , sau phản ứng thu được bao nhiêu gam NaAlO2 và bao nhiêu gam NaOH ?
Một amino axit X chứa 1 nhóm NH2 và 1 nhóm COO, trong đó oxi chiếm 35,955% khối lượng. Lấy 26,7 gam X cho tác dụng với 200 ml dung dịch NaOH 2M. Cô cạn dung dịch sau phản ứng thu được bao nhiêu gam rắn khan? A. 37,30 gam B. 33,30 gam C. 44,40 gam D. 36,45 gam
Đọc tiếp
Một amino axit X chứa 1 nhóm NH2 và 1 nhóm COO, trong đó oxi chiếm 35,955% khối lượng. Lấy 26,7 gam X cho tác dụng với 200 ml dung dịch NaOH 2M. Cô cạn dung dịch sau phản ứng thu được bao nhiêu gam rắn khan?
A. 37,30 gam
B. 33,30 gam
C. 44,40 gam
D. 36,45 gam
Đáp án A
Từ %O=> MX= 89 => nX=0.3 mol , nNaOH = 0.4 mol
BTKL : 26.7+ 0.4*40=m +0.3*18 => m =37.3 gam
Đúng 0
Bình luận (0)
Một amino axit X chứa 1 nhóm NH2 và 1 nhóm COO, trong đó oxi chiếm 35,955% khối lượng. Lấy 26,7 gam X cho tác dụng với 200 ml dung dịch NaOH 2M. Cô cạn dung dịch sau phản ứng thu được bao nhiêu gam rắn khan? A. 37,30 gam. B. 33,30 gam. C. 44,40 gam. D. 36,45 gam.
Đọc tiếp
Một amino axit X chứa 1 nhóm NH2 và 1 nhóm COO, trong đó oxi chiếm 35,955% khối lượng. Lấy 26,7 gam X cho tác dụng với 200 ml dung dịch NaOH 2M. Cô cạn dung dịch sau phản ứng thu được bao nhiêu gam rắn khan?
A. 37,30 gam.
B. 33,30 gam.
C. 44,40 gam.
D. 36,45 gam.
Cho 200 ml dung dịch H2SO4 1M tác dụng với 300 ml dung dịch NaOH 2M, sau phản ứng thu được dung dịch X.
(a) Viết các PTHH xảy ra.
(b) Nếu cho mẩu quỳ tím vào dung dịch X thì có hiện tượng gì? Giải thích.
(c) Cô cạn dung dịch X thu được bao nhiêu gam chất rắn khan?
Ta có nH2SO4 = 0,2 . 1,5 = 0,3 ( mol )
nBa(OH)2 = 0,3 . 0,8 = 0,24 ( mol )
H2SO4 + Ba(OH)2 → BaSO4 + 2H2O
0,3...........0,24
⇒Lập tỉ số
Đúng 2
Bình luận (0)
1. Cho 3,42 gam Al2(SO4)3 tác dụng với 200 ml dung dịch NaOH, sau phản ứng thu được 0,78 gam kết tủa. Nồng độ mol nhỏ nhất của dung dịch NaOH đã dùng là2. Rót V ml dung dịch NaOH 2M vào cốc đựng 300 ml dung dịch Al2(SO4)3 0,25M thu được kết tủa. Lọc kết tủa rồi nung đến khối lượng ko đổi được 5,1 gam chất rắn. Giá trị lớn nhất của V là3. Cho 150 ml dung dịch KOH 1,2M tác dụng với 100 ml dung dịch AlCl3 nồng độ x mol/l, thu được dung dịch Y và 4,68 gam kết tủa. Loại bỏ kết tủa, thêm tiếp 175 ml d...
Đọc tiếp
1. Cho 3,42 gam Al2(SO4)3 tác dụng với 200 ml dung dịch NaOH, sau phản ứng thu được 0,78 gam kết tủa. Nồng độ mol nhỏ nhất của dung dịch NaOH đã dùng là
2. Rót V ml dung dịch NaOH 2M vào cốc đựng 300 ml dung dịch Al2(SO4)3 0,25M thu được kết tủa. Lọc kết tủa rồi nung đến khối lượng ko đổi được 5,1 gam chất rắn. Giá trị lớn nhất của V là
3. Cho 150 ml dung dịch KOH 1,2M tác dụng với 100 ml dung dịch AlCl3 nồng độ x mol/l, thu được dung dịch Y và 4,68 gam kết tủa. Loại bỏ kết tủa, thêm tiếp 175 ml dung dịch KOH 1,2M vào Y, thu được 2,34 gam kết tủa. Giá trị của x là:
Làm 3 bài trên nhưng không dùng phương trình ion, dùng pthh với ạ
1) \(n_{Al\left(OH\right)_3}=\dfrac{0,78}{78}=0,01\left(mol\right)\)
PTHH: \(Al_2\left(SO_4\right)_3+6NaOH\rightarrow3Na_2SO_4+2Al\left(OH\right)_3\)
0,03<----------------------0,01
=> nNaOH min = 0,03 (mol)
=> \(C_{M\left(NaOH\right)}=\dfrac{0,03}{0,2}=0,15M\)
2) \(n_{Al_2O_3}=\dfrac{5,1}{102}=0,05\left(mol\right)\)
\(n_{Al_2\left(SO_4\right)_3}=0,3.0,25=0,075\left(mol\right)\)
PTHH: \(6NaOH+Al_2\left(SO_4\right)_3\rightarrow3Na_2SO_4+2Al\left(OH\right)_3\)
0,45<------0,075-------------------------->0,15
\(NaOH+Al\left(OH\right)_3\rightarrow NaAlO_2+2H_2O\)
0,05<----0,05
\(2Al\left(OH\right)_3\underrightarrow{t^o}Al_2O_3+3H_2O\)
0,1<-------0,05
=> nNaOH max = 0,5 (mol)
=> \(V_{dd}=\dfrac{0,5}{2}=0,25\left(l\right)=250\left(ml\right)\)
3)
\(n_{KOH\left(1\right)}=0,15.1,2=0,18\left(mol\right)\)
\(n_{Al\left(OH\right)_3\left(1\right)}=\dfrac{4,68}{78}=0,06\left(mol\right)\)
\(n_{AlCl_3}=0,1.x\left(mol\right)\)
Do khi cho KOH tác dụng với dd Y xuất hiện kết tủa
=> Trong Y chứa AlCl3 dư
PTHH: \(3KOH+AlCl_3\rightarrow3KCl+Al\left(OH\right)_3\)
0,18---->0,06----------------->0,06
\(n_{KOH\left(2\right)}=0,175.1,2=0,21\left(mol\right)\)
\(n_{Al\left(OH\right)_3\left(2\right)}=\dfrac{2,34}{78}=0,03\left(mol\right)\)
PTHH: \(3KOH+AlCl_3\rightarrow3KCl+Al\left(OH\right)_3\)
(0,3x-0,18)<--(0,1x-0,06)------->(0,1x-0,06)
\(KOH+Al\left(OH\right)_3\rightarrow KAlO_2+2H_2O\)
(0,1x-0,09)<-(0,1x-0,09)
=> \(\left(0,3x-0,18\right)+\left(0,1x-0,09\right)=0,21\)
=> x = 1,2
Đúng 8
Bình luận (2)
Cho 19,8 gam hỗn hợp hai axit HCOOH và CH3COOH (có tỉ lệ mol tương ứng 3 : 1) tác dụng với 20,7 gam rượu etylic, hiệu suất các phản ứng este hóa là 75%. a. Tính khối lượng este thu được sau phản ứng. b. Đem hỗn hợp sau phản ứng este hóa cho tác dụng hết với 250 ml dung dịch NaOH 2M, kết thúc phản ứng cô cạn dung dịch thì thu được bao nhiêu chất rắn khan.
Đọc tiếp
Cho 19,8 gam hỗn hợp hai axit HCOOH và CH3COOH (có tỉ lệ mol tương ứng 3 : 1) tác dụng với 20,7 gam rượu etylic, hiệu suất các phản ứng este hóa là 75%.
a. Tính khối lượng este thu được sau phản ứng.
b. Đem hỗn hợp sau phản ứng este hóa cho tác dụng hết với 250 ml dung dịch NaOH 2M, kết thúc phản ứng cô cạn dung dịch thì thu được bao nhiêu chất rắn khan.
Câu 6.
a) Cho 200 ml dung dịch CH3COOH 2M tác dụng vừa đủ với dung dịch NaOH. Tính khối lượng NaOH tham gia phản ứng.
b) Cho 60 gam CH3COOH tác dụng với 100 gam C2H5OH thu được 55 gam CH3COOC2H5 . Tính hiệu suất của phản ứng trên.
a) nCH3COOH= 0,4(mol)
PTHH: CH3COOH + NaOH -> CH3COONa + H2O
0,4____________0,4(mol)
=> mNaOH=0,4. 40=16(g)
b) nCH3COOH= 1(mol)
nC2H5OH= 100/46= 50/23(mol)
Vì : 1/1< 50/23 :1
=> C2H5OH dư, CH3COOH hết, tính theo nCH3COOH.
PTHH: CH3COOH + C2H5OH \(⇌\) CH3COOC2H5 + H2O (đk: H+ , nhiệt độ)
Ta có: nCH3COOC2H5(thực tế)= 0,625(mol)
Mà theo LT: nCH3COOC2H5(LT)= nCH3COOH=1(mol)
=>H= (0,625/1).100=62,5%
Đúng 1
Bình luận (0)
cho m gam al tác dụng với dd hcl 2m. sau phản ứng cho dung dịch tác dụng với 0,3 mol naoh ( đủ ) hỏi vhcl tham gia phản ứng là bao nhiêu
Ý bạn là tìm \(V_{dd_{HCl}}\) đúng không?
\(PTHH:2Al+6HCl\rightarrow2AlCl_3+3H_2\uparrow\\ AlCl_3+3NaOH\rightarrow Al\left(OH\right)_3\downarrow+3NaCl\\ \Rightarrow n_{AlCl_3}=\dfrac{1}{3}n_{NaOH}=0,1\left(mol\right)\\ \Rightarrow n_{HCl}=3n_{AlCl_3}=0,3\left(mol\right)\\ \Rightarrow V_{dd_{HCl}}=\dfrac{0,3}{2}=0,15\left(l\right)\)
Đúng 2
Bình luận (0)