Ngâm một vật bằng Cu có kl10g trong 250g dung dịch AgNO3 4%. Khi lấy vạt ra thì lượng AgNO3 trong dung dịch giảm 17%. Tinh kl vật sau phản ứng

Những câu hỏi liên quan
Ngâm một vật bằng đồng có khối lượng 10g trong 250g dung dịch AgNO3 4% khi lấy vật ra thì khối lượng AgNO3 trong dung dịch giảm 17%. Xác định khối lượng của vật sau phản ứng.
Khối lượng vật sau phản ứng = 10 + 0,01 x 108 – 0,005 x 64 = 10,76 g
Đúng 0
Bình luận (0)
Ngâm một vật bằng đồng có khối lượng 12g trong 250g dung dịch AgNO3 4% . Khi lấy vật ra thì lượng AgNO3 trong dung dịch giảm 17% . Khối lượng của vật sau phản ứng là (Cu = 64, Ag = 108, N = 14, O = 16)
A. 12,76 gam.
B. 10,76 gam.
C. 12,67 gam.
D. 10,67 gam.
\(n_{AgNO_3}=\dfrac{250.4}{100.170}=\dfrac{1}{17}\left(mol\right)\)
=> \(n_{AgNO_3\left(pư\right)}=\dfrac{1}{17}.17\%=0,01\left(mol\right)\)
PTHH: Cu + 2AgNO3 --> Cu(NO3)2 + 2Ag
____0,005<--0,01--------------------->0,01
=> m = 12 - 0,005.64 + 0,01.108 = 12,76(g)
=> A
Đúng 1
Bình luận (0)
Ngâm một vật bằng đồng có khối lượng 10g trong 250g dung dịch AgNO3 4% khi lấy vật ra thì khối lượng AgNO3 trong dung dịch giảm 17%.
Viết phương trình hóa học của phản ứng và cho biết vai trò các chất tham gia phản ứng.
2AgNO3 + Cu → Cu(NO3)2 + 2Ag
Phương trình ion thu gọn: Cu + 2Ag+ → Cu2+ + 2Ag↓
AgNO3 là chất oxi hóa, Cu là chất khử.
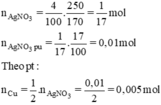
Áp dụng tăng giảm khối lượng
Đúng 0
Bình luận (0)
Ngâm một vật bằng Cu có khối lượng 15g trong 340g dung dịch AgNO3 6%. Sau một thời gian lấy vật ra thấy khối lượng AgNO3 trong dung dịch giảm 25%. Khối lượng của vật sau phản ứng là
A. 15,26 g
B. 17,28 g
C. 16,15 g
D. 18,16g
Khối lượng của AgNOg trong dung dịch là:
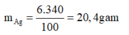
Phương trình phản ứng xảy ra:
![]()
Cứ 1 mol Cu phản ứng với 2 mol AgNO3, sinh ra 1 mol Cu(NO3)2 và 2 mol Ag, khối lượng kim loại tăng
![]()
Khối lượng AgNO3 đã tham gia phản ứng:
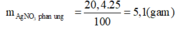
Từ (1)=> Số mol Cu đã phản ứng:
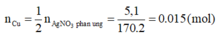
=> Khối lượng của vật sau phản ứng: m = 15 + 152.0,015 = 17,28 (gam).
Đáp án B.
Đúng 0
Bình luận (0)
Bài 5: Ngâm một vật bằng đồng có khối lượng 50 gam vào 250 gam dung dịch AgNO3 6%. Khi lấy vật ra thì khối lượng AgNO3 trong dung dịch giảm 17%.
a) Xác đinh khối lượng của vật lấy ra sau phản ứng. Biết toàn bộ lượng bạc sinh ra đều bám vào vật.
b) Tính nồng độ phần trăm các chất có trong dung dịch sau phản ứng khi lấy vật ra.
Đọc tiếp
Bài 5: Ngâm một vật bằng đồng có khối lượng 50 gam vào 250 gam dung dịch AgNO3 6%. Khi lấy vật ra thì khối lượng AgNO3 trong dung dịch giảm 17%.
a) Xác đinh khối lượng của vật lấy ra sau phản ứng. Biết toàn bộ lượng bạc sinh ra đều bám vào vật.
b) Tính nồng độ phần trăm các chất có trong dung dịch sau phản ứng khi lấy vật ra.
PT: \(Cu+2AgNO_3\rightarrow Cu\left(NO_3\right)_2+2Ag\)
a, m AgNO3 (pư) = 250.17%.6% = 2,55 (g)
\(\Rightarrow n_{AgNO_3\left(pư\right)}=\dfrac{2,55}{170}=0,015\left(mol\right)\)
Theo PT: nCu (pư) = 1/2nAgNO3 = 0,0075 (mol)
nAg = nAgNO3 = 0,015 (mol)
⇒ m vật lấy ra = 50 - mCu (pư) - mAg = 51,14 (g)
b, Ta có: m dd sau pư = 0,0075.64 + 250 - 0,015.108 = 248,86 (g)
Theo PT: nCu(NO3)2 = 1/2nAgNO3 = 0,0075 (mol)
\(\Rightarrow C\%_{Cu\left(NO_3\right)_2}=\dfrac{0,0075.188}{248,86}.100\%\approx0,57\%\)
\(C\%_{AgNO_3}=\dfrac{250.6\%-2,55}{248,86}.100\%\approx5\%\)
Đúng 1
Bình luận (0)
Ngâm một vật bằng đồng có khối lượng 5g trong 250g dung dịch AgNO3 8%. Sau một thời gian, lấy vật ra và kiểm tra thấy lượng AgNO3 trong dung dịch đầu giảm 85%.
a) Tính khối lượng vật sau phản ứng? Biết bạc sinh ra bám vào vật.
b) Tính nồng độ % của các chất hòa tan trong dung dịch sau khi lấy vật ra.
LẸ . LÁT ĐI HỌC R
Ngâm một vật bằng đồng có khối lượng 50gam vào 250 gam dung dịch AgNO3 6% khi Lấy vật ra thấy khối lượng AgNO3 trong dung dịch giảm 17%
a) Hãy xác định khối lượng của vật lấy ra sau phản ứng biết Ag sinh ra Bám vào vật
b) tính nồng độ phần trăm của chất có trong dung dịch sau phản ứng
a./ Khối lượng AgNO3 trong dd ban đầu: m(AgNO3) = 250.6% = 15g
Khối lượng AgNO3 pư: m(AgNO3 pư) = 17%.15 = 2,55g
→ n(AgNO3) = 2,55/170 = 0,015mol
2AgNO3 + Cu → 2Ag + Cu(NO3)2
0,015___0,0075_0,015__0,0075
Khối lượng của vật lấy ra sau pư:
m = 50 + m(Ag) - m(Cu pư) = 50 + 0,015.108 - 0,0075.64 = 51,14g
b./ Khối lượng các chất có trong dd sau pư:
m[Cu(NO3)2] = 0,0075.188 = 1,41g
m(AgNo3 dư) = m(AgNO3) - m(AgNO3 pư) = 15 - 2,55 = 12,45g
Khối lượng dd thu được:
m(dd) = m(dd AgNO3) + m(Cu pư) - m(Ag) = 250 + 0,0075.64 - 0,015.108 = 248,86g
Thành phần % các chất có trong dung dịch
%AgNO3 dư = 12,45/248,86 .100% = 5%
%Cu(NO3)2 = 1,41/248,86 .100% = 0,57%
Đúng 1
Bình luận (0)
Ngâm một thanh kim loại bằng đồng có khối lượng 10gam trong 250 gam dung dịch 4%. Khi lấy vật ra khỏi dd thì khối lượng AgNO3 trong dung dịch giảm 17%. Khối lựợng của thanh kim loại sau phản ứng là? A. 10,76 g B. 10,67 g C. 9,67 g D. 9,76 g
Đọc tiếp
Ngâm một thanh kim loại bằng đồng có khối lượng 10gam trong 250 gam dung dịch 4%. Khi lấy vật ra khỏi dd thì khối lượng AgNO3 trong dung dịch giảm 17%. Khối lựợng của thanh kim loại sau phản ứng là?
A. 10,76 g
B. 10,67 g
C. 9,67 g
D. 9,76 g
Ngâm 1 vật bằng đồng có khối lượng 10g trong 250g dung dịch AgNO3 4%. Khi lấy vật ra khỏi dung dịch thì khối lượng AgNO3 trong dung dịch giảm 17%. Khối lượng của vật sau phản ứng là bao nhiêu?
\(n_{AgNO_3}=\dfrac{250.4}{100.170}=\dfrac{1}{17}\left(mol\right)\)
Sau phản ứng, lượng AgNO3 giảm đi là khối lượng AgNO3 đã tác dụng \(\Rightarrow n_{AgNO_3}\left(pứ\right)=17\%.\dfrac{1}{17}=0,01\left(mol\right)\) \(Cu\left(0,005\right)+2AgNO_3\left(0,01\right)\rightarrow Cu\left(NO_3\right)_2+2Ag\left(0,01\right)\) Theo PTHH: \(\left\{{}\begin{matrix}n_{Cu\left(tan-ra\right)}=0,005\left(mol\right)\\n_{Ag\left(tao-thanh\right)}=0,01\left(mol\right)\end{matrix}\right.\)\(\Rightarrow\left\{{}\begin{matrix}m_{Cu\left(tan-ra\right)}=0,32\left(g\right)\\m_{Ag\left(tao-thanh\right)}=1,08\left(g\right)\end{matrix}\right.\) => Sau phản ứng khối lượng thanh kim loại tăng: \(=1,08-0,32=0,76\left(g\right)\) \(\Rightarrow m_{c.ran-sau-pứ}=20+0,76=10,76\left(g\right)\)
Đúng 0
Bình luận (0)
PTHH: \(Cu+2AgNO_3\rightarrow Cu\left(NO_3\right)_2+2Ag\)
1 2 2
0.005 0.01 0.01(mol)
\(m_{AgNO3}=\frac{250.4}{100}=10\left(g\right)\)
\(\Rightarrow n_{AgNO3\left(pư\right)}=\frac{10.17}{100.170}=0.01\left(mol\right)\)
Khối lượng vật sau phản ứng:
\(10+\left(108.0,01\right)-\left(64.0,005\right)=10,76\left(g\right)\)
Đúng 0
Bình luận (0)



















