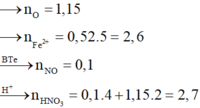Những câu hỏi liên quan
cho dung dịch hcl 2m tác dụng vừa đủ với 30g hh A gồm fe feo feco3 thấy thoát ra 6,72 lít một hh khí và tạo ra 50,8g muối fecl2.
a) tính thể tích hcl đã dùng
b) tính % theo khối lượng mỗi chất trong A
thực hiện phản ứng nhiệt nhôm hh gồm Fe2O3 và Al. Sau phản ứng hoàn toàn, nghiền nhỏ hh sản phẩm, trộn đều và chia thành 2 phần. Phần 1 cho tác dụng với dung dịch NaOH dư thì có 4,48l H2 thoát ra. Chất rắn còn lại có khối lượng bằng 44.8% khối lượng phần 1. Phần 2 tác dụng hết với dd HCl thì giải phóng 13.44l H2. khối lượng hh ban đầu là
Vì các phản ứng hoàn toàn mà khi cho Y + NaOH ----> H2 chứng tỏ Al dư, Fe2O3 chuyển hết thành Fe. Vậy trong Y có chứa Al: 0,03 mol ( nH2 = 3/2nAl); nFe = 0,06 mol (mFe = m rắn = 3,36 g)
Từ pư: 2Al + Fe2O3 ---> Al2O3 + 2Fe => nFe2O3 = nAl2O3, mà nFe2O3 = nFe/2 => nAl2O3 = 0,03 mol
m phần 1 = 7,23 g => m phần 2 = 21,69 g. Hay p2 = 3 p1
=> Trong phần 2 có: Al: 0,09 mol; Fe: 0,18 mol; Al2O3: 0,09 mol
Bảo toàn e (giả sử chỉ tạo Fe2+, vì ta chưa biết sản phẩm có Fe3+ hay không): 3nNO < 3nAl + 2nFe => có NH4+
Gọi số mol Fe2+: x, Fe3+: y, NH4+: z
=> Bảo toàn electron: 0,09.3 + 2x + 3y = 0,17.3 + 8z
x + y = 0,18 (bảo toàn Fe)
1,52 = 0,09.3.2 ( nH+ phản ứng với Al2O3) + 0,17.4 + 10z
=> x = 0,06; y = 0,12; z = 0,03
Bảo toàn N: nNO3- = nHNO3 - nNO - nNH4+ = 1,32 mol
=> m = 21,69 + NO3- = 103,53 g
Đúng 0
Bình luận (0)
Hòa tan hoàn toàn 57,6 gam hỗn hợp A gồm fe3o4, fe203, feo, fe vào dung dịch hcl cần 360 gam dung dich hcl 18,25% để tác dụng vừa đủ . Sau phản ứng thu đưực V(l) h2 và dung dich b. Cho toàn bộ h2 sinh ra tác dụng với cuo dư ở nhiệt độ cao thu được hỗn hợp chất rắn có khối lương nhỏ hơn khối lượng cuo ban đầu là 3,2 gam a, nếu cô cạn dung dịch b thì thu bao nhiêu gam muối khan b, nếu hỗn hợp a ban đầu có tỉ lệ mol n(fe2o3) : n ( feo) 1: 1. Tính C% các chất trong dung dich b c.Hỗn hợp X cũng chứa...
Đọc tiếp
Hòa tan hoàn toàn 57,6 gam hỗn hợp A gồm fe3o4, fe203, feo, fe vào dung dịch hcl cần 360 gam dung dich hcl 18,25% để tác dụng vừa đủ . Sau phản ứng thu đưực V(l) h2 và dung dich b. Cho toàn bộ h2 sinh ra tác dụng với cuo dư ở nhiệt độ cao thu được hỗn hợp chất rắn có khối lương nhỏ hơn khối lượng cuo ban đầu là 3,2 gam
a, nếu cô cạn dung dịch b thì thu bao nhiêu gam muối khan
b, nếu hỗn hợp a ban đầu có tỉ lệ mol n(fe2o3) : n ( feo) = 1: 1. Tính C% các chất trong dung dich b c.Hỗn hợp X cũng chứa fe304, fe2o3, feo, fe. Nếu dùng 100g X cho tác dụng với 2(l) dd HCL 2M.Chứng minh rằng hh X tan hết
a, nếu cô cạn dung dịch b thì thu bao nhiêu gam muối khan
b, nếu hỗn hợp a ban đầu có tỉ lệ mol n(fe2o3) : n ( feo) = 1: 1. Tính C% các chất trong dung dich b c.Hỗn hợp X cũng chứa fe304, fe2o3, feo, fe. Nếu dùng 100g X cho tác dụng với 2(l) dd HCL 2M.Chứng minh rằng hh X tan hết
Fe3O4 + 8HCl --> FeCl2 + 2FeCl3 + 4H2O
_a_______8a______a_____2a______4a_
Fe2O3 + 6HCl --> 2FeCl3 + 3H2O
_b______6b_______2b_____3b_
FeO + 2HCl --> FeCl2 + H2O
_c____2c_______c______c_
Fe + 2HCl --> FeCl2 + H2
_d___2d________d________d_
H2 + CuO --> Cu + H2O
_d____d_____d_____d_
nCuO = 3.2 / 80 = 0.04
=> d = 0.04
mHCl = 360 * 18.25 / 100 = 65.7 (g)
nHCl = 65.7 / 36.5 = 1.8 (mol)
=> 8a + 6b + 2c + 2d = 1.8
=> 8a + 6b + 2c + 0.08 = 1.8
=> 8a + 6b + 2c = 1.72
=> 4a + 3b + c = 0.86
a)
theo đlbtkl ta có
mHCl + mhh = mmuối + mH2O + mH2
65.7 + 57.6 = mmuối + 0.86 * 18 + 0.04 * 2
=> mmuối = 107.74 (g)
b) Fe3O4 + 8HCl --> FeCl2 + 2FeCl3 + 4H2O
_a_______8a______a_____2a______4a_
Fe2O3 + 6HCl --> 2FeCl3 + 3H2O
_b______6b_______2b_____3b_
FeO + 2HCl --> FeCl2 + H2O
_b____2b_______b______b_
Fe + 2HCl --> FeCl2 + H2
0.2__0.4_______0.2____0.2
nH2 = nFe = 0.2
232a + 232b =57.6-0.2X56
8a + 8b = 1.8-0.2X2
vô nghiệm vì nFe2O3 =nFeO tuong đương 2ẩn cung M
Đúng 0
Bình luận (1)
cho 27,2 g hỗn hợp A gồm Fe và Fe2O3 tác dụng với dung dịch HCl 20% thu được 4,48 lít H2(đktc) với dd B tính
a) khối lượng mỗi chất trong hh A
b) khối lượng dung dịch HCl 20% cần dùng
c) nồng độ phần trăm các chất có trong dd b
Fe=56 H=1 Cl=35,5 O=16
PTHH: \(Fe+2HCl\rightarrow FeCl_2+H_2\uparrow\)
\(Fe_2O_3+6HCl\rightarrow2FeCl_3+3H_2O\)
a) Ta có: \(n_{H_2}=\dfrac{4,48}{22,4}=0,2\left(mol\right)=n_{Fe}\)
\(\Rightarrow m_{Fe}=0,2\cdot56=11,2\left(g\right)\) \(\Rightarrow m_{Fe_2O_3}=16\left(g\right)\)
b+c) Ta có: \(\left\{{}\begin{matrix}n_{Fe}=0,2\left(mol\right)\\n_{Fe_2O_3}=\dfrac{16}{160}=0,1\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow n_{HCl}=2n_{Fe}+6n_{Fe_2O_3}=1\left(mol\right)\) \(\Rightarrow m_{ddHCl}=\dfrac{36,5}{20\%}=182,5\left(g\right)\)
Mặt khác: \(n_{FeCl_2}=0,2\left(mol\right)=n_{H_2}=n_{FeCl_3}\) \(\Rightarrow\left\{{}\begin{matrix}m_{FeCl_2}=0,2\cdot127=25,4\left(g\right)\\m_{FeCl_3}=0,2\cdot162,5=32,5\left(g\right)\\m_{H_2}=0,2\cdot2=0,4\left(g\right)\end{matrix}\right.\)
\(\Rightarrow m_{dd}=m_{hhA}+m_{ddHCl}-m_{H_2}=209,3\left(g\right)\)
\(\Rightarrow\left\{{}\begin{matrix}C\%_{FeCl_2}=\dfrac{25,4}{209,3}\cdot100\%\approx12,14\%\\C\%_{FeCl_3}=\dfrac{32,5}{209,3}\cdot100\%\approx15,53\%\end{matrix}\right.\)
Đúng 3
Bình luận (0)
\(n_{H2}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\)
Pt : \(Fe+2HCl\rightarrow FeCl_2+H_2|\)
1 2 1 1
0,2 0,4 0,2 0,2
\(Fe_2O_3+6HCl\rightarrow2FeCl_3+3H_2O|\)
1 6 2 3
0,1 0,6 0,2
a) \(n_{Fe}=\dfrac{0,2.1}{1}=0,2\left(mol\right)\)
\(m_{Fe}=0,2.56=11,2\left(g\right)\)
\(m_{Fe2O3}=27,2-11,2=16\left(g\right)\)
b) Có : \(m_{Fe2O3}=16\left(g\right)\)
\(n_{Fe2O3}=\dfrac{16}{160}=0,1\left(mol\right)\)
\(n_{HCl\left(tổng\right)}=0,4+0,6=1\left(mol\right)\)
⇒ \(m_{HCl}=1.36,5=36,5\left(g\right)\)
\(m_{ddHCl}=\dfrac{36,5.100}{20}=182,5\left(g\right)\)
c) \(n_{FeCl2}=\dfrac{0,2.1}{1}=0,2\left(mol\right)\)
⇒ \(m_{FeCl2}=0,2.127=25,4\left(g\right)\)
\(n_{FeCl3}=\dfrac{0,6.2}{6}=0,2\left(mol\right)\)
⇒ \(m_{FeCl3}=0,2.162,5=32,5\left(g\right)\)
\(m_{ddspu}=27,2+182,5-\left(0,2.2\right)=209,3\left(g\right)\)
\(C_{FeCl2}=\dfrac{25,4.100}{209,3}=12,14\)0/0
\(C_{FeCl3}=\dfrac{32,5.100}{209,3}=15,53\)0/0
Chúc bạn học tốt
Đúng 0
Bình luận (0)
Hỗn hợp X gồm FeO, Fe2O3, Fe3O4, CuO. Hoà tan m gam hỗn hợp X trong dung dịch HCl vừa đủ thu được dung dịch Y chứa m + 63,25 gam chất tan. Dung dịch Y tác dụng với tối đa 0,52 mol KMnO4 trong môi trường H2SO4. Nếu cho m gam hỗn hợp X tác dụng với dung dịch HNO3 loãng dư (sản phẩm khử duy nhất là NO) thì số mol HNO3 tham gia phản ứng là A. 3,0 B. 2,8 C. 2,9 D. 2,7
Đọc tiếp
Hỗn hợp X gồm FeO, Fe2O3, Fe3O4, CuO. Hoà tan m gam hỗn hợp X trong dung dịch HCl vừa đủ thu được dung dịch Y chứa m + 63,25 gam chất tan. Dung dịch Y tác dụng với tối đa 0,52 mol KMnO4 trong môi trường H2SO4. Nếu cho m gam hỗn hợp X tác dụng với dung dịch HNO3 loãng dư (sản phẩm khử duy nhất là NO) thì số mol HNO3 tham gia phản ứng là
A. 3,0
B. 2,8
C. 2,9
D. 2,7
Giúp với ạ , mình cần gấp :(( Cho 6,8g hỗn hợp A gồm Mg và MgO tác dụng với dung dịch HCl dư, thu được 4,48 lit a. Viết phương trình phản ứng xảy ra khi (ở đktc) b. linh khỏi lượng mọi chất trong hỗn hợp A. a. Tinh thể tích dung dịch HCl 2M đu đe hòa tan 6,8g bỗn hợp A. ( Cho biết: Mg = 24. H = \; C!=354; O=16 )
\(a,Mg+2HCl\rightarrow MgCl_2+H_2\\ MgO+2HCl\rightarrow MgCl_2+H_2O\\ n_{Mg}=n_{H_2}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\\ \Rightarrow m_{Mg}=0,2.24=4,8\left(g\right)\\ \Rightarrow m_{MgO}=m_{hhA}-m_{Mg}=6,8-4,8=2\left(g\right)\\ c,n_{MgO}=\dfrac{2}{40}=0,05\left(mol\right)\\ n_{HCl}=2.\left(n_{Mg}+n_{MgO}\right)=2.\left(0,2+0,05\right)=0,5\left(mol\right)\\ \Rightarrow V_{ddHCl}=\dfrac{0,5}{2}=0,25\left(l\right)\)
Đúng 3
Bình luận (0)
Cho 70.7g hh Fe3O4 và ZnO tác dụng vừa đủ với H2 thu được chất rắn A gồm 2 kim loại.Cho toàn bộ chất rắn A tác dụng với dung dịch HCl 14,6% vừa đủ thu đc dung dịch B và 20,16l H2 đktc. a)Tính % khối lượng mỗi oxit trong hỗn hợp đầu.
b)Tính C% chất tan trong dung dịch B
a)
Gọi $n_{Fe_3O_4} = a(mol) ; n_{ZnO} = b(mol)$
Ta có : 232a + 81b = 70,7(1)
$Fe_3O_4 + 4H_2 \xrightarrow{t^o} 3Fe + 4H_2O$
$ZnO + H_2 \xrightarrow{t^o} Zn + H_2O$
$Fe + 2HCl \to FeCl_2 + H_2$
$Zn + 2HCl \to ZnCl_2 + H_2$
Theo PTHH :
$n_{H_2} = 3a + b = \dfrac{20,16}{22,4} = 0,9(mol)(2)$
Từ (1)(2) suy ra a = 0,2 ; b = 0,3
%\%m_{Fe_3O_4} = \dfrac{0,2.232}{70,7}.100\% = 65,6\%$
$\%m_{ZnO} = \dfrac{0,3.81}{70,7}.100\% = 34,4\%$
b)
$n_{HCl} = 2n_{H_2} = 1,8(mol) \Rightarrow m_{dd\ HCl} = \dfrac{1,8.36,5}{14,6\%} = 450(gam)$
$m_{dd\ B} = 0,2.3.56 + 0,3.65 + 450 - 0,9.2 = 501,3(gam)$
$C\%_{FeCl_2} = \dfrac{0,6.127}{501,3}.100\% = 15,2\%$
$C\%_{ZnCl_2} = \dfrac{0,3.136}{501,3}.100\% = 8,14\%$
Đúng 5
Bình luận (0)
Cho 15,72 gam hỗn hợp gồm Mg, Al và Zn tác dụng với oxi không khí, sau phản ứng thu được 23,88 gam hỗn hợp A gồm các oxit (MgO, Al2O3, ZnO). Hòa tan hoàn toàn A trong dung dịch HCl dư.
a) Tính số mol HCl đã tham gia phản ứng
b) Tính khối lượng muối clorua thu được.
a) Bảo toàn khối lượng : $n_{O(oxit)} = \dfrac{23,88 - 15,72}{16} = 0,51(mol)$
$2H^+ + O^{2-} \to H_2O$
$n_{HCl} = 2n_O = 0,51.2 = 1,02(mol)$
b)
$n_{Cl^-} = n_{HCl} = 1,02(mol)$
Suy ra :
$m_{muối} = m_{kim\ loại} + m_{Cl} = 15,72 + 1,02.35,5 =51,93(gam)$
Đúng 1
Bình luận (0)
Cho hỗn hợp X gồm Cu, Fe, Mg. Nếu cho 24,8g X tác dụng với Cl2 dư thì sau phản ứng thu được 75,4g hh muối khan. Mặt khác 0,3mol X tác dụng với dung dịch HCl dư thu được 5,6l h2. Tính thành phần phần trăm khối lượng Mg trong X